
索元生物历经7年,用其全基因组平台找到其在研产品DB104的生物标志物DGM4,且已证明了药物疗效。DB104的治疗群体是难治性抑郁症,其生物标志物DGM4在20%的难治性抑郁症患者中呈阳性。
近期索元已经开启对外授权合作的步伐。在5月的2024年DJS创新合作峰会上,索元生物将现场路演。
索元生物董事长罗文博士告诉研发客,公司正在和多家国际大药厂接洽合作事宜。这主要得益于DB104治疗难治性抑郁症(TRD)的关键性临床试验积极结果的公布。
从2012年成立至今12年,索元终于在首个产品上证明了其精准医疗“基因组学+新药”的研发理念。综观索元的模式,乃是引入临床“失败”新药,利用大数据组学打造的全基因组平台发现生物标志物(biomarker),通过新发现的biomarker筛选患者并重新开展临床试验,验证药物疗效。DB104在2b期临床中证明了对TRD的疗效,也证明了索元模式“biomarker+新药”的可行性。

索元生物董事长 罗文
罗文认为,如果DB104能成功上市,将是CNS领域第一个精准医疗的突破,类似于当年易瑞沙找到EGFR突变对于肺癌的意义。同时他表示,随着DB104的成功,将有计划重启IPO之路。
2017年,索元生物从BMS收购DB104时,研发客就采访过罗文(拓展阅读 索元获AMRI/BMS抗抑郁药全球授权,新模式见真章)。7年过后,索元不仅找到DB104的生物标志物DGM4,且已证明了药物疗效。
索元生物首席财务官陈纪正女士将在2024DJS代表公司路演。欢迎参与投票“谁是您最喜爱的路演公司”,投票时间从即日起至5月15日16:00,活动详情见本期次条。

或将申请有条件上市
研发客:请您介绍一下DB104治疗难治性抑郁症的具体研究情况、疗效如何?
罗文:这项关键性国际多中心临床研究ENLIGHTEN,共纳入197例患者,治疗6周后,在基因生物标志物DGM4阳性TRD患者中达到主要临床终点和所有次要终点。
其中在主要终点蒙哥马利-阿斯伯格抑郁量表(MADRS)总分相对于基线的变化方面,DB104用药组量表打分相比安慰剂组要低4.4分(p值0.0056), 将近40%的改善。单从MADRS评分看,DB104疗效与已获批治疗TRD的Spravato疗效相当。Spravato在56mg或84mg剂量的MADRS总分未超过4分。
并且DB104在安全性和使用便利性层面也具备优势。Spravato为鼻喷制剂,DB104是每天口服一次的片剂。
DB104在2017年被收购前,BMS已开展了11项1期、3项2b期大型临床试验,在上千例患者中验证了产品的安全性和耐受性。而Spravato改良于麻醉剂氯胺酮,上市后因安全性问题和滥用风险被FDA加以黑框警告,只能在医生监督下使用,给药两小时内须由专业人员陪护,一定程度上限制了其临床应用。
研发客:DB104将来上市将有多大的市场空间?销售峰值将达多少?
罗文:
DB104的治疗群体是难治性抑郁症。根据人民日报发布《2022年国民抑郁症蓝皮书》,中国患抑郁症人数超过9500万,其中难治性抑郁症患者占这近1亿例中的约三分之一。且DB104的生物标志物DGM4在20%的TRD患者中呈阳性。
20%的比例在生物标志物中已属于较高比例,一些肿瘤突变基因NTRK1、ROS1、RET等只有1%~2%比例,但不妨碍各大药厂投入重金研发。
从竞争对手看,Spravato于2019年在美国上市后销量持续上涨,2024年第一季度销售额达2.25亿美金,同比增长72%,成为年销售额超过十亿美金的“重磅炸弹”应该没有悬念。DB104从药物依从性、安全性各方面相较Spravato都有优势。我们预测DB104上市后全球的峰值销售可能会接近20亿美金。
研发客:索元生物对DB104进一步的规划是什么?
罗文:
产品的注册申请程序正在按部就班的进行中。DB104在2b期临床试验获得积极数据,我认为有可能尝试将其作为关键性临床(pivotal trial)结果向药监部门申请有条件上市的批准。
此外,我们也正在和一些国际大厂沟通合作事宜。近年国内药企授权出海浪潮正热,一些创新药甚至在临床前就被授权。而且大药厂有强势回归CNS趋势,仅2023年底就有两笔大额收购交易,即BMS以140亿美金收购Karuna、艾伯维87亿美金收购Cerevel。类似于DB104的first-in-class新药,也高度符合MNC的需求,尤其是DB104已获得2b期积极结果。
从索元公司本身看,自2012成立至今一直坚持精准医疗,需要有一个突破口证明我们的研发策略是正确的。如今DB104获得重大突破,索元短期将集中所有资源用于这款产品开发。
容易检测到的biomarker
研发客:可否请您以DB104为例,解释一下索元筛选biomarker的过程?
罗文:
我们收集了BMS针对DB104开展的两项2b期临床试验,在试验受试者的全血样本中提取DNA,对其中上百例样本进行了全基因组扫描,从上百万个位点中通过大数据分析、人工智能等多种计算工具,历经两年时间,最终发现了一个全新的生物标志物并将其命名为Denovo Genomic Marker4(DGM4)。
同时,为验证DGM4是预测疗效的药物基因组生物标志物,而非疾病预后生物标志物。我们在对照组受试者中开展相同的生物标志物分析,结果表明,DGM4是可以预测疗效的生物标志物。
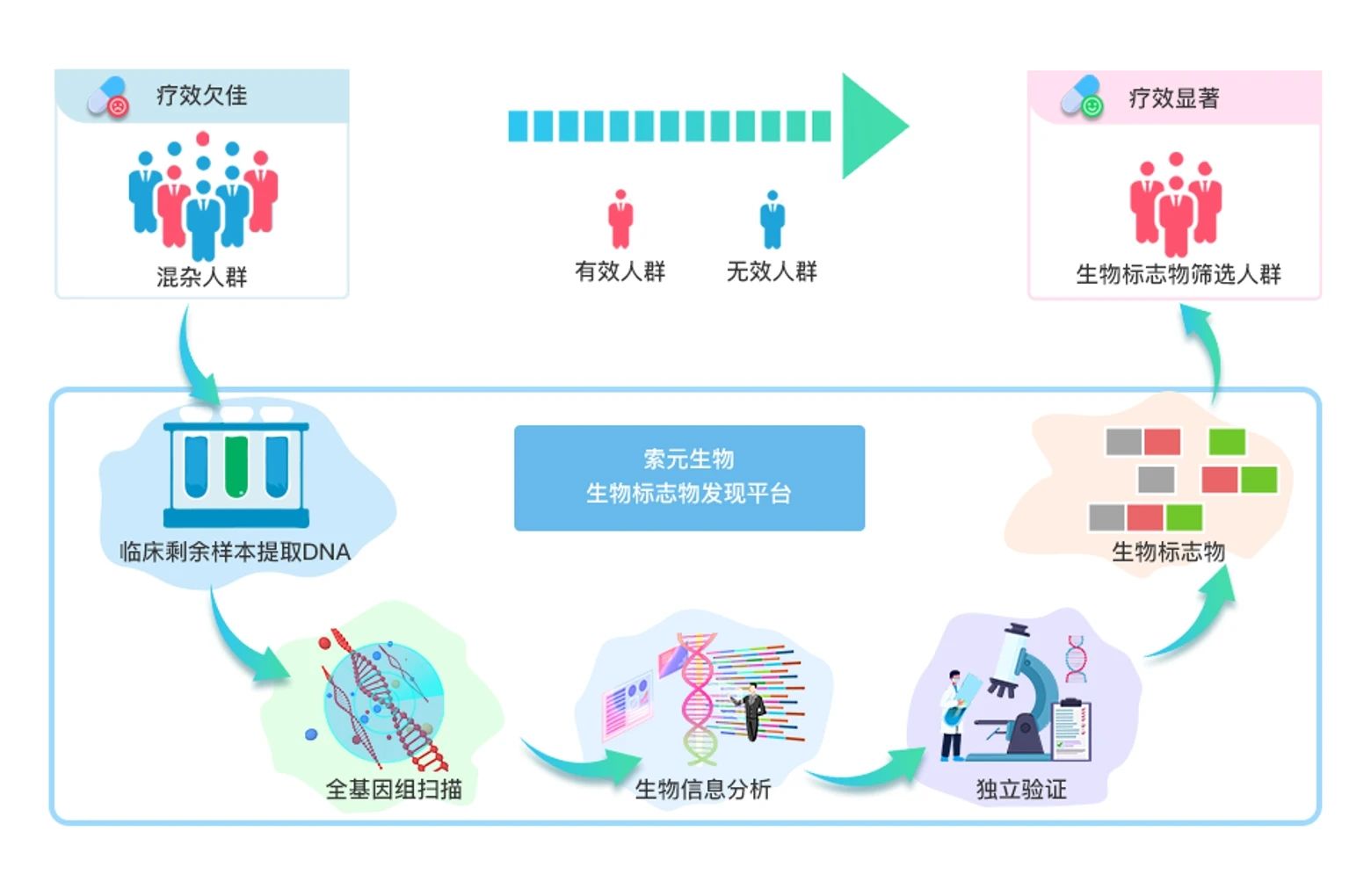
索元的生物标志物发现平台
研发客:索元生物标志物发现平台的特点和难点是什么?
罗文:
biomarker的寻找已历经3代,第一代的典型是易瑞沙,药物靶点就是biomarker;第二代的代表是结肠癌治疗药物Erbitux,靶点是EGFR,biomarker则是KRAS。KRAS在EGFR信号传导通路的下游,寻找起来相对复杂。一代和二代生物标志物都是从已有的科学文献推测,属于知识导向。
索元模式是第三代,不再局限于已知的生物信息传导通路,而是以数据导向的反向式检索,在全人类基因组中扫描。这也应对了索元生物的英文名称Denovo,完全从头发现,是从0到1的过程。
这是索元模式的核心也是难点。
人类基因组共有30亿个碱基对,从30亿位点中找出一两个跟药效相关的biomarker,无异于大海捞针。所以,尽管前期我们收购药物时进行了精挑细选,也不能保证每个项目都能找到biomarker。
例如DB103,自收购至今6年多时间仍未找到其生物标志物,但我们仍未放弃。索元管线的8款产品(见下图)中,有DB102、DB104和DB107发现了biomarker,分别是DGM1、DGM4和DGM7。
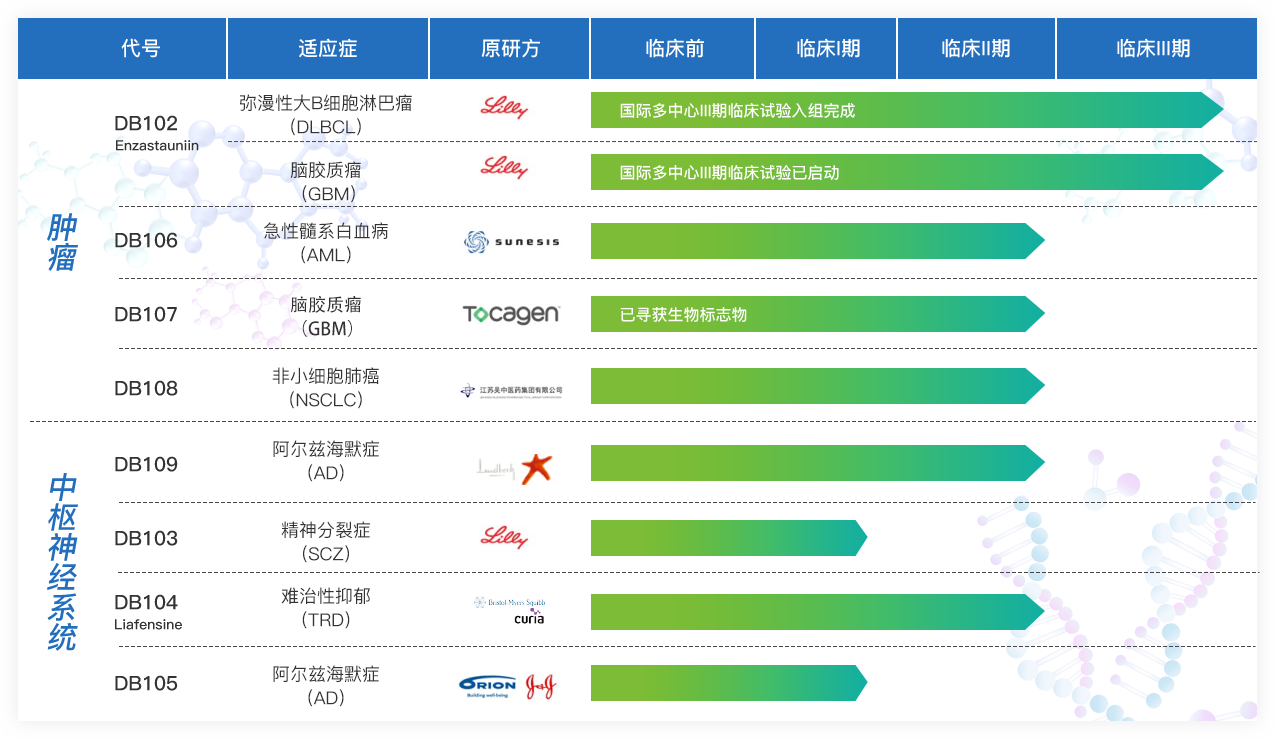
而一旦找到了biomarker,其应用就非常容易,普及率很高。以肿瘤生物标志物来做对比。通常抗肿瘤药的伴随诊断所针对的肿瘤突变基因,必须从肿瘤组织提取进行活检。而索元的biomarker是由SNP(单核苷酸多态性)组成的生物标志物,胚系SNP来自父母遗传,存在于全身各个细胞中,因此通过血液、甚至唾液就能检测,不需要获取病灶组织的样本。这种核酸检测简易快捷,方便临床患者,可以做到无创检测。
总结起来,找biomarker特别困难,但检测非常容易,这也是索元模式的一大特色。我们在DB104临床入组预筛时就使用过该方法,效率非常高。
上市之路可能重启
研发客:索元生物的研发理念需要哪些核心技术的融合?
罗文:
索元生物的研发模式,是一项跨学科的系统工程,将大数据基因组学应用于创新药研发,汇集了大数据、基因组学、分子生物学、临床各类学科人才。
而我本身的职业生涯也跨越了多个领域。本科是临床医学,研究生是分子生物学。工作后在蛋白激酶研发前沿公司Sugen(后被辉瑞收购),及Ligand Pharmaceutical从事新药研发。在人类基因组完成的2000年,加入当时最大的基因组学公司Incyte Genomics,对于基因组大数据的价值有切身感受。跨学科的职业经历,也让我认定要将基因组学应用于创新药的研发。
研发客:索元生物在关注哪些前沿技术,开展哪些技术合作?
罗文:
索元生物本身就是商业模式及技术平台超前的研发驱动公司,自然对各类创新技术充满兴趣,也正在和全球最前沿的公司和科研院所合作,不断提升自身研发水平。如,与Nurosene合作,利用AI技术NetraPlacebo帮助解决CNS临床试验中的安慰剂效应,提升试验成功率。
索元生物还与哈佛大学、清华大学的脑电波专家合作过。目前CNS临床终点大多是量表打分,例如抑郁症的汉密尔顿抑郁量表、蒙哥马利抑郁量表,而量表打分具有主观性,脑电波是客观的定量指标。不过这些都属于探索性实践合作,真正用于临床还需要获得监管部门的认可,在此之前的临床终点还是必须依据现有国际金标准。
研发客:2021年撤回科创板IPO申请后,索元还考虑上市吗?
罗文:
2021年中国药品市场热点是biosimilar和me-too药物,科创板、港股上市的大部分是这类药企。索元模式至今在全球范围内都没有同类企业,当时更是没有。公司独特的商业模式没有得到验证,这都是挑战。
而如今DB104临床成功,核心技术DGM生物标志物发现平台得到验证,我认为公司的上市之路已被打开。同时,DB104对外授权合作也在同步展开,产生的超额收益使公司能够提前进入投资丰收期。
而且药监部门一直在支持精准医疗开发。2021年底CDE发布了《生物标志物在抗肿瘤药物临床研发中应用的技术指导原则》,而后在ADC、PD-1/L1、基因治疗等各类指南中都提及生物标志物的重要性。
编辑 | 姚嘉
yao.jia@PharmaDJ.com