2024年10月13日,博瑞医药(688166.SH)自主研发的GLP-1(胰高血糖素样肽1)和GIP(葡萄糖依赖性促胰岛素多肽)受体双重激动剂——BGM0504注射液在非糖尿病的超重或肥胖受试者中开展的II期临床试验(CTR20233198)达到主要终点和关键次要终点,展现出良好的综合代谢获益。
BGM0504注射液已完成的II期临床试验(CTR20233198)是一项在非糖尿病的超重或肥胖受试者中多次给药的安全性、耐受性、PK/PD特征和有效性的随机、双盲、安慰剂平行对照的临床研究。本项研究共纳入了120例中国非糖尿病的超重或肥胖受试者,各组在体重、腰围、BMI等方面的基线特征基本均衡。II期临床试验初步结果显示,BGM0504注射液5 mg、10 mg、15 mg剂量组受试者,每周给药1次,给药26~30周(2~6周的剂量滴定期+目标剂量稳定治疗期24周)后的整体耐受性、安全性良好。各剂量组受试者在体重、腰围等核心减重指标方面均明显优于安慰剂组(p<0.0001),在次要疗评指标方面如心血管代谢风险指标(血压、血尿酸、甘油三酯/总胆固醇/低密度脂蛋白胆固醇等)、增加胰岛素敏感性的相关指标(空腹血糖/空腹胰岛素)、患者结局报告指标(体重对生活品质的影响量表)等较基线均有改善,且优于安慰剂组。
1、 核心减重指标完美达成,BGM0504注射液每周给药1次减重疗效强劲且起效快:
(1)体重
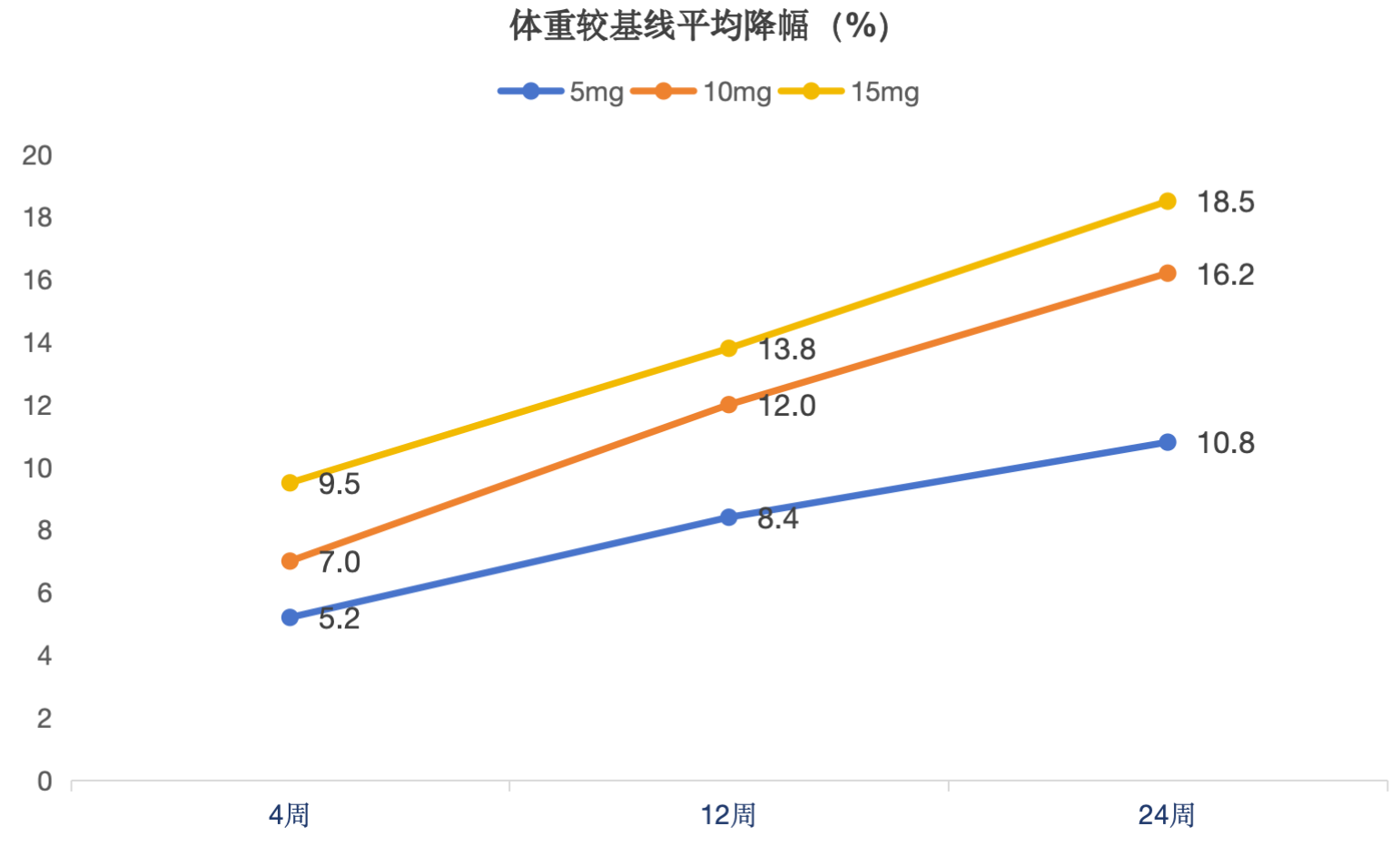
·在目标剂量给药第4周时,BGM0504注射液5mg组、10mg组、15mg组体重较基线平均降幅百分比(扣除安慰剂)分别为5.2%、7.0%和9.5%。
·目标剂量给药第12周时,BGM0504注射液5mg组、10mg组和15mg组体重较基线平均降幅百分比(扣除安慰剂)分别为8.4%、12.0%和13.8%。
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组体重较基线平均降幅百分比(扣除安慰剂)分别为10.8%、16.2%和18.5%;此外,目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg与安慰剂组空腹体重相对基线的变化百分比的95%置信区间分别为:[-12.93,-8.61]、[-19.20,-13.23]和[-23.02,-16.54],p值均小于0.0001且各组95%置信区间上限均小于0,各剂量组均优于安慰剂组。
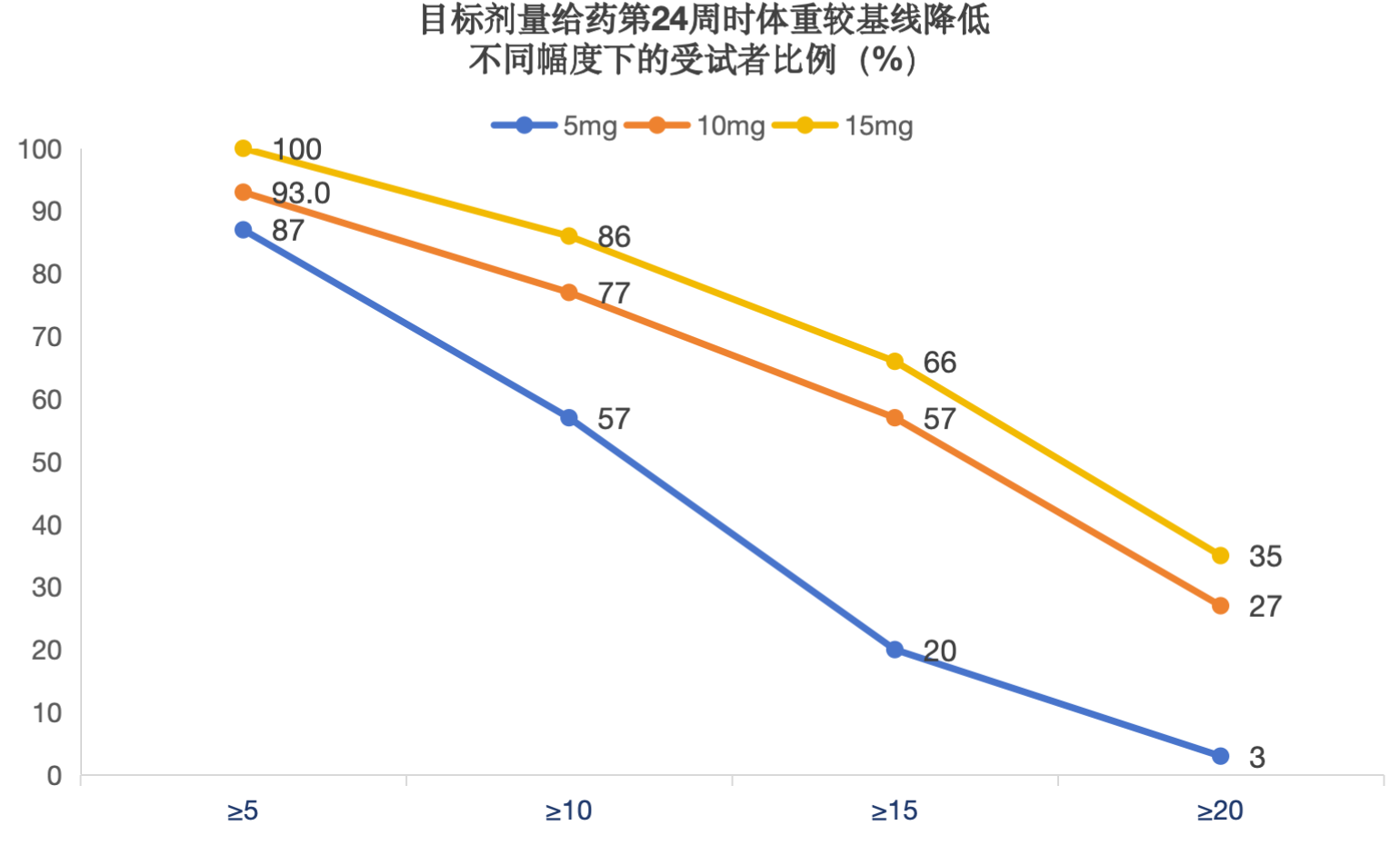
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组体重较基线降低≥5%的受试者比例分别为87%、93%和100%,体重较基线降低≥10%的受试者比例分别为57%、77%和86%,体重较基线降低≥15%的受试者比例分别为20%、57%和66%,体重较基线降低≥20%的受试者比例分别为3%、27%和35%。此外,BGM0504注射液10mg组和15mg组体重较基线降低≥25%的受试者比例分别为13%和20%,降低≥30%的受试者比例分别为3%和7%。
(2)腰围
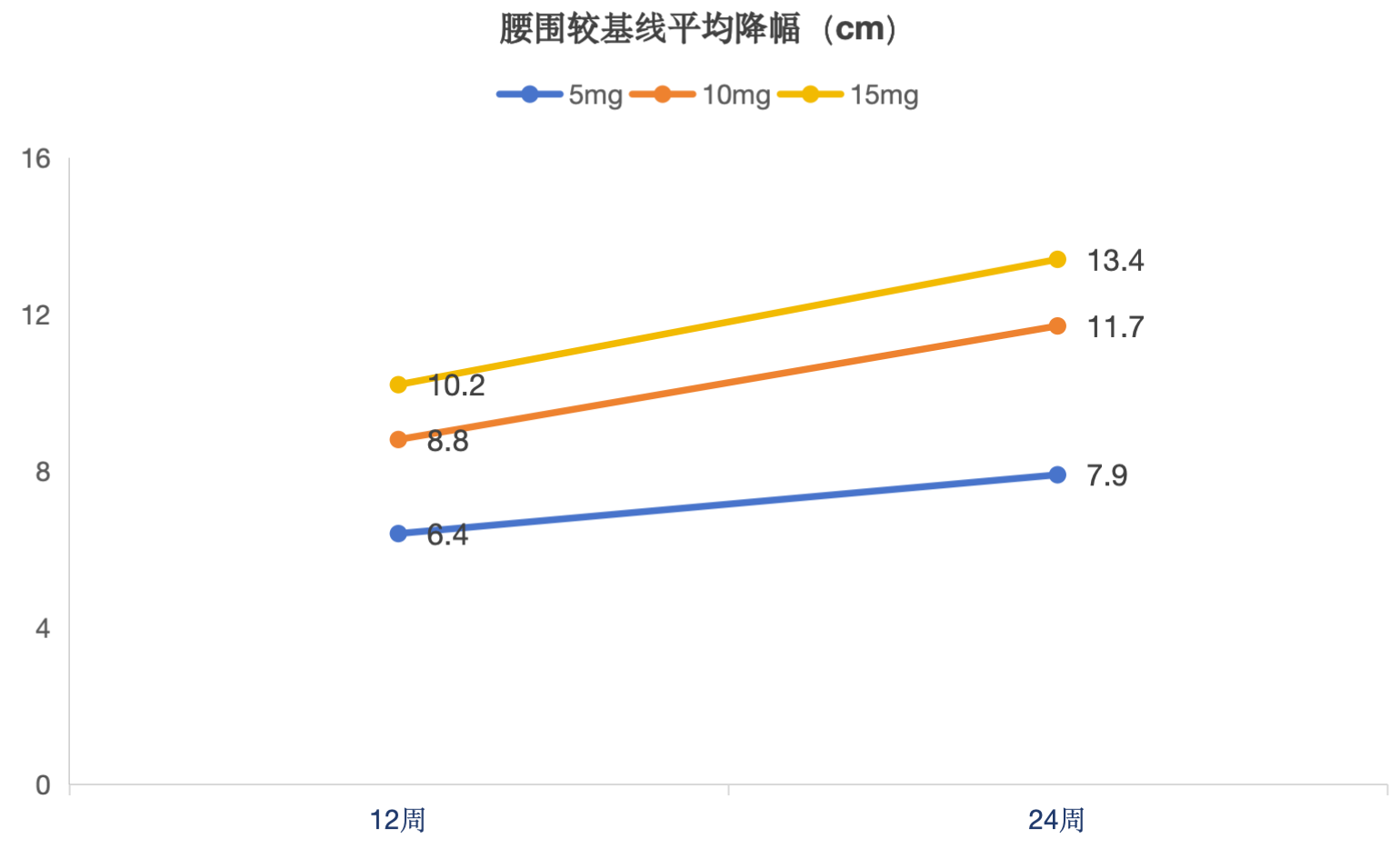
目标剂量给药第12周时,BGM0504注射液5mg组、10mg组和15mg组腰围较基线平均降幅(扣除安慰剂)分别为6.4cm、8.8cm和10.2cm。
目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组腰围较基线平均降幅(扣除安慰剂)分别为7.9cm、11.7cm和13.4cm;此外,目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg与安慰剂组腰围相对基线的变化的95%置信区间分别为:[-9.76,-5.36]、[-13.58,-8.38]和[-14.47,-8.67],p值均小于0.0001且各组95%置信区间上限均小于0,各剂量组均优于安慰剂组。
2、 次要终点提示BGM0504注射液能显著降低多项心血管代谢风险指标
(1)血压
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组SBP较基线平均降幅(扣除安慰剂)分别为11.7mmHg、14.7mmHg和12.5mmHg。
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组DBP较基线平均降幅(扣除安慰剂)分别为5.5mmHg、7.2mmHg和9.0mmHg。
(2)血尿酸、甘油三酯、总胆固醇、低密度脂蛋白胆固醇
目标剂量给药第24周时,BGM0504注射液5mg~15mg组血尿酸较基线平均降幅及降幅百分比(扣除安慰剂)为22~61μmol/L(6%~14%)。
目标剂量给药第24周时,BGM0504注射液5mg~15mg组甘油三酯较基线平均降幅百分比(扣除安慰剂)为23%~39%。
目标剂量给药第24周时,BGM0504注射液5mg~15mg组总胆固醇较基线平均降幅百分比(扣除安慰剂)为6%~12%。
目标剂量给药第24周时,BGM0504注射液5mg~15mg组低密度脂蛋白胆固醇较基线平均降幅百分比(扣除安慰剂)为9%~10%。
3、 次要终点提示BGM0504注射液表现出增加胰岛素敏感性趋势和改善体重对生活品质的影响
(1)空腹血糖
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组空腹血糖较基线平均降幅百分比(扣除安慰剂)分别为7%、13%和16%。
(2)空腹胰岛素
·目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组空腹胰岛素较基线平均降幅及降幅百分比(扣除安慰剂)分别为23.5pmol/L(20%)、58.8pmol/L(32%)和91.7pmol/L(56%)。
(3)体重对生活品质的影响量表
目标剂量给药第24周时,BGM0504注射液5mg组、10mg组和15mg组体重对生活品质的影响量表较基线评分改善提高(扣除安慰剂)为2~12分。
4、安全性及耐受性良好、无新增安全性信号
BGM0504 注射液每周给药1次、 5mg~15mg剂量下连续给药26~30周整体安全性和耐受性良好,与其它肠促胰岛素类药物基本一致,所发生的不良事件绝大多数为1~2 级,且大多未经干预即可恢复,所发生的不良反应多见于胃肠道系统方面(GI),严重程度主要为1级,发生时间集中在剂量滴定阶段及目标剂量给药前4周,继续给药后可逐渐耐受。整个试验过程中未发生任何低血糖事件和其他非预期不良反应以及未发生导致剂量下调和导致退出试验的不良反应。
BGM0504注射液在超重/肥胖患者中的2期临床研究顾问北京大学人民医院纪立农教授表示:“我国成人超重及肥胖合计患病率已超过50%,预计到 2030年,中国成人超重及肥胖合计患病率将达到 65.3%。肥胖已成为中国的重大公共卫生问题。在生活方式干预的基础上,临床上亟待更优减重效果、长期应用安全性高、患者使用依从性好的药物,在体重控制的同时兼顾血脂、血糖、血压等多指标改善以及最终心血管和肾脏获益。BGM0504注射液作为新一代GLP-1/GIP双受体激动剂,在已完成的中国超重/肥胖患者的2期临床试验中初步表现出耐受性、安全性良好,各剂量组受试者在体重、腰围等核心减重指标均明显优于安慰剂组、可显著降低患者体重和改善腰围。在次要疗评指标如心血管代谢风险指标(血压、血尿酸、甘油三酯/总胆固醇/低密度脂蛋白胆固醇等)、增加胰岛素敏感性的相关指标(空腹血糖/空腹胰岛素)、患者结局报告指标(体重对生活品质的影响量表)等较基线均有效改善,且优于安慰剂组。后续也将在中国成人超重/肥胖患者中开展BGM0504注射液和安慰剂对照的3期临床研究。我期待不久的将来BGM0504注射液可以为中国超重/肥胖患者的疾病和健康管理提供更多的药物治疗选择!”
BGM0504注射液在超重/肥胖患者中的2期临床研究由湘雅三医院阳国平教授和金萍教授共同担任主要研究者表示:“多靶点GLP-1RA类药物是目前内分泌领域新药研发的热点,一直受到临床治疗领域及药物研发领域专家的广泛关注。BGM0504注射液为新一代GLP-1/GIP双受体激动剂,目前处于国内周制剂药物研发的第一梯队。II期研究初步结果显示,BGM0504注射液每周给药一次能够有效降低超重/肥胖患者的体重、腰围等核心指标,以及改善血压、血尿酸、血脂等心血管代谢风险指标、同时呈现出增加胰岛素敏感性指标的初步效果等,可为超重/肥胖患者带来直接或潜在的多重获益。我们期待BGM0504注射液能够在后续III期关键临床研究中进一步验证II期临床的疗效和安全性,为超重/肥胖患者提供更多的治疗选择。”
声明:
1)BGM0504注射液为研究中的药品,尚未在中国获批;
2)博瑞医药不推荐任何未获批的药品/适应症使用;
3)该前瞻性陈述基于我们在陈述之日的已完成BGM0504注射液2期减重研究的初步预期和假设进行的,本品最终的减重疗效还需要后续大样本量上中国非糖尿病肥胖或超重受试者3期验证性临床研究来进一步确认。我们不承担更新或修改任何前瞻性陈述的义务,无论是由于新信息、未来事件或其他原因。