• YL201在小细胞肺癌、鼻咽癌、肺淋巴上皮样癌及非小细胞肺癌等难治性肿瘤中展现出疗效,ORR与DCR均超过现有标准治疗,且安全性可控;
• 目前YL201已在小细胞肺癌、鼻咽癌适应症进入III期临床研究;
• 中国学者主导、全球协作的全球同步临床开发,为国产创新药出海树立了标杆。
近日,宜联生物医药有限公司(以下简称“宜联生物”)在2025年欧洲肺癌大会(ELCC)年会上公布了其靶向B7H3的抗体偶联药物(ADC)YL201在肺癌患者中的颅内疗效数据,这一数据进一步巩固了YL201在治疗晚期实体瘤方面的潜力。
同时,YL201治疗晚期实体瘤的I期临床研究结果也已在国际顶级期刊《自然·医学》(Nature Medicine)上发表,该研究由中山大学肿瘤防治中心张力教授团队牵头,是一项全球多中心、开放标签的I期/Ib期临床试验,覆盖全球54家中心,纳入312例患者,为全球难治性肿瘤患者提供了新的治疗选择。

论文链接:https://www.nature.com/articles/s41591-025-03600-2
颅内疗效显著:ELCC年会公布最新数据
在ELCC年会上,宜联生物公布的YL201在肺癌患者中的颅内疗效数据来自于在中、美开展的I期临床剂量递增和剂量扩展研究(NCT05434234 & NCT06057922)。截至2024年11月15日,该项研究共入组329例晚期实体瘤患者,其中29例肺癌患者存在基线脑转移,包括21例小细胞肺癌患者和8例野生型非小细胞肺癌患者。这些患者既往均接受过标准治疗,中位治疗线数(范围)为1(1-5)。
在有效性方面,29例存在基线脑转移病灶(靶病灶或非靶病灶)的肺癌患者中,确认的颅内客观缓解率(ic-ORR)为17.2%(95% CI: 5.8–35.8),颅内疾病控制率(ic-DCR)为93.1%(95% CI: 77.2–99.2)。对于13例存在基线脑部靶病灶的患者,确认的ic-ORR为30.8%(95% CI: 9.1–61.4),ic-DCR为100.0%(95% CI: 75.3–100)。其中,小细胞肺癌和野生型非小细胞肺癌亚组人群的ic-ORR分别为30.0%(95% CI: 6.7–65.3)和33.3%(95% CI: 0.8–90.6)。
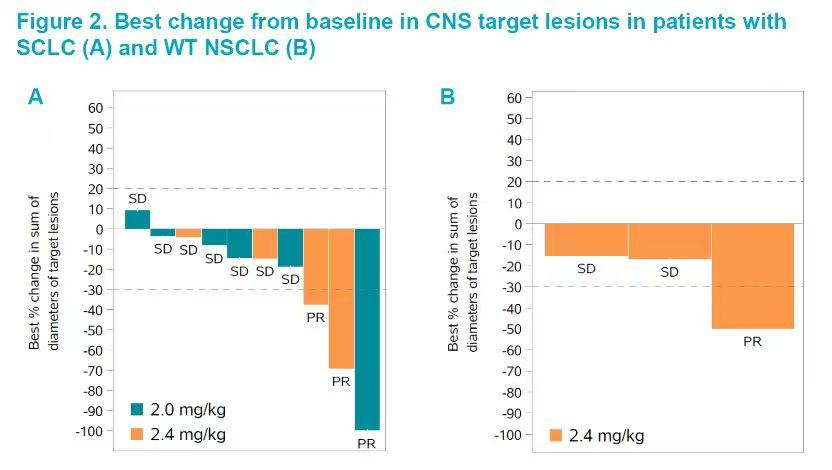
对于既往6个月内未接受过脑部放疗的患者,YL201同样显示出良好的颅内疗效。确认的ic-ORR为57.1%(95% CI: 18.4–90.1),ic-DCR为100.0%(95% CI: 59.0–100)。在颅内无进展生存期(ic-PFS)方面,29例存在基线脑转移(靶病灶或非靶病灶)的肺癌患者的中位ic-PFS达到了6.3个月(95% CI: 3.9–8.9)。其中,小细胞肺癌亚组人群的中位ic-PFS为6.2个月(95% CI: 3.8–8.9),野生型非小细胞肺癌亚组人群的中位ic-PFS为7.4个月(95% CI: 1.2–NR)。
在显示出良好颅内疗效的同时,YL201的中枢神经系统毒性却相当低。在接受治疗的全部329例患者中,只有0.9%的患者报告了≥3级的神经系统疾病。这一结果表明,YL201在治疗存在脑转移的肺癌患者中具有显著的疗效和良好的安全性。
宜联生物医药首席医学官秦续科博士说:“宜联生物在ELCC大会上公布的数据是对之前数据强有力的补充,进一步证明了YL201在肺癌患者中,尤其是存在脑转移的肺癌患者中的治疗效果。考虑到脑转移会显著影响肺癌患者的预后,我们目前的结果是一个非常令人鼓舞的信号。目前YL201已在小细胞肺癌适应症中开展了III期临床研究,我们认为这次ELCC大会上公布的数据,会进一步增强我们对YL201治疗这些患者的信心”。
全球多中心突破:YL201覆盖多瘤种,疗效全面领跑
而发表在《自然·医学》YL201的临床试验结果,中山大学肿瘤防治中心张力教授、赵洪云教授,宜联生物薛彤彤博士为该文章的通讯作者,中山大学肿瘤防治中心马宇翔副主任医师、杨云鹏主任医师、黄岩主任医师、方文峰教授、薛锦慧医师、山东省肿瘤医院孟祥姣教授,浙江省肿瘤医院范云教授,MD Anderson Cancer Center的Siqing Fu教授为该文章的共同第一作者。
这是一项全球多中心、开放标签的I期/Ib期研究,分为剂量递增(I期)和剂量扩展(Ib期)两部分,纳入的患者类型广泛,包括广泛期小细胞肺癌(ES-SCLC)、鼻咽癌(NPC)、非小细胞肺癌(NSCLC)等。研究覆盖了亚洲、欧美等多个地域的人群,体现了国际间的合作与参与。
在287例可评估疗效的患者中,尽管有158例(55.1%)的患者既往已经接受过2线及以上的抗肿瘤治疗后进展,但YL201仍表现出显著的抗肿瘤活性。在117例(40.8%)患者中观察到了客观缓解,疾病控制率(DCR)高达83.6%。这一结果在小细胞肺癌、鼻咽癌和肺淋巴上皮瘤样癌患者中尤其值得关注。
小细胞肺癌:破解耐药困局,提供“中国方案”
在小细胞肺癌领域,YL201的表现尤为亮眼。在72例可评估的广泛期小细胞肺癌(ES-SCLC)患者中,客观缓解率(ORR)达到63.9%,疾病控制率(DCR)达91.7%,中位无进展生存期(mPFS)为6.3个月。这一结果显著优于拓扑替康(ORR约为24%)和芦比替定(ORR约为35%)等现有的二线治疗方案。
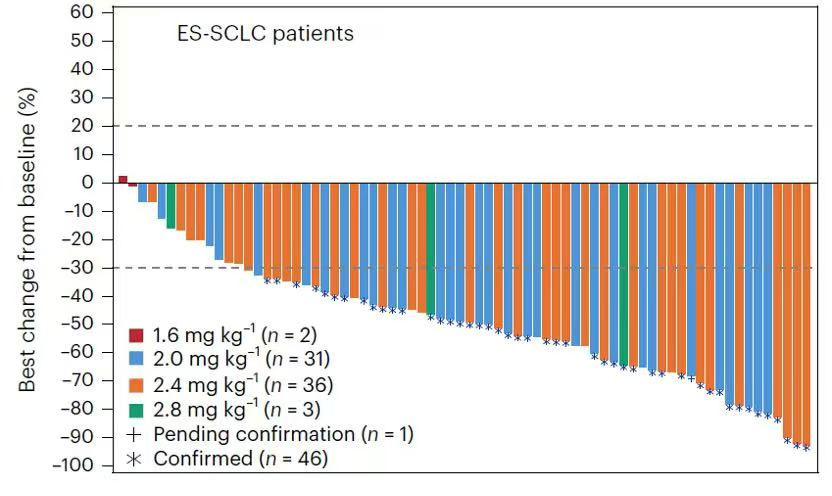
基于这一临床表现,为了造福更多患者,宜联生物已开展了一项“评估注射用YL201对比注射用盐酸托泊替康在复发性小细胞肺癌患者中的有效性和安全性的多中心、随机对照、开放标签的III期研究”。该研究将进一步验证YL201在小细胞肺癌后线治疗中的疗效和安全性,有望为这一难治性肿瘤提供新的治疗策略。
鼻咽癌:全球首次报道B7H3靶向药物疗效
在鼻咽癌方面,YL201在70例可评估的鼻咽癌(NPC)患者中,客观缓解率为48.6%,疾病控制率为92.9%,中位无进展生存期为7.8个月,中位缓解持续时间为8.4个月。这一疗效显著优于现有的标准治疗方案,如多西他赛(客观缓解率约为24%)和PD-1抗体(客观缓解率20-30%不等)。
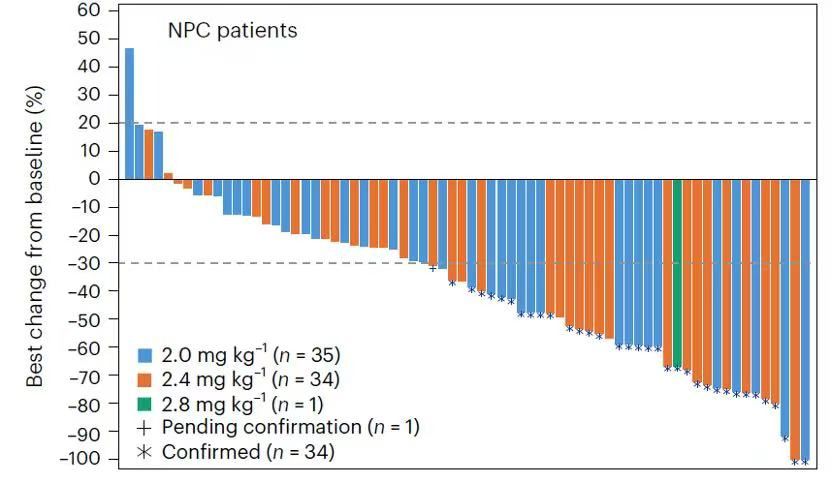
基于这一结果,宜联生物已开展了一项“YL201对比研究者选择的化疗治疗既往经PD-(L)1抑制剂和至少二线化疗治疗失败的复发或转移性鼻咽癌患者的随机、对照、多中心III期临床研究”。该研究将进一步探索YL201在鼻咽癌患者中的疗效和安全性,有望为这一难治性肿瘤提供新的治疗选择。
肺淋巴上皮瘤样癌:全球首个靶向ADC药物报道
肺淋巴上皮瘤样癌(LELC)是一种与EB病毒(EBV)感染密切相关的NSCLC亚型,目前缺乏有效的靶向治疗药物。在24例可评估的淋巴上皮瘤样癌(LELC)患者中,YL201的客观缓解率为54.2%,填补了这一领域后线治疗的空白,这也是全球首次报道靶向B7H3的ADC在该瘤种中的疗效数据。
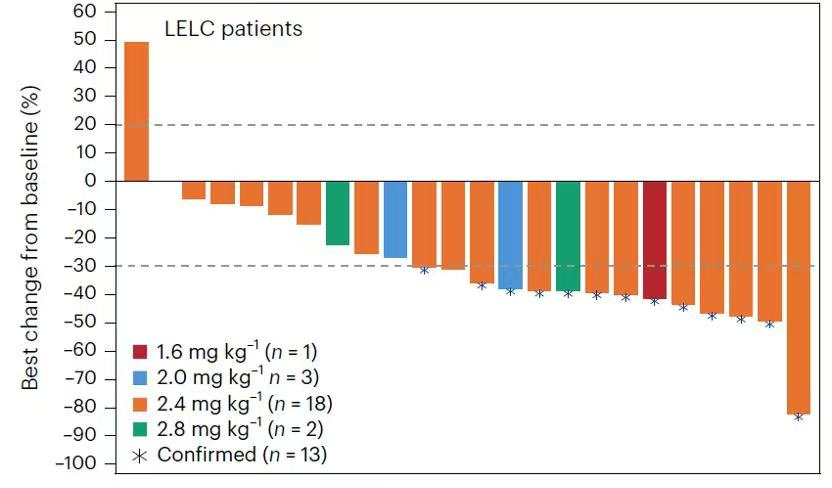
安全可控:充分支持治疗,安全与耐受表现良好
在安全性方面,该临床研究显示3级或以上的相关不良事件(TRAE)发生率为54.5%,以中性粒细胞减少(31.7%)最为常见。但值得注意的是,YL201的治疗中断率(5.4%)和剂量减少率(17.0%)相对较低。间质性肺病(ILD)的发生率仅为1.3%,低于同类B7H3的ADC药物DS-7300治疗后ILD的发生率(6.9%)。
研究结果显示,在充分的粒细胞集落刺激因子等对症支持治疗下,患者的血液学毒性可以得到迅速控制和恢复。在后续治疗中有针对性地预防治疗后,治疗相关不良事件的发生率迅速下降。这表明YL201的安全性整体可控,治疗相关的毒性在充分的支持治疗中得到有效缓解。
国产原研+全球协作:引领国际新药研发
本研究自2022年启动并开始招募受试者以来,就引发了全球关注。2024年9月在欧洲肿瘤大会ESMO上,本研究更新的部分结果同样获得优先口头报告展示的邀请。在鼻咽癌、小细胞肺癌上有效的抗肿瘤活性数据得到全球关注,引发国际同行高度评价。
作为首个由中国学者主导、全球研发的B7H3靶向ADC,YL201的全球多中心模式不仅加速了临床试验进程,更打通了药物国际化的通路,也为国产创新药出海树立了标杆。
YL201作为首个在EBV相关肿瘤(如NPC和LELC)中显示出显著疗效的B7H3靶向ADC,为这些难治性肿瘤患者提供了新的治疗选择。本研究结果为YL201的进一步开发提供了强有力的支持。
目前,针对小细胞肺癌和鼻咽癌的III期临床试验已经启动(NCT06612151和NCT06629597),将评估YL201在更大规模患者群体中的长期疗效和安全性。期待YL201的后续结果能够进一步验证其疗效和安全性,未来造福更多的肿瘤患者。
YL201研究者简介:

通讯作者 张力教授
-
中山大学肿瘤防治中心内科主任导师、博士生导师、二级教授、肺癌首席专家
-
中国抗癌协会(CACA)癌症康复与姑息治疗专业委员会主任委员
-
中国抗癌协会(CACA)肿瘤药物临床研究专业委员会候任主任委员
-
中国临床肿瘤学会(CSCO)免疫治疗专家委员会主任委员
-
中国临床肿瘤学会(CSCO)非小细胞肺癌专家委员会副主任委员
-
中国临床肿瘤学会(CSCO)肿瘤支持与康复治疗专家委员会副主任委员
-
广东省医学会临床研究学分会主任委员
-
广东省临床医学会精准医学分会主任委员

通讯作者 赵洪云教授
-
中山大学肿瘤防治中心I期病房主任,临床研究部副主任,教授,主任医师,博士生导师
-
广东省临床医学学会肺癌精准治疗及临床研究专委会主任委员
-
中国抗癌协会肿瘤药物临床研究专业委员会青年委员会副主任委员
-
广东省抗癌协会化疗专业委员会青年委员会副主任委员
-
《健康中国2030》肿瘤健康之“肺癌规范化诊疗”项目组专家顾问

第一作者 马宇翔副主任医师
-
中山大学肿瘤防治中心肿瘤学博士,副主任医师,硕士生导师
-
中山大学肿瘤防治中心临床试验中心I期病房副主任医师
-
广东省临床医学会肺癌精准治疗与临床研究专业委员会秘书
-
广东省抗癌协会化疗专业青年委员会委员

宜联生物向参研中心和研究者颁发荣誉证书留影(部分)

共同第一作者 浙江省肿瘤医院 范云教授

共同作者 浙江大学医学院附属第一医院 刘健教授

共同作者 江西省肿瘤医院 刘智华教授

共同作者 桂林医学院第二附属医院 李碧慧教授

共同作者 郑州大学第一附属医院 李明君教授

共同作者 河南省肿瘤医院 杨树军教授

共同作者 江西省肿瘤医院 李金高教授

共同作者 四川省肿瘤医院 张鹏教授
关于宜联生物医药
宜联生物医药成立于2020年,是一家专注于开发创新型偶联药物的临床阶段生物科技公司。目前公司己开发出多种不同机制的具有自主知识产权的新型毒素连接子技术, 其中基于肿瘤微环境可裂解的喜树碱类毒素连接子(TMALIN®)技术已经有十项ADC产品获得中美临床批准并启动临床研究。宜联生物医药致力于以未满足的临床需求为目标,为全球肿瘤患者带来更好的治疗方案。宜联生物医药位于苏州和波士顿,在上海和新加坡设有分支机构。
关于YL201
YL201是一款宜联生物医药开发的靶向B7-H3的抗体偶联药物。B7-H3在多种恶性肿瘤的分化和起始细胞上过表达,但在正常组织中的表达有限,具备针对多癌种开发ADC药物的潜力。YL201是宜联生物医药利用新一代具有自主知识产权的肿瘤微环境可激活的新型毒素连接子平台技术(TMALIN®)与高度特异性的B7-H3抗体偶联所开发,其治疗晚期实体瘤的I期临床研究结果在国际顶级期刊《自然·医学》发表。目前,YL201正在多个适应症中广泛开展临床探索,其中在小细胞肺癌、鼻咽癌适应症中已进入关键临床阶段。