由复旦大学附属肿瘤医院邵志敏教授团队牵头的伊尼妥单抗联合帕妥珠单抗和白蛋白紫杉醇作为HER2阳性乳腺癌新辅助治疗的疗效和安全性的多中心单臂II期临床试验结果在国际肿瘤领域权威期刊《Cancer Letters》 (IF:9.1, JCR分区Q1/中科院分区Q1)正式发表。结果显示:伊尼妥单抗+帕妥珠单抗+白蛋白紫杉醇4周期新辅助治疗HER2阳性乳腺癌,病理完全缓解(tpCR)率达56.5%。

研究关键亮点:
-
全人群tpCR率高达56.5%(95% CI: 43.3%-69.0%),为HER2+早期乳腺癌患者带来新希望
-
ER阴性患者tpCR率高达90.9%
-
客观缓解率(ORR)达90.3%
-
安全性可控,≥3级不良事件以血液学毒性为主(中性粒细胞减少32.3%),无治疗相关死亡
-
全程无抗药抗体(ADA)产生
研究提示:该方案为HER2阳性乳腺癌新辅助治疗提供新选择,尤其对ER阴性患者潜力显著!
研究背景
HER2阳性乳腺癌约占所有乳腺癌的15%-20%,其生物学特征表现为侵袭性强、复发风险高,传统化疗时代患者预后较差。随着抗HER2靶向治疗(如曲妥珠单抗、帕妥珠单抗)的广泛应用,患者的生存率显著提升。然而,新辅助治疗(即在手术前进行的全身治疗)的病理完全缓解(pCR)率仍有提升空间。pCR是预测患者长期生存的重要指标,更高的pCR率通常意味着更低的复发风险。因此,探索更高效、安全的新辅助治疗方案成为临床研究的重点。
伊尼妥单抗(Inetetamab)是我国自主研发的新型抗HER2单克隆抗体,其独特之处在于通过Fc段的工程化改造,增强了抗体依赖性细胞毒性(ADCC)效应。临床前研究显示,这种改造可更高效地激活免疫细胞(如自然杀伤细胞),从而提升对肿瘤细胞的杀伤能力。基于此,研究者提出假设:将伊尼妥单抗与帕妥珠单抗及白蛋白紫杉醇联合使用,可能通过多重机制协同增效,为HER2阳性乳腺癌患者带来更高的pCR率。
研究方法与设计
这项前瞻性、多中心、单臂II期临床试验共纳入62例符合标准的HER2阳性早期或局部晚期乳腺癌患者。研究方案设计如下:
治疗方案:患者接受4个周期(每3周为一周期)的联合治疗。
伊尼妥单抗:首剂8 mg/kg,后续6 mg/kg,静脉滴注,每3周一次。
帕妥珠单抗:首剂840 mg,后续420 mg,静脉滴注,每3周一次。
白蛋白紫杉醇:125 mg/m²,静脉滴注,每周一次。
主要终点:总病理完全缓解率(tpCR),定义为术后乳腺原发灶和区域淋巴结均无浸润性癌残留(即病理分期为ypT0/is,ypN0)。
次要终点:客观缓解率(ORR,通过影像学评估肿瘤缩小程度)、安全性(不良事件分级)和免疫原性(抗药物抗体产生情况)。
研究团队通过严格的入组标准筛选患者,所有病例均经病理学确诊为HER2阳性(IHC 3+或FISH阳性),且排除存在远处转移或既往接受过抗HER2治疗者。治疗后,患者接受手术切除,并由独立病理专家进行盲法评估以确认pCR状态。
关键研究结果
1.疗效数据:显著提升的pCR率
总体人群:tpCR率为56.5%(35/62例;95%置信区间:43.3%-69.0%),这一数据优于历史对照中部分曲妥珠单抗联合化疗方案的表现(约40%-50%)。
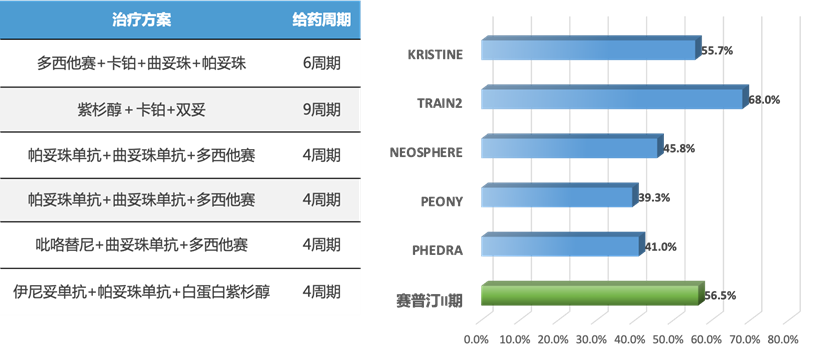
图1 本研究与历史研究的tpCR数据对比
ER阴性亚组:在ER阴性(雌激素受体阴性)患者中,tpCR率高达90.9%(20/22例),提示该方案对激素受体阴性人群可能具有更强的抗肿瘤活性。既往研究显示,ER阴性/HER2阳性乳腺癌对双靶向治疗(如曲妥珠+帕妥珠单抗)的应答优于ER阳性患者,本研究的发现进一步支持这一规律。
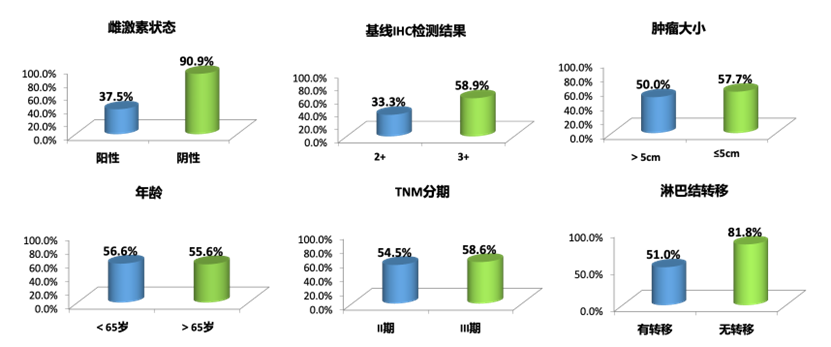
图2 亚组疗效分析
客观缓解率:90.3%的患者达到完全缓解或部分缓解,表明治疗在缩小肿瘤体积方面效果显著。
2.安全性:可控的不良事件
血液学毒性:≥3级不良事件以中性粒细胞减少(32.3%)、白细胞减少(19.4%)为主,与白蛋白紫杉醇的已知毒性谱一致。
非血液学毒性:感染性肺炎(3.2%)和腹泻(3.2%)发生率较低,且无治疗相关死亡事件。
3.免疫原性:所有患者在整个治疗期间均未检测到抗药物抗体(ADA),表明伊尼妥单抗的免疫原性风险极低。
结论
伊尼妥单抗联合帕妥珠单抗及白蛋白紫杉醇的新辅助治疗方案,在HER2阳性乳腺癌患者中展现出令人鼓舞的疗效和可控的安全性,特别是为ER阴性患者提供了潜在的高效治疗选择。这一研究不仅为临床实践提供了新策略,也为国产创新药物的开发和应用奠定了重要基础。未来,随着更多证据的积累,该方案有望成为HER2阳性乳腺癌新辅助治疗的标准选择之一。
参考文献:
[1] Zuo WJ, Ma LX, Wang ZH,et al. Efficacy and safety of inetetamab plus pertuzumab and nab-paclitaxel as neoadjuvant therapy for HER2+ breast cancer: A single-arm multicenter phase II clinical trial. Cancer Lett. 2025 May 10:217785. doi: 10.1016/j.canlet.2025.217785. Epub ahead of print. PMID: 40354993.
关于三生国健
三生国健是中国第一批专注于抗体药物的创新型生物医药高新技术企业之一。公司拥有研、产、销一体化成熟平台,专注于单抗、双抗、多抗及多功能重组蛋白等新技术研究,拥有丰富的大规模抗体产业化和质量控制经验。公司是“免疫与炎症全国重点实验室”依托单位、拥有抗体药物国家工程研究中心、国家企业技术中心、上海市抗体技术创新中心、上海抗体工程技术研究中心等国家级和上海市级高新技术平台,承担过国家重大新药创制、“863”计划、国家发改委及上海市重大项目及各部委课题百余项,多次获得上海市级和浦东新区科学技术奖。目前,公司拥有18个处于不同开发阶段的自身免疫在研创新药物项目,均为治疗用生物制品1类药品,部分在研药物为中美双报。公司是国家知识产权示范企业、上海市知识产权示范企业,累计申请发明专利近200件,获得发明专利授权近百项,产品覆盖国内32个省、自治区、直辖市,并销往海外十余个国家。