2025年5月27日──来凯医药(2105.HK)今日宣布,公司将在美国糖尿病协会(American Diabetes Association, ADA)第85届科学年会上,以壁报形式展示多项增肌减脂领域的研发成果——
-
靶向ActRII的三款单克隆抗体LAE102、LAE103和LAE123的临床前数据
-
以及其中一款针对ActRIIA的单抗LAE102的首次人体研究数据
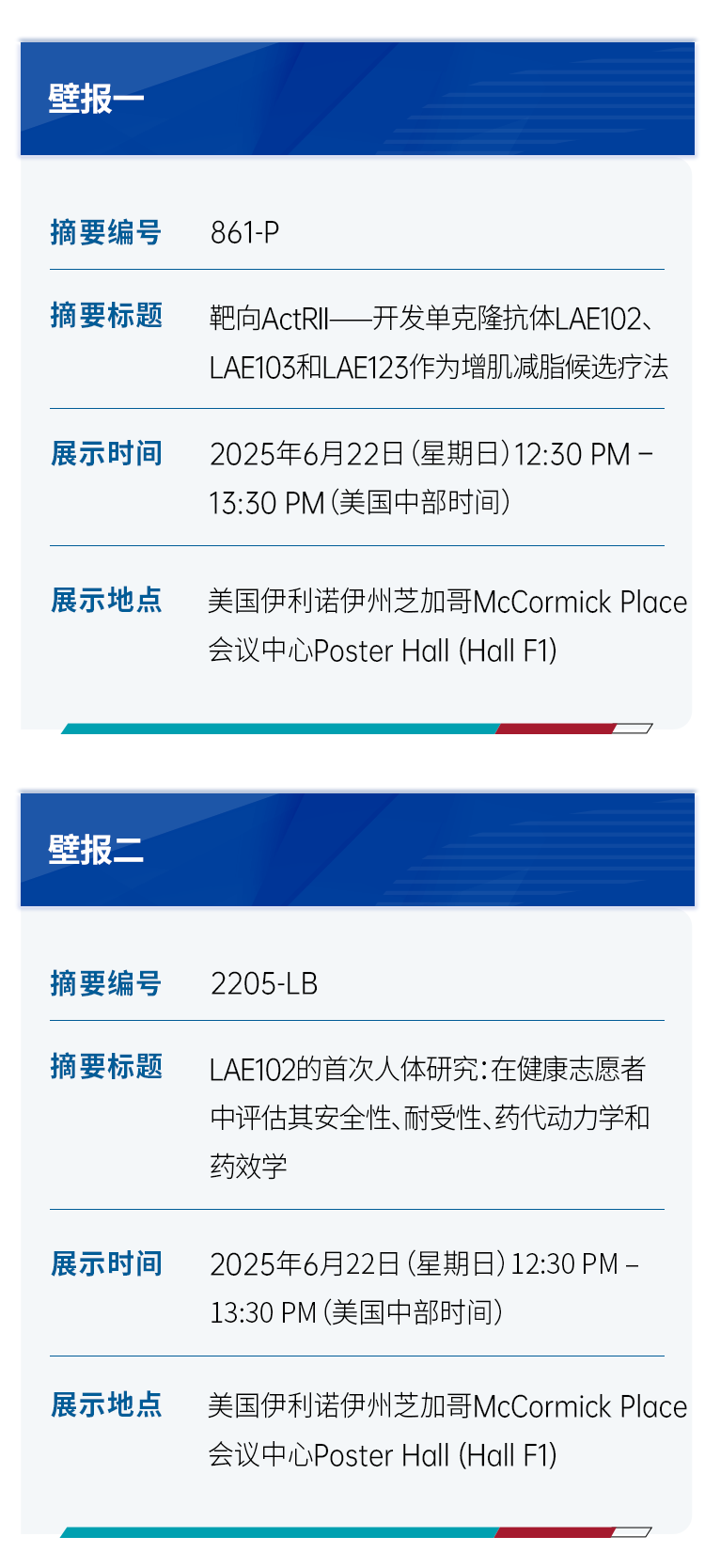
LAE102是来凯医药自主研发的一种ActRIIA单克隆抗体,在临床前模型中已显示出增加肌肉并减少脂肪的效果。在已完成的中国I期临床试验单剂量递增研究(SAD研究)中,单次剂量的LAE102给药导致激活素A水平显著且持续增加,表明了强有力的靶点抑制。这项研究的详细数据将于本次ADA会议上披露。
此外,来凯与礼来合作在美国快速推进LAE102肥胖症治疗的临床研究。
来凯围绕ActRII通路的自主研发深入布局,LAE103(ActRIIB选择性抗体)和LAE123(针对ActRIIA/IIB双靶点抑制剂)均已进入IND支持性研究阶段,将探索临床用于肌肉及危重疾病领域的创新疗法。
ADA科学年会是全球糖尿病领域的顶级学术盛会,将于今年6月20日至23日在美国芝加哥召开。
关于来凯医药(股份代码:2105.HK)
来凯医药成立于2016年,是一家以科学为驱动、处于临床阶段的生物医药科技公司,致力于为全球代谢疾病、癌症及肝纤维化患者带来新型疗法。
截至2024年12月31日,来凯医药围绕LAE102、LAE002(afuresertib)、LAE001及LAE005启动了七项临床试验,以解决肥胖症及癌症领域未被满足的医疗需求。
LAE102是来凯自主研发针对ActRIIA的单克隆抗体。阻断Activin-ActRII通路可促进肌肉再生和减少脂肪,这使LAE102有望成为一种实现高质量体重控制的候选药物。LAE102已获得中国和美国针对肥胖适应症的新药临床试验(IND)批准,I期临床研究正在全速推进。2024年11月,来凯与礼来签订一项临床合作协议,旨在支持和加速LAE102针对肥胖症治疗的全球临床开发。
在靶向ActRII受体这一特定领域,来凯团队积累了丰富的经验及深厚的专业知识,并正在开发更多的候选药物,以最大限度地发挥此靶点的价值。LAE103是ActRIIB选择性抗体,LAE123是针对ActRIIA/IIB的双靶点抑制剂,两者均为我们自主研发用于肌肉及其他疾病适应症的抗体。
在癌症领域,来凯已经建立全面的候选药物组合,包括LAE002(afuresertib)、LAE001及其他七种临床前候选药物。LAE002(afuresertib)是一种AKT强效抑制剂,抑制所有三种AKT亚型(AKT1、AKT2及AKT3),也是全球两种处于晚期临床开发阶段的针对乳腺癌及前列腺癌的AKT抑制剂之一。目前来凯医药针对HR+/HER2-乳腺癌III期关键研究(AFFIRM-205)顺利推进中。
2023年6月29日,来凯医药在香港联合交易所有限公司(“香港交易所”)主板上市,股份代码:2105.HK。