2025年6月27日,北京质肽生物医药科技有限公司自主研发的创新性GLP-1/FGF21双重激动剂-ZT003注射液,正式获得美国食品药品监督管理局(FDA)新药临床试验批准,其适应症为代谢功能障碍相关脂肪性肝炎(MASH)的治疗,ZT003即将在国外开展I期临床试验。这一重大进展,标志着质肽生物创新药国际化战略迈向新台阶。
质肽生物联合创始人、R&D高级副总裁张媛媛博士表示:“对于晚期的MASH患者,如已经发生纤维化、肝硬化的患者,目前尚无有效的治疗手段。我们自主研发的创新型GLP-1/FGF21双激动剂 - ZT003凭借其独特的分子设计在临床前试验中展现了其逆转肝纤维化的疗效,有望成为MASH治疗领域最具潜力的疗法。我们对即将开展的临床试验充满信心,期待进一步评估其临床疗效和安全性。”
质肽生物创始人、董事长兼首席执行官张旭家博士表示:“本次ZT003注射液临床试验获批,是该款产品研发进程中的又一重要里程碑,将进一步提升质肽生物在代谢治疗领域的核心竞争力,也是对质肽生物国际化创新能力和技术水平的高度认可。质肽生物将持续发挥在代谢病领域的独特优势,快速有力推进ZT003的临床开发,早日为全球MASH患者带来更有效的治疗方案。”
关于MASH
代谢功能障碍相关脂肪性肝炎(MASH),是代谢功能障碍相关脂肪性肝病(MASLD)的一种进展形式。MASH的特征是肝脏脂肪变性伴随炎症、肝细胞气球样变和脂肪堆积引起的细胞损伤,可能导致晚期纤维化、肝硬化和肝细胞癌(HCC)。在全球范围内,MASLD影响约25%的人口。MASH是肝硬化、HCC和肝病死亡的重要原因。大约10-30%的单纯脂肪变性患者会发展为脂肪性肝炎和晚期肝病,2型糖尿病(T2D)患者的危险性显著更高。肥胖,特别是腹部肥胖,和T2D与MASLD和MASH相关并发症(包括晚期纤维化和肝硬化)的进展密切相关。目前全球唯一获批用于治疗MASH的药物Resmetirom,改善肝脏脂肪性肝炎和纤维化的比例相对较低,且不适用于肝硬化人群。开发更好的治疗MASH的创新药还有着巨大的未被满足的临床需求。
关于ZT003注射液
ZT003是一种新型的单分子GLP-1/FGF21双激动融合蛋白。临床试验结果已显示GLP-1受体激动剂可以显著缓解MASH患者代谢功能障碍,促进体重减轻,显示出在肝脏脂肪、炎症和纤维化方面的改善;FGF21可通过不同机制降低MASH患者肝脏甘油三酯和胆固醇水平,增强肝脏交感神经活动,减少肝脏新生脂肪生成和纤维化,在临床试验中已显示出逆转MASH肝硬化患者纤维化的巨大潜力。ZT003独特的分子设计,实现了GLP-1和FGF21双靶点的协同与互补效应(如图),在临床前MASH动物模型中展现出显著的改善肝脏脂肪、炎症和纤维化水平的能力,有望成为MASH治疗领域最具潜力的疗法。
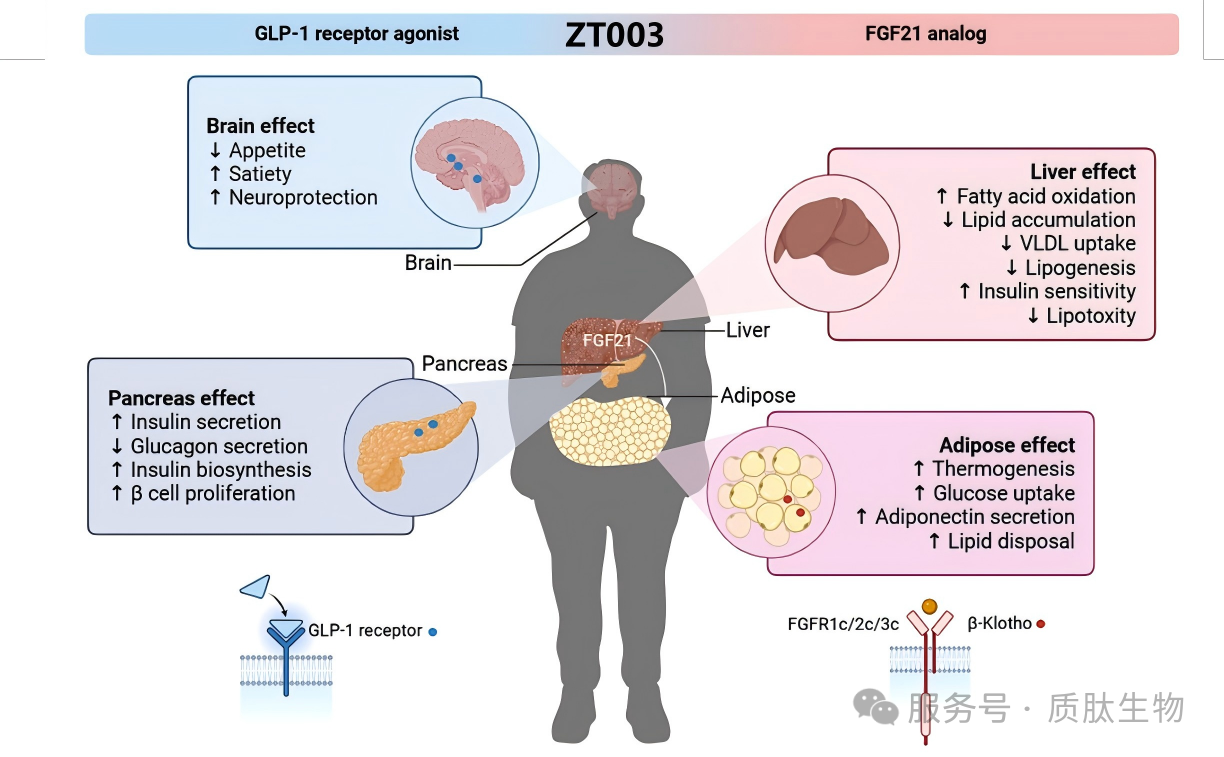
(GLP-1/FGF21双靶点协同互补治疗MASH机制示意图)