2025年9月9日,复宏汉霖(2696.HK)自主研发的重组抗EGFR单克隆抗体HLX07联合抗PD-1单抗H药 汉斯状®(斯鲁利单抗)用于一线治疗EGFR高表达晚期或转移性鳞状非小细胞肺癌(sqNSCLC)患者的 II 期剂量探索研究的更新数据在2025年世界肺癌大会(World Conference on Lung Cancer)上发布。

EGFR高表达庞大人群,治疗空白亟待破局
在全球非小细胞肺癌(NSCLC)患者中,EGFR高表达的比例约为40%–89%(取决于病理分型、种族等因素),意味着每年有数百万新发患者属于这一人群[1-3]。尤其是在sqNSCLC患者中,EGFR高表达患者占比达89%[1-2]。
然而,与携带EGFR驱动突变患者相比,EGFR高表达人群通常缺乏适用于EGFR靶向治疗的驱动突变,因此目前无法实现精准治疗。另一方面,尽管PD-(L)1抑制剂已被纳入晚期或转移性sqNSCLC一线治疗的主流方案,但针对EGFR高表达人群,迄今尚无经验证的一线治疗方案。这一庞大人群仍面临治疗匮乏、生存率低、预后差等多重困境,亟需创新方案填补这一临床空白。
双靶点聚焦,优势互补,激发协同潜力
HLX07是复宏汉霖自主开发的创新EGFR的单克隆抗体。相比西妥昔单抗该产品具备更低的免疫原性和更好的靶点亲和力。同时通过Fc端改造,HLX07大大延长了产品的半衰期,3周的给药频率使其更适合与肿瘤免疫产品的临床联用。临床前研究表明,HLX07具有更出色的生物活性,在不同肿瘤模型中均能显著抑制肿瘤细胞的生长,并与H药显示出很强的协同作用[4]。H药作为全球首个一线获批用于广泛期小细胞肺癌的抗PD-1单抗,迄今已惠及逾12万名患者,覆盖全球近半数人口。两者联用,不仅阻断EGFR生长信号,更同步激活免疫应答,极具联合协同治疗潜力。
临床信号积极,安全性可控
HLX10HLX07-sqNSCLC-201研究是一项随机、多中心的II期剂量探索研究,包括4个部分,评估了HLX07(不同剂量)、斯鲁利单抗和化疗的多种组合。第3部分评估了三药组合的初步有效性,EGFR高表达(H评分≥150)且无既往系统治疗的患者被1:1随机分至两组,分别接受静脉注射HLX07 800 mg或1000 mg,联合斯鲁利单抗和化疗。
根据此次更新数据,HLX07联合斯鲁利单抗及化疗在EGFR高表达sqNSCLC患者中展现出显著的抗肿瘤活性和持久疗效。在中位随访18.6个月时,两个剂量组均实现了约70%的客观缓解率(ORR)和超过90%的疾病控制率(DCR);高剂量组的中位无进展生存期(PFS)达到17.4个月,低剂量组的中位PFS在随访时尚未达到,两组的中位总生存期(mOS)和持续缓解时间(mDOR)均未达到,显示出疗效持久且有进一步改善的潜力。多数治疗期间不良事件(TEAE)如皮疹等均在可控范围内,安全性良好。
详细数据
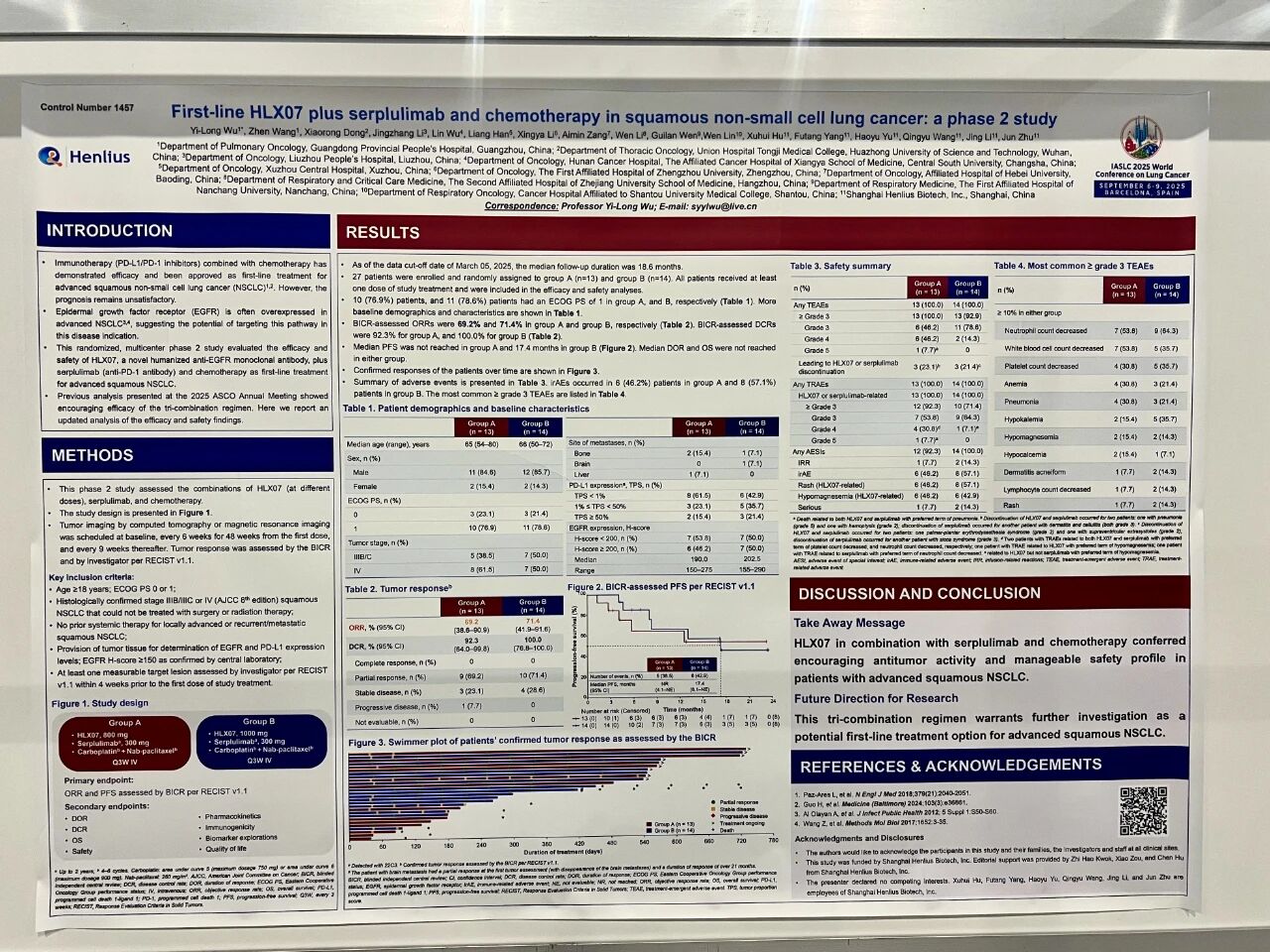
截至2025年3月5日,共有27例患者参与并随机分配至研究第3部分的A组(n=13)或B组(n=14)。两组患者分别每三周一次接受800 mg HLX07(A组)或1000 mg HLX07(B组)联合300 mg斯鲁利单抗和化疗。15例(55.6%)患者患有转移性sqNSCLC。中位随访时间为18.6个月。
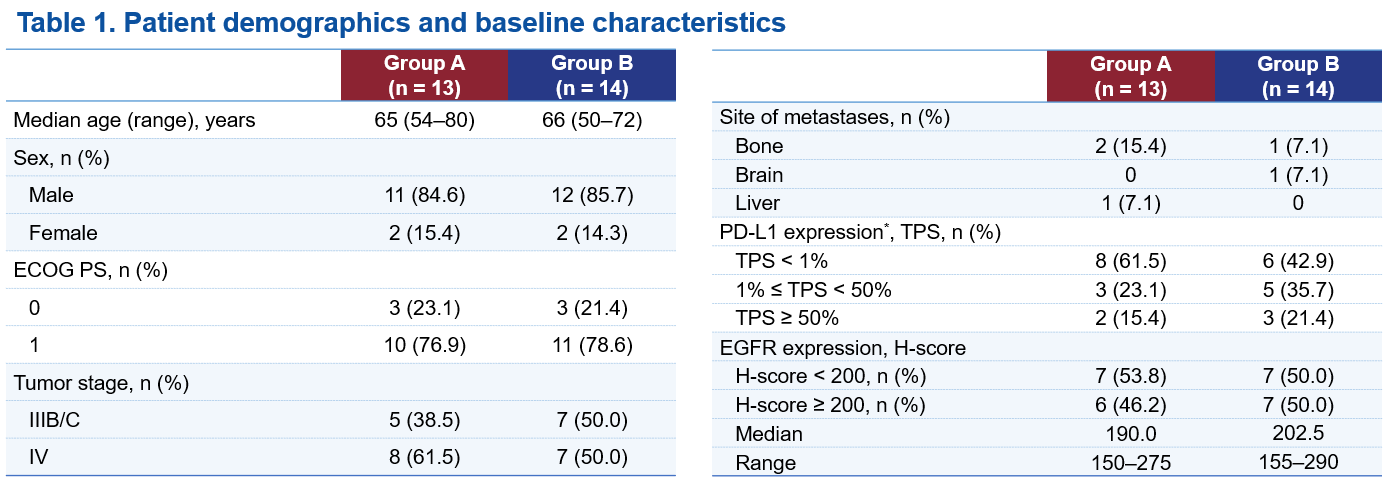
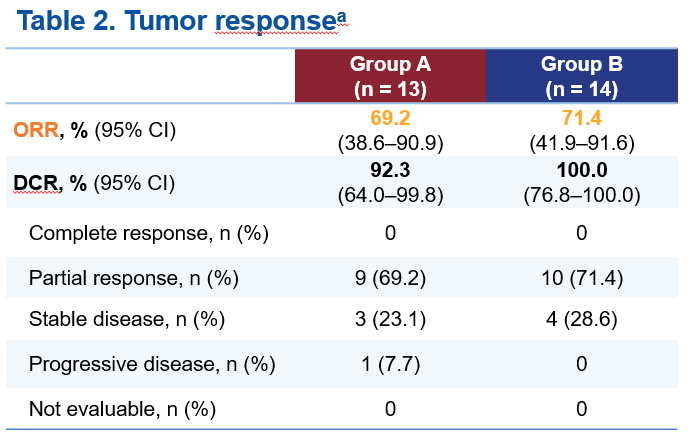
A组和B组中,独立影像评估委员会(IRRC)根据RECIST 1.1评估的确认ORR分别为69.2%(95% 置信区间[CI] 38.6–90.9)和71.4%(95% CI 41.9–91.6),疾病控制率分别为92.3%(95% CI 64.0–99.8)和100%(95% CI 76.8–100.0)。
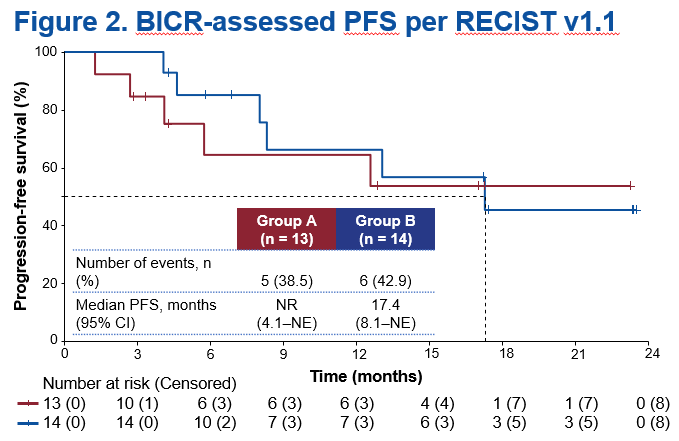
A组的中位PFS尚未达到,B组中位PFS为17.4个月(95% CI 8.1–不可评估)。
截至数据截止日期,两组的中位总生存期和持续缓解时间均未达到。
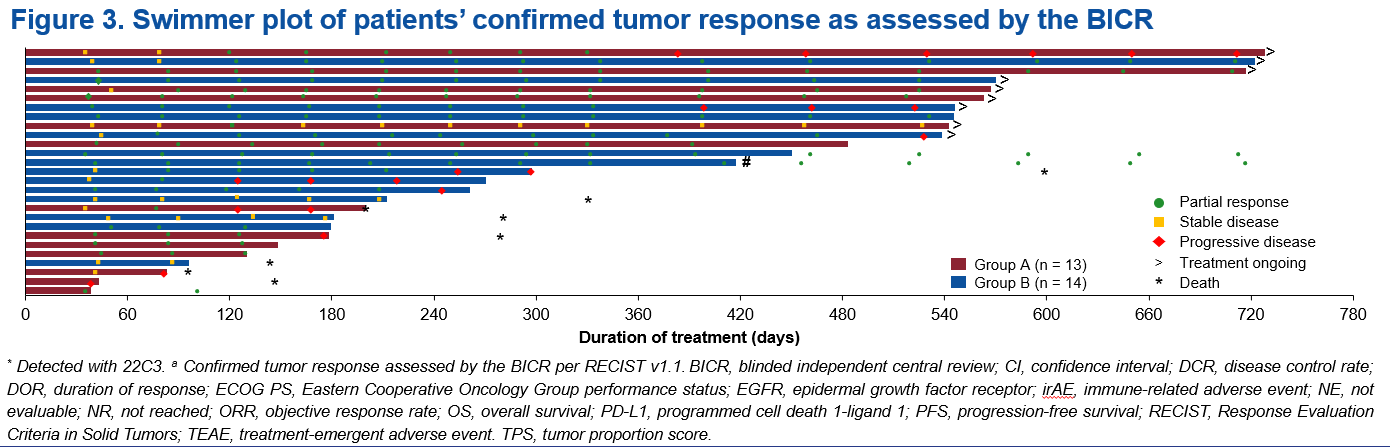
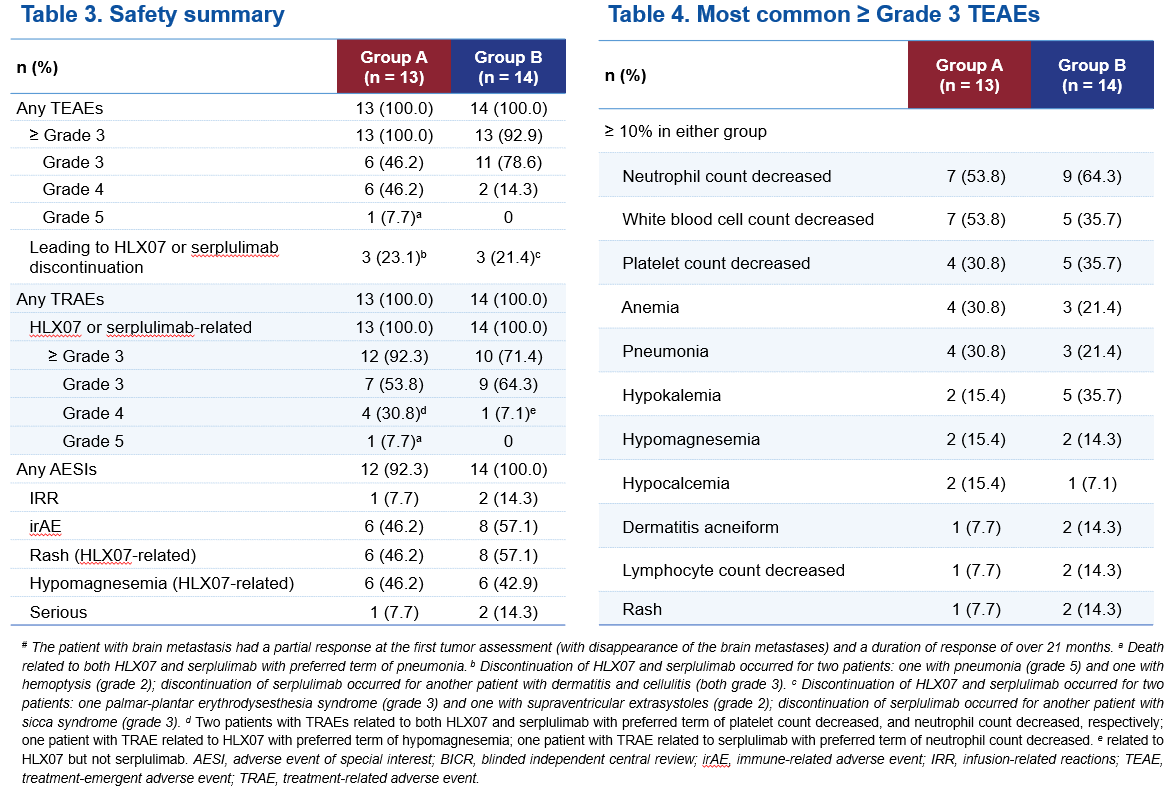
两组所有患者均报告了治疗期间不良事件(TEAE),常见的≥3级TEAE以皮肤反应、电解质紊乱为主,与同类药物相比,未发现新的安全性信号。
复宏汉霖在肺癌治疗领域持续深耕,从斯鲁利单抗引领小细胞肺癌免疫治疗,到HLX43、HLX07等多元管线覆盖非小细胞肺癌多个分子特征,公司正逐步构建差异化、全人群覆盖的产品矩阵。本研究的积极结果不仅验证了EGFR靶向与免疫治疗联合的可行路径,也为填补EGFR高表达sqNSCLC一线治疗空白提供了新可能,为后续更大规模研究蓄势。
关于复宏汉霖
复宏汉霖(2696.HK)是一家国际化的创新生物制药公司,致力于为全球患者提供可负担的高品质生物药,产品覆盖肿瘤、自身免疫疾病、眼科疾病等领域,已在全球获批上市9款产品,5个上市申请分别获中国药监局、美国FDA和欧盟EMA受理。自2010年成立以来,复宏汉霖已建成一体化生物制药平台,高效及创新的自主核心能力贯穿研发、生产及商业运营全产业链。公司已建立完善高效的全球创新中心,按照国际药品生产质量管理规范(GMP)标准进行生产和质量管控,不断夯实一体化综合生产平台,其中,公司商业化生产基地已相继获得中国、欧盟和美国GMP认证。
复宏汉霖前瞻性布局了一个多元化、高质量的产品管线,涵盖约50个分子,并全面推进基于自有抗PD-1单抗H药汉斯状®的肿瘤免疫联合疗法。截至目前,公司已获批上市产品包括全球首个获批一线治疗小细胞肺癌的抗PD-1单抗汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)、自主研发的中美欧三地获批单抗生物类似药汉曲优®(曲妥珠单抗,美国商品名:HERCESSI™,欧洲商品名:Zercepac®)、国内首个生物类似药汉利康®(利妥昔单抗)、以及地舒单抗生物类似药Bildyos®和Bilprevda®。公司亦同步就19个产品在全球范围内开展30多项临床试验,对外授权全面覆盖欧美主流生物药市场和众多新兴市场。
【参考文献】
[1] Prabhakar CN. Epidermal growth factor receptor in non-small cell lung cancer. Transl Lung Cancer Res. 2015;4(2):110-118. doi:10.3978/j.issn.2218-6751.2015.01.01
[2] Karlsen E-A, Kahler S, Tefay J, Joseph SR, Simpson F. Epidermal Growth Factor Receptor Expression and Resistance Patterns to Targeted Therapy in Non-Small Cell Lung Cancer: A Review. Cells. 2021; 10(5):1206. https://doi.org/10.3390/cells10051206
[3] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263.
[4] Tseng,Yun-Chih Cheng, Chieh-Hsin Ho, Shih Chieh Chen, Yanling Wang, Eugene Liu,Hassan Issafras & Weidong Jiang (2021) Distinguishing features of a novelhumanized anti-EGFR monoclonal antibody based on cetuximab with superiorantitumor efficacy, Expert Opinion on Biological Therapy, 21:11, 1491-1507.