-在头对头非人灵长类动物研究中,ASC35的平均表观半衰期(observed half-life)约为14天,比替尔泊肽长6倍,支持在人体中每月一次皮下给药。
-在头对头非人灵长类动物研究中,ASC35静脉注射和皮下注射后的药物暴露量比替尔泊肽静脉注射和皮下注射分别高约80%和70%。
-体外实验显示,ASC35对GLP-1受体(GLP-1R)和GIP受体(GIPR)的激动活性比替尔泊肽强约4倍。
-在头对头饮食诱导肥胖(DIO)小鼠研究中,ASC35的减重效果较替尔泊肽相对提升约71%。
-预计将于2026年第二季度向美国食品药品监督管理局(FDA)递交ASC35新药临床试验申请(IND)。
香港,2025年10月13日--歌礼制药有限公司(香港联交所代码:1672,简称“歌礼”)宣布,已选定一款有望成为同类最佳每月一次皮下注射GLP-1受体(GLP-1R)/GIP受体(GIPR)双靶点激动剂多肽ASC35作为临床开发候选药物。歌礼预计将于2026年第二季度向美国食品药品监督管理局(FDA)递交ASC35治疗肥胖症的新药临床试验申请(IND)。
ASC35是利用歌礼基于结构的AI辅助药物发现(Artificial Intelligence-Assisted Structure-Based Drug Discovery,AISBDD)和超长效药物开发平台(Ultra-Long-Acting Platform,ULAP)技术自主研发的GLP-1R与GIPR双靶点激动剂多肽。体外实验显示,ASC35对GLP-1R和GIPR的激动活性比替尔泊肽强约4倍。与每周一次给药的替尔泊肽相比,经设计优化的ASC35实现了更长的表观半衰期(以血药浓度降至Cmax的50%所需时间计)及更高的每毫克多肽生物利用度,从而支持每月一次皮下给药,且注射体积不超过1毫升。这些经设计优化的特性使其在规模化生产中成本更低(scalability advantages in manufacturing)。
在头对头非人灵长类动物研究中,ASC35缓释皮下储库型(depot)制剂的平均表观半衰期(observed half-life)约为14天,比FDA批准的替尔泊肽皮下制剂长6倍。在头对头非人灵长类动物研究中,ASC35静脉注射和皮下注射后的药物暴露量(以血药浓度曲线下面积计)比替尔泊肽静脉注射和皮下注射分别高约80%和70%。非人灵长类动物与人体间的药代动力学关系已得到多款激动剂多肽充分验证。例如,替尔泊肽在非人灵长类动物中的半衰期为56小时,在人体内的半衰期则为128小时(5.3天)[1]。因此,根据非人灵长类动物研究预测,ASC35在人体中的表观半衰期可能不少于30天。这些临床前数据支持ASC35在人体中每月一次给药治疗肥胖症。与其它肠促胰素多肽相比,ASC35在非人灵长类动物中有更长的表观半衰期及更平缓的药代动力学特征,这些优势也可能使其在人体中具有更好的胃肠道耐受性。
在头对头饮食诱导肥胖(DIO)小鼠研究中(DIO模型已被证实对人体中的疗效具有高度预测性),给药相同摩尔浓度的ASC35和替尔泊肽,ASC35减重达33.6%,替尔泊肽达19.6%,ASC35的减重效果相对提升达71%(表1)。每毫克多肽的减重效果更优,也可能使ASC35在规模化生产中成本更低。
表1. 在DIO小鼠中,ASC35的减重效果显著优于替尔泊肽,且差异具有统计学显著性
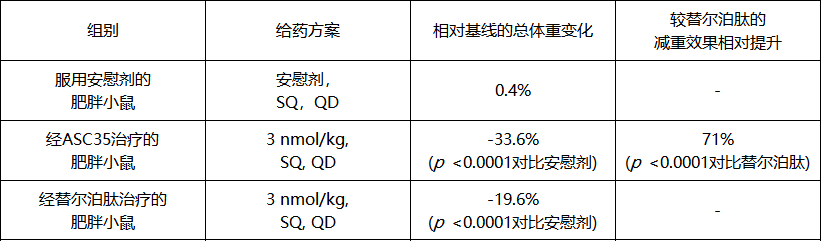
注释:治疗周期:14天;DIO小鼠/肥胖小鼠:饮食诱导肥胖小鼠;SQ:皮下注射;QD:每日一次。
ASC35在体外激动活性、表观半衰期、皮下生物利用度及减重效果方面均优于替尔泊肽,这些优势表明其有望成为同类最佳的肥胖症疗法。
歌礼创始人、董事会主席兼首席执行官吴劲梓博士:“我们的首款激动剂多肽进入临床开发阶段彰显了公司对创新的承诺,也与我们的小分子药物管线形成了战略互补,以治疗肥胖症及其他代谢疾病。
临床前特性表明,ASC35有望实现同类最佳疗效及每月一次的给药频率,这些特点可能带来优越的减重效果和更简便、对患者更友好的剂量滴定(titration)方案。”
ASC35潜在联合疗法研究
ASC35正在作为单药及联合疗法进行开发,用于治疗心脏代谢疾病,包括肥胖症、糖尿病和代谢功能障碍相关脂肪性肝炎(MASH)。歌礼计划将GLP-1R/GIPR双靶点激动剂ASC35与每月一次皮下给药的胰淀素(amylin)受体激动剂多肽ASC36联用,治疗肥胖症和糖尿病。歌礼还计划将ASC35与每月一次皮下给药的脂肪靶向甲状腺受体β(THRβ)激动剂ASC47联用,用于治疗肥胖症及代谢功能障碍相关脂肪性肝炎等多种代谢疾病。
歌礼的AISBDD与ULAP技术可设计、优化并开发多款每月一次皮下注射超长效多肽,包括ASC35和ASC36。基于多肽的特性,本公司可利用其专有的ULAP技术,为皮下储库中的多肽设计多种缓释速率常数(k),从而在预设的给药间隔内精确释放注射的多肽,降低血药浓度峰谷比并改善临床疗效。
[1] Jennifer A Martin et al, Absorption, distribution, metabolism, and excretion of tirzepatide in humans, rats, and monkeys, European Journal of Pharmaceutical Sciences 202 (2024)106895, https://doi.org/10.1016/j.ejps.2024.106895
关于歌礼制药有限公司
歌礼制药有限公司是一家全价值链整合型生物技术公司,聚焦有望成为治疗代谢疾病同类最佳(best-in-class)和同类首创(first-in-class)药物的开发和商业化。利用公司专有的基于结构的AI辅助药物发现(Artificial Intelligence-Assisted Structure-Based Drug Discovery,AISBDD)和超长效药物开发平台(Ultra-Long-Acting Platform,ULAP)技术,歌礼已自主研发多款候选药物,包括其核心项目:ASC30,一款在研小分子GLP-1受体(GLP-1R)激动剂,既可每日一次口服也可每月一次至每季度一次皮下注射作为减重治疗疗法和减重维持疗法,用于长期体重管理。歌礼已在香港联交所上市(1672.HK)。