2025年10月18日,四川科伦博泰生物医药股份有限公司(下称“科伦博泰”或“公司”,6990.HK)宣布,在德国柏林举行的2025年欧洲肿瘤内科学会(ESMO)年会上,大连医科大学第二附属医院李曼教授以口头报告形式公布了靶向人滋养细胞表面抗原2(TROP2)的抗体偶联药物(ADC)芦康沙妥珠单抗(sac-TMT,商品名:佳泰莱®)用于经治局部晚期或转移性激素受体阳性(HR+)人类表皮生长因子受体2阴性(HER2-)乳腺癌(BC)的III期OptiTROP-Breast02研究结果(报告编号:LBA23,优选论文专场1:转移性乳腺癌)。此前,芦康沙妥珠单抗(sac-TMT)用于治疗这一适应症的新增适应症上市申请已获国家药品监督管理局(NMPA)受理,并被纳入优先审评审批程序。

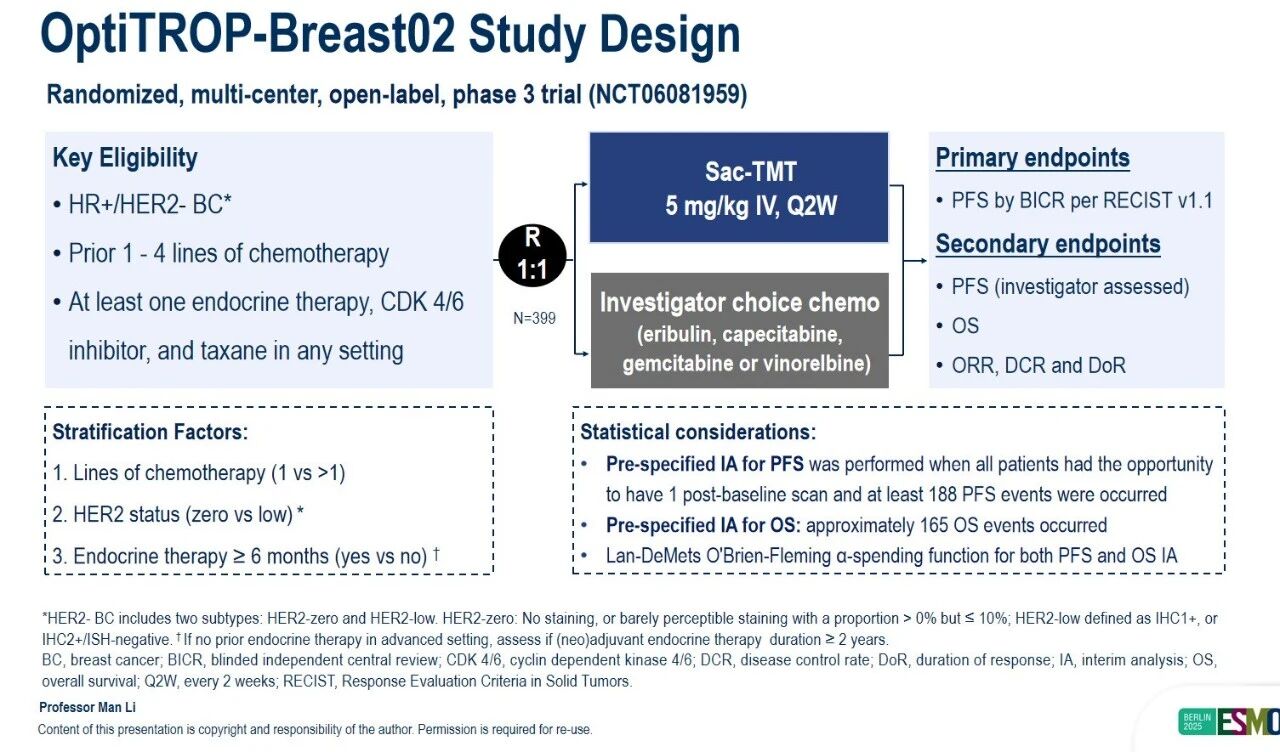
在OptiTROP-Breast02研究中,共有399例既往接受过CDK4/6抑制剂治疗且在晚期或转移性阶段接受过至少一种化疗后进展的HR+/HER2- BC患者,被随机(1:1)分配接受芦康沙妥珠单抗(sac-TMT)或研究者选择的化疗(ICC)治疗。
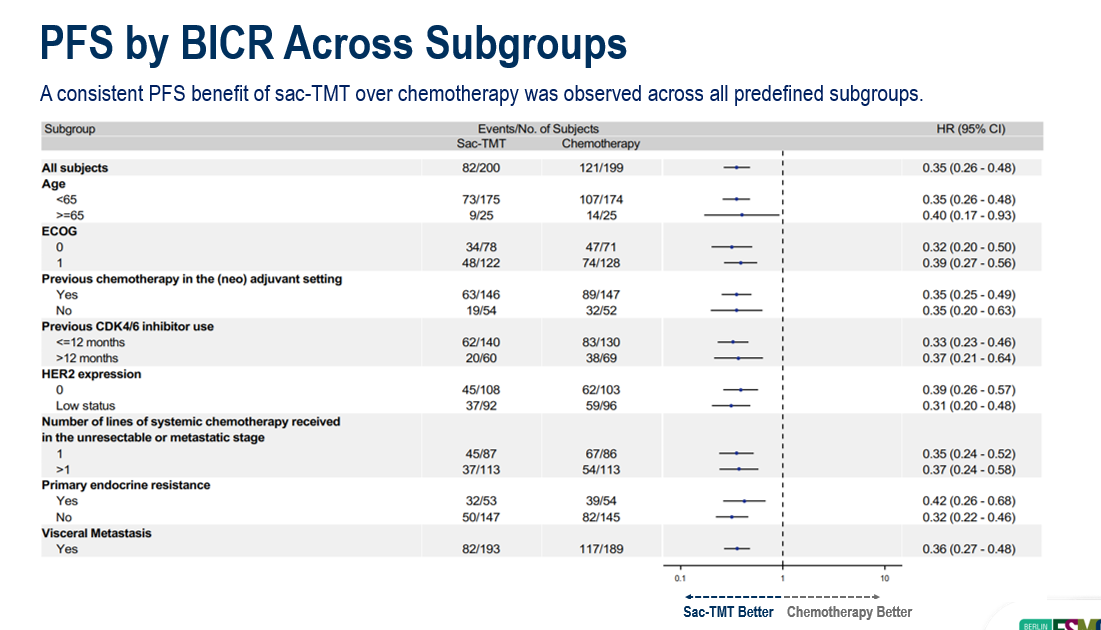
数据截至2025年1月22日,芦康沙妥珠单抗(sac-TMT)组的中位PFS较ICC组有显著延长(8.3个月对比4.1个月;HR, 0.35;95% CI, 0.26-0.48;P<0.0001),且在不同HER2表达水平的患者中均观察到临床获益(PFS的HR:在HER2不表达患者中为0.39, 95% CI, 0.26-0.57;在HER2低表达患者中为0.31, 95% CI, 0.20-0.48)。
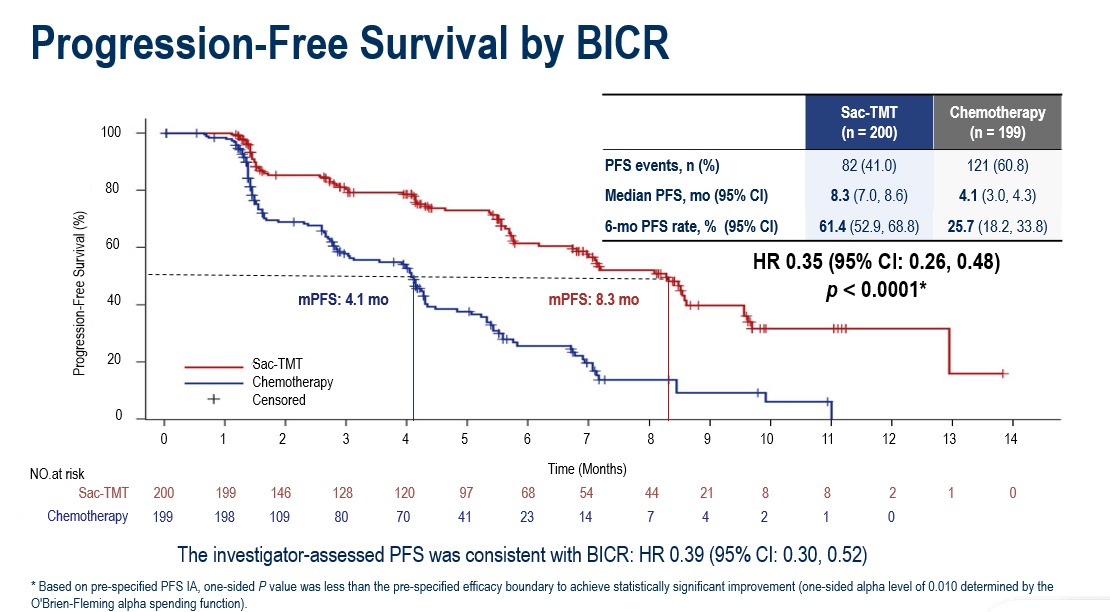
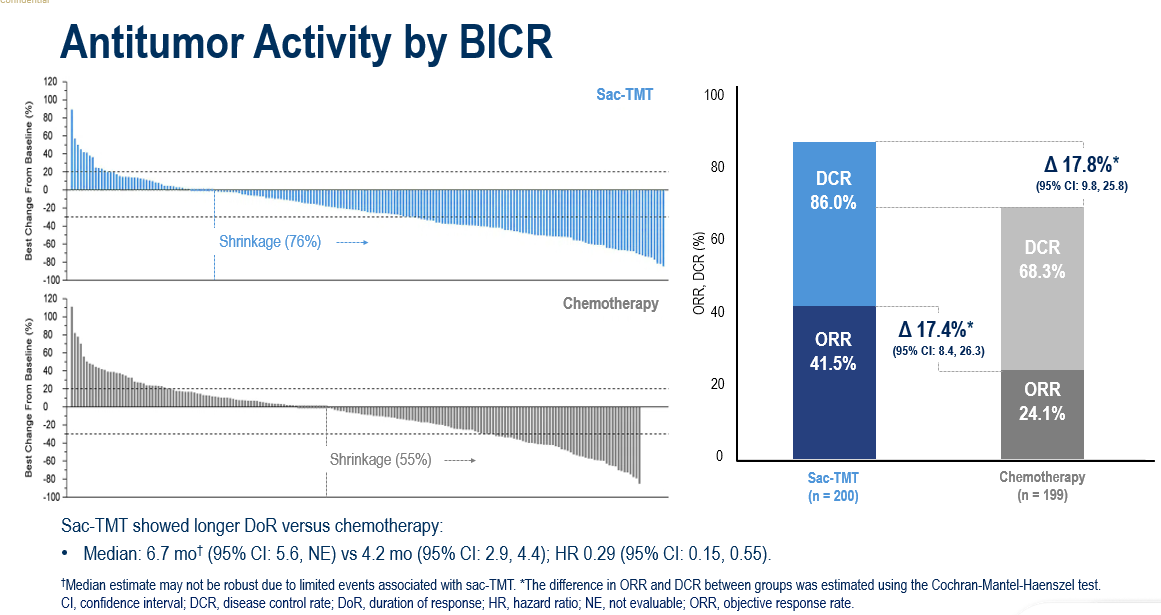
芦康沙妥珠单抗(sac-TMT)相较化疗显示出更长的持续缓解时间(DoR),其客观缓解率(ORR)亦优于ICC组。
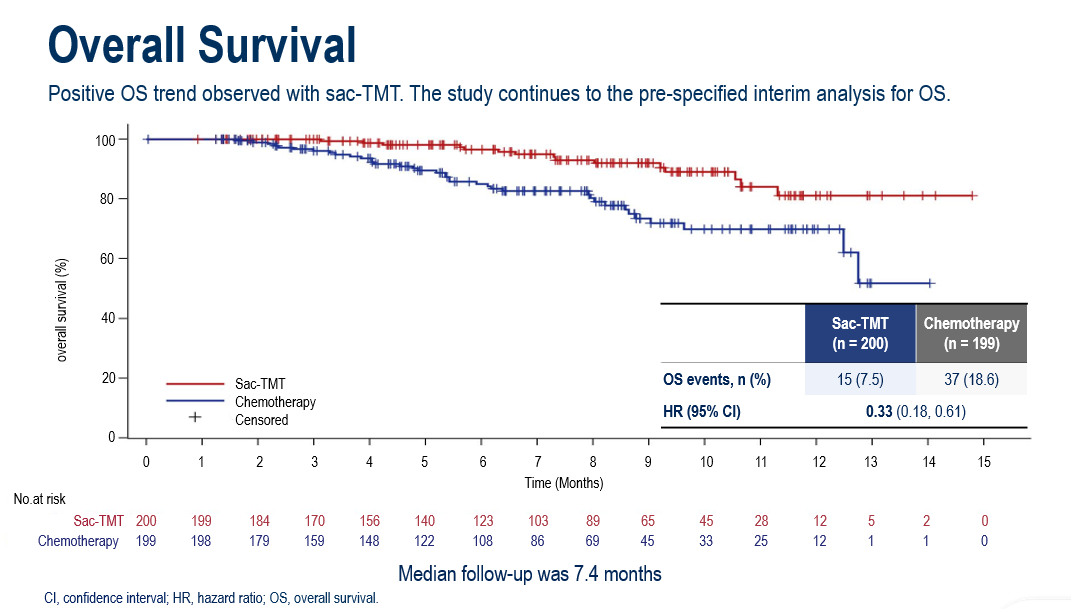
芦康沙妥珠单抗(sac-TMT)组的OS相对ICC组存在更有利的趋势 (HR, 0.33; 95% CI, 0.18-0.61)。
62.0%的芦康沙妥珠单抗(sac-TMT)组患者和64.8%的ICC组患者出现了3级以上治疗相关不良事件(TRAE)。0%的芦康沙妥珠单抗(sac-TMT)组患者和0.5%的ICC组患者因TRAE导致停药;1.5%的芦康沙妥珠单抗(sac-TMT)组患者和1.0%的ICC组患者出现肺炎病例(均为1-2级)。
研究表明,芦康沙妥珠单抗(sac-TMT)的PFS相比化疗显示出统计学意义及临床意义的显著改善,且在所有预设亚组以及不同HER2表达水平的患者中均观察到PFS获益。芦康沙妥珠单抗(sac-TMT)同样显示出OS的获益趋势(HR, 0.33;95% CI: 0.18-0.61),并表现出良好且可管理的安全性特征,未发现新的安全性信号。目前,芦康沙妥珠单抗单药和联合pembrolizumab用于治疗未接受过化疗的HR+/HER2-乳腺癌患者的全球III期临床研究(NCT06312176)正在开展,计划入组1200人;另外一项在相同人群中在中国开展的III期注册研究(NCT07071337)正在入组患者,计划入组430人。
大连医科大学第二附属医院李曼教授表示:经III期OptiTROP-Breast02研究证实,无论HER2表达状态如何,芦康沙妥珠单抗(sac-TMT)在经治HR+/HER2-乳腺癌患者中均显示出治疗潜力。作为首个聚焦HR+/HER2-晚期乳腺癌全中国人群的III期临床试验,OptiTROP-Breast02研究数据在ESMO大会的发布,标志着中国在该适应症领域临床研究的重要突破。这项研究的积极成果不仅为HR+/HER2-乳腺癌治疗提供了循证依据,更为乳腺患者提供了安全、可靠的全新治疗选择。
关于芦康沙妥珠单抗(sac-TMT,佳泰莱®)
作为本公司的核心产品,芦康沙妥珠单抗(sac-TMT)是一款本公司拥有自主知识产权的新型TROP2 ADC,针对NSCLC、BC、胃癌(GC)、妇科肿瘤等晚期实体瘤。Sac-TMT采用新型连接子进行开发,其通过偶联一种贝洛替康衍生的拓扑异构酶I抑制剂作为有效载荷,药物抗体比(DAR)达到7.4。Sac-TMT通过重组抗TROP2人源化单克隆抗体特异性识别肿瘤细胞表面的TROP2,其后被肿瘤细胞内吞并于细胞内释放有效载荷KL610023。KL610023作为拓扑异构酶I抑制剂,可诱导肿瘤细胞DNA损伤,进而导致细胞周期阻滞及细胞凋亡。此外,其亦于肿瘤微环境中释放KL610023。鉴于KL610023具有细胞膜渗透性,其可实现旁观者效应,即杀死邻近的肿瘤细胞。
于2022年5月,本公司授予默沙东(美国新泽西州罗威市默克公司的商号)在大中华区(包括中国内地、香港、澳门及台湾)以外的所有地区开发、使用、制造及商业化sac-TMT的独家权利。
截至目前,sac-TMT的3项适应症已于中国获批上市,分别用于治疗既往至少接受过 2 种系统治疗(其中至少1种治疗针对晚期或转移性阶段)的不可切除的局部晚期或转移性三阴性乳腺癌(TNBC)、经EGFR-TKI和含铂化疗治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状NSCLC以及经EGFR-TKI治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状NSCLC。Sac-TMT是全球首个在肺癌适应症获批上市的TROP2 ADC药物。此外,sac-TMT用于治疗既往接受过内分泌治疗且在晚期或转移性阶段接受过其他系统治疗的不可切除的局部晚期或转移性激素受体阳性(HR+)且人类表皮生长因子受体2阴性(HER2-)BC的新增适应症上市申请已获CDE受理,并被纳入优先审评审批程序。
目前,科伦博泰已在中国开展9项注册性临床研究。默沙东已启动15项正在进行的sac-TMT作为单药疗法或联合帕博利珠单抗*或其他抗癌药物用于多种类型癌症的全球性3期临床研究(这些研究由默沙东申办并主导)。
*帕博利珠单抗(可瑞达®)为美国新泽西州罗威市默克公司的附属公司Merck Sharp & Dohme LLC (MSD)的注册商标
关于科伦博泰
四川科伦博泰生物医药股份有限公司(简称“科伦博泰生物”,股票代码:6990.HK)是科伦药业控股子公司,专注于创新生物技术药物及小分子药物的研发、生产、商业化及国际合作。公司围绕全球和中国未满足的临床需求,重点布局肿瘤、自身免疫、炎症和代谢等重大疾病领域,建设国际化药物研发与产业化平台,致力于成为在创新药物领域国际领先的企业。公司目前拥有30余个重点创新药项目,其中4个项目已获批上市,1个项目处于NDA阶段,10余个项目正处于临床阶段。公司成功构建了享誉国际的专有ADC及新型偶联药物平台OptiDCTM,已有2个ADC项目获批上市,多个ADC或新型偶联药物产品处于临床或临床前研究阶段。