写这篇文章,是希望拨开喧嚣的“AI万能论”和悲观的“全是泡沫论”,呈现一个更平衡、更务实的图景。

研发客:冯文昌博士,我听说您最近在《医学评论》期刊上发表了一篇新论文,题为《超越炒作:人工智能(AI)在医疗健康中的真实应用图景》,能给我们讲讲这篇文章主要讲了什么?又是什么促使您写这样一篇综述?
冯博士:
是的,这篇论文是我应《医学评论》主编的邀请撰写的。当时他希望有一篇既全面又接地气的综述,帮助生物医药领域的同行,无论是临床医生、药企研发人员,还是政策制定者, 快速把握AI在医疗医药中“到底能做什么、不能做什么、风险在哪、未来又在哪”。我觉得这个任务很有意义,于是花了整整6个月时间,系统梳理了全球四大监管机构(FDA、EMA、PMDA、NMPA)在AI监管上的最新实践,分析了AIDD(人工智能驱动的药物发现)、临床辅助诊断、真实世界证据生成等场景的最新进展与瓶颈。
这篇文章的核心观点其实就一句话:AI不是魔法,但也不是泡沫;它是工具,更是新范式。比如在新药研发领域,传统模式靠“试错+运气”,而AIDD正在把流程变成“理解—建模—设计—验证”的理性工程。我们看到已有项目从靶点发现到进入临床只用了1~2年,远快于传统3~5年的周期。但这不意味着所有AI公司都靠谱;真正经得起考验的,是那些能把AI深度嵌入从分子设计到患者分层全链条,并拿出II~III期临床数据的 “AI原生制药公司”(AI-Native Pharma)。
同时,我也花了很大篇幅讨论挑战。比如“黑箱”问题如何侵蚀临床信任,AI“幻觉”如何可能导致错误引用,训练数据偏差又怎样加剧医疗不平等。更重要的是,我强调:技术再先进,也必须服务于人。所以文章特别指出,FDA和EMA都不允许AI替代人类判断,而是定位为“增强智能”,最终签字做决策的永远是医生或监管机构的审评员。
写这篇文章,是希望拨开喧嚣的“AI万能论”和悲观的“全是泡沫论”,呈现一个更平衡、更务实的图景。毕竟,医疗关乎生命,容不得半点浮夸。而真正的突破,往往发生在实验室、临床和监管三者协同的交汇点上。这篇文章如果能让更多从业者少走弯路、多做实事,那我这6个月就没有白熬了。
研发客:当前,AI在医疗健康领域的应用可谓炙手可热,您作为这一交叉领域的资深专家,能否先为我们概括一下:AI究竟正在如何重塑现代医学的整体格局?
冯博士:
确实,AI已经不只是一个技术热点,而是正在深度重构整个医疗体系。简单来说,它正从三个核心维度推动变革:一是优化临床诊疗与医疗服务流程,比如通过预测模型,提前干预高风险患者;二是加速临床科学发现,像用机器学习和其它AI工具挖掘新的生物标志物或治疗路径;三是彻底改变药物研发模式。过去需要十年、耗资数十亿美元的创新药,现在借助AI可能几个月就能锁定候选分子。可以说,AI正在把传统的“经验医学”推向“精准+预见性医学”。
研发客:听起来非常振奋人心!那在实际临床场景中,AI具体是怎么“落地”的?有没有一些已经产生明显效果的例子?
冯博士:
有的,而且不少已经进入日常使用。比如在影像科,卷积神经网络(CNN)能比资深放射科医生更快、更准地识别肺部小结节;在急诊,随机森林算法可以预测未来几小时的患者流量,帮助医院动态调配人力和床位;还有大型语言模型(LLM),能实时分析电子病历,一旦发现患者有脓毒症早期迹象,立刻给出评估和用药建议。甚至在康复领域,强化学习正在调控外骨骼机器人,让中风患者恢复得更快。这些都不是未来幻想,而是今天很多医院已经在试用或部署的技术。
AI在药物研发中的应用
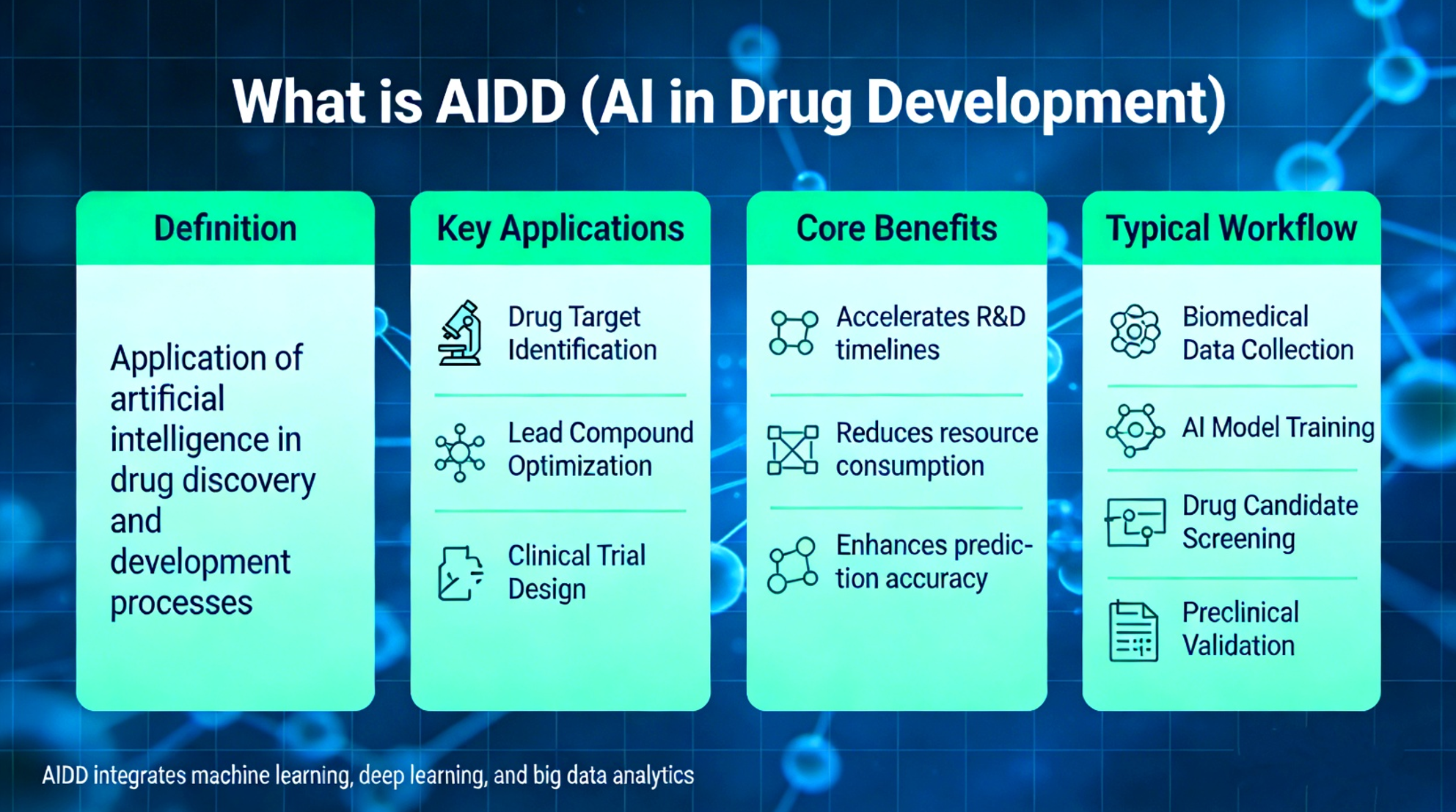
研发客:冯博士,当下最热的莫过于AIDD了。大家常说新药研发“十年十亿美金”,AI真的能打破这个魔咒吗?它具体在哪些环节带来了提速?
冯博士:
完全可行,而且已有成功案例。AI正在从源头重塑整个药物研发流程。比如在靶点发现阶段,AI能快速分析海量科学文献和多组学数据,找出过去被忽略的致病通路;例如BenevolentAI就帮阿斯利康发现了5个全新靶点,其中一个(SRF)已被实验证实与肺纤维化密切相关。到了分子设计环节,生成式AI如GAN能 “从零创造” 具有理想特性的新化合物。英矽智能用AI设计的抗肺纤维化候选药,仅18个月就从靶点推进到临床前验证,而传统流程通常要好几年。
研发客:这些进展一般都会用上那类的AI工具,能否展开说说?
冯博士:
在生物医学研究中,深度学习模型能同时分析基因组、转录组、蛋白组等多组学数据,找出哪些突变组合预示着患者对免疫治疗有反应, 这比单看一种数据准得多。像LASSO、XGBoost这些经典算法,加上新兴的图神经网络,已经能高效预测免疫治疗效果,而深度学习在新抗原预测上尤其突出。更有意思的是迁移学习:先用TCGA这样的大型癌症数据库训练模型,再微调用于本地小样本队列,既省GPU算力,又能捕捉罕见致癌变异。到了药物研发端,生成对抗网络(GAN)更是打开了“分子想象力”的天花板。比如GENTRL系统,仅用46天就从零设计出全新的DDR1激酶抑制剂, 传统方法可能要几年。它的机制是:生成器不断提出新分子结构,判别器立刻筛掉违反“类药五原则”或有心脏毒性风险的,再通过强化学习优化剩下的候选物,确保它们既有效、又可合成。不仅如此,AI还能整合医保理赔和历史试验数据,提前预判某个临床试验会不会招不到人、会不会出现安全信号,让药企把钱花在刀刃上。可以说,AI正在把新药研发从“碰运气”变成“精准工程”。
研发客:原来如此,我们是否可以说AIDD已从根本上改变新药研发的方式?
冯博士:
AIDD彻底改变了传统的 “发现 — 筛选 — 试错” 模式。传统方式依赖于大量的实验时间和研发周期,并且具有很高的失败率。而AIDD推动行业走向一个更加理性的流程:“理解 — 建模 — 设计 — 验证 — 迭代”。这种方式允许我们在更早阶段识别失败的可能性,使得失败成本更低、更容易解释,同时也提高了早期成功的几率并大幅缩短了研发时间。特别是在癌症或阿尔茨海默病等复杂疾病的治疗中,AIDD能够围绕那些被反复验证但总是失败的“问题靶点”,通过计算模拟优先筛选出从未合成过但从机制上看更有潜力的候选药物。
研发客:听起来AIDD确实带来了许多创新,那么它具体上,它是如何帮助科学家找到全新机制的呢?
冯博士:
AIDD的其中一个关键工具是从零设计 (De Novo Design),这标志着AI能真正成为“发明引擎”。此外,AIDD并不局限于人类预先设定的分子骨架进行调整,而是基于目标结构、物理化学性质及ADME/毒性等多重要求,在庞大的化学-生物空间内自动生成全新的分子骨架。这种能力让科学家们可以探索超出直觉范围之外的设计方案,比如开发针对病变微环境条件激活的分子或是能够同时调节多条通路的网络药理学分子。这些往往是大多数科学家难以想象或尝试的方案,但在AI的多目标优化下成为可能。
研发客:听说现在连临床试验都用上了AI,这又是怎么提高效率的?
冯博士:
是的,AI让临床试验变得更智能、更精准。首先,它能自动比对电子病历和入组标准,快速筛选合适患者,大幅缩短招募时间;其次,通过分析历史数据和地理信息,AI还能优化试验中心选址,提升入组效率。最震撼的例子是英矽智能,他们把肺纤维化药物的II期试验启动时间压缩到传统周期的一半,成本也降到十分之一。此外,AI还能优化剂量方案、选择终点,帮助寻找有效的生物标志物来筛选更能受益的患者,甚至预测受试者脱落风险,让整个试验设计更科学、更高效。
研发客:AIDD在临床试验的未来前景将会如何?它将如何影响医疗实践?
冯博士:
在未来,AIDD将与精准医疗深度融合,从“为疾病找药”转向“为个体设计新药”。每位患者的基因组、代谢图谱和免疫特征都将作为算法输入,支持半定制乃至完全定制化的治疗方案,尤其是在癌症和神经退行性疾病领域。此外,随着数字孪生 (Digital Twin) 患者技术的发展,AI辅助的患者分层以及“虚拟临床+真实验证”的混合模式将使临床试验变得更加精确、高效且节省资源。这意味着我们不仅能更快地找到有效的治疗方法,还能更好地预测药物对特定个体的效果,从根本上改变这些“医学黑洞”的研究逻辑。最终,这不仅会提升治疗效果,还会降低整体医疗成本,开启个性化医疗的新时代。
研发客:除了开发新药,AI在“老药新用”和安全性评估方面也有建树吧?能不能举个实际例子?
冯博士:
当然有!“老药新用”是AI大显身手的领域。2020年初,BenevolentAI通过知识图谱 (Knowledge Graph) 分析,迅速锁定类风湿关节炎药物巴瑞替尼(Baricitinib)可能对新冠有效,后来果然获得FDA紧急使用授权。在安全性方面,AI还能提前预测药物的ADME/T特性(吸收、分布、代谢、排泄和毒性),减少后期失败风险。更进一步,它还能通过真实世界数据(比如医保记录、电子病历)实时监测上市后药物的不良反应,比传统自发报告系统更敏感、更及时,极大加强了药物警戒能力。
研发客:请您展望一下,AI在生物医学研究中的整合,是否正在催生一种全新的科研范式?
冯博士:
确实如此。AI不再只是工具,而是正在构建一个“可计算的生物医学知识体系”。比如,AlphaFold和RoseTTAFold能高精度预测蛋白质结构,甚至揭示新的结合口袋;多组学整合平台如MOFA、DeepOmics能把基因、蛋白、代谢数据融合起来,模拟疾病机制;知识图谱如Open Targets则把疾病、基因、药物的关系可视化。这些技术让我们能在计算机里“预演”疾病进展和治疗反应,推动科研从“试错式”走向“预测式”。可以说,AI正在把药物研发和基础研究带入一个更快、更准、更个性化的全新时代。
AI在监管科学中的应用
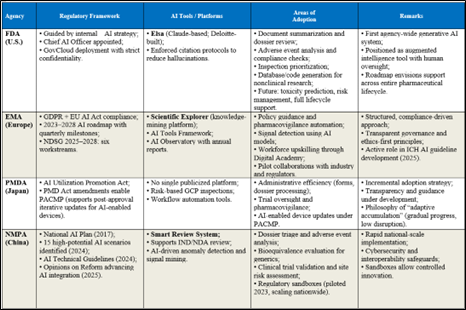
摘录自冯博士《医学评论》期刊的学术论文表二
研发客:冯博士,FDA是如何利用AI来改进其药品审批流程的?能给我们介绍一下Elsa这个平台吗?
冯博士:
Elsa是FDA在2025年6月正式部署的一个基于先进大语言模型的生成式AI平台。它由Deloitte与Anthropic合作开发,运行在一个安全的GovCloud环境中。Elsa能够自动化许多复杂且耗时的监管任务,比如文档合成、不良事件报告分析、临床协议评估等。通过使用验证过的文档库和强制引用机制,Elsa大大提高了关键过程的效率,如安全档案摘要、标签内容和快速比较评估等。
研发客:听起来Elsa确实很有用,但它有没有遇到过什么挑战呢?
冯博士:
确实有挑战。例如,“幻觉”现象(AI Hallucination),系统可能会编造不存在的研究或监管文件的引用。不过,FDA已经采取措施解决这个问题,当Elsa配置为仅使用经过验证的文档库并启用强制引用机制时,“幻觉”的风险显著降低。长远来看,Elsa的目标是支持整个药品生命周期的所有阶段,包括从上市后监测到风险管理。
研发客:那么欧洲EMA在这方面有什么进展呢?
冯博士:
EMA也非常积极地将AI整合进其监管框架。2024年9月,EMA发布了关于“医药产品生命周期中AI使用”的最终反思报告,并制定了一个涵盖2023至2028年的AI工作计划。其中一个重要里程碑是Scientific Explorer平台的推出,它帮助欧盟监管者更高效地处理复杂的科学建议文档,从而实现更快、更精确的决策。
研发客:日本PMDA在AI应用方面有什么特别之处吗?
冯博士:
PMDA已于2025年10月正式发布了《PMDA监管中人工智能应用行动计划》。该计划系统阐述了PMDA对AI技术在审评审批流程中应用的当前思考与具体实施举措。随着众多企业日益广泛地将AI工具应用于研究及注册资料撰写工作,PMDA亦准备在内部审评流程中整合相关技术。为此,PMDA正通过开展专项培训持续提升审评员的专业能力,以确保能够对AI技术进行恰当且高效的评估。此外,PMDA还修改了《药品和医疗器械法》,加入了批准后变更管理协议(PACMP),以确保AI驱动的医疗设备在批准后的持续改进和迭代更新符合规范。
研发客:中国NMPA在这一领域有哪些举措?
冯博士:
中国NMPA非常重视AI在药物监管中的应用,发布了“药物管理典型AI应用场景清单”,详细描述了如何将AI嵌入监管实践。例如,NMPA使用的“智能审核系统”集成了机器学习算法,用于优先处理监管提交、检测档案中的异常以及自动化常规合规检查。这些措施不仅减轻了人工负担,还加快了审批时间。另外,药品审评中心(CDE)发文通知自2026年3月起,化学药品、化学原料药和生物制品的药物临床试验申请、药品上市许可注册申请、补充申请、境外生产药品再注册申请和仿制药一致性评价申请等,可按照eCTD方式申报。这一模块化、结构化、电子化申报资料递交方式,标志着CDE在收集高质量数据上又迈出一步,也为后续开展AI训练与学习打下基础,进一步推动AI在审评审批中的应用。
研发客:大家总说AI能提升监管效率,但除了“快”和“省”,它对监管科学本身有没有更深层的价值?
冯博士:
效率只是起点,AI真正的潜力在于重塑监管科学的底层逻辑。比如,不同审评员在不同时间看同一份材料,结论有时会有差异,这叫“审评变异性”。AI可以通过申报资料结构化的监管知识库和可追溯的证据链,让决策依据更一致、更透明。更重要的是,新药审评早已不只依赖临床试验数据,还要整合真实世界证据、上市后安全信号、甚至患者报告等补充信息。AI能将这些碎片化、多源的数据流融合成一个连贯、可重复、可审计的决策支持框架,帮助监管者在不确定性中做出更稳健的判断。换句话说,AI不只是让审评“跑得更快”,而是让整个监管体系“想得更清、判得更准、说得更明”,这才是它对监管科学最深远的贡献。
研发客:全球主要药品监管机构在AI应用上的共同点是什么?
冯博士:
尽管各国监管机构的实施方式和速度有所不同,但有一个共同点是明确的:AI作为增强工具而非替代品的角色。所有监管机构都强调了AI必须在严格的人类监督下操作,确保科学完整性和患者安全。无论是FDA的Elsa平台带来的效率提升,EMA的细致三年AI路线图,还是PMDA和NMPA的谨慎推进策略,都表明了一个趋势:AI正在重新定义监管科学,压缩时间线,增强药物警戒,并开启一个以患者为中心的新时代。这种跨司法管辖区的协调努力预示着全球医疗产品监督架构的根本转变。
AI在医疗实践和医疗诊断中的应用
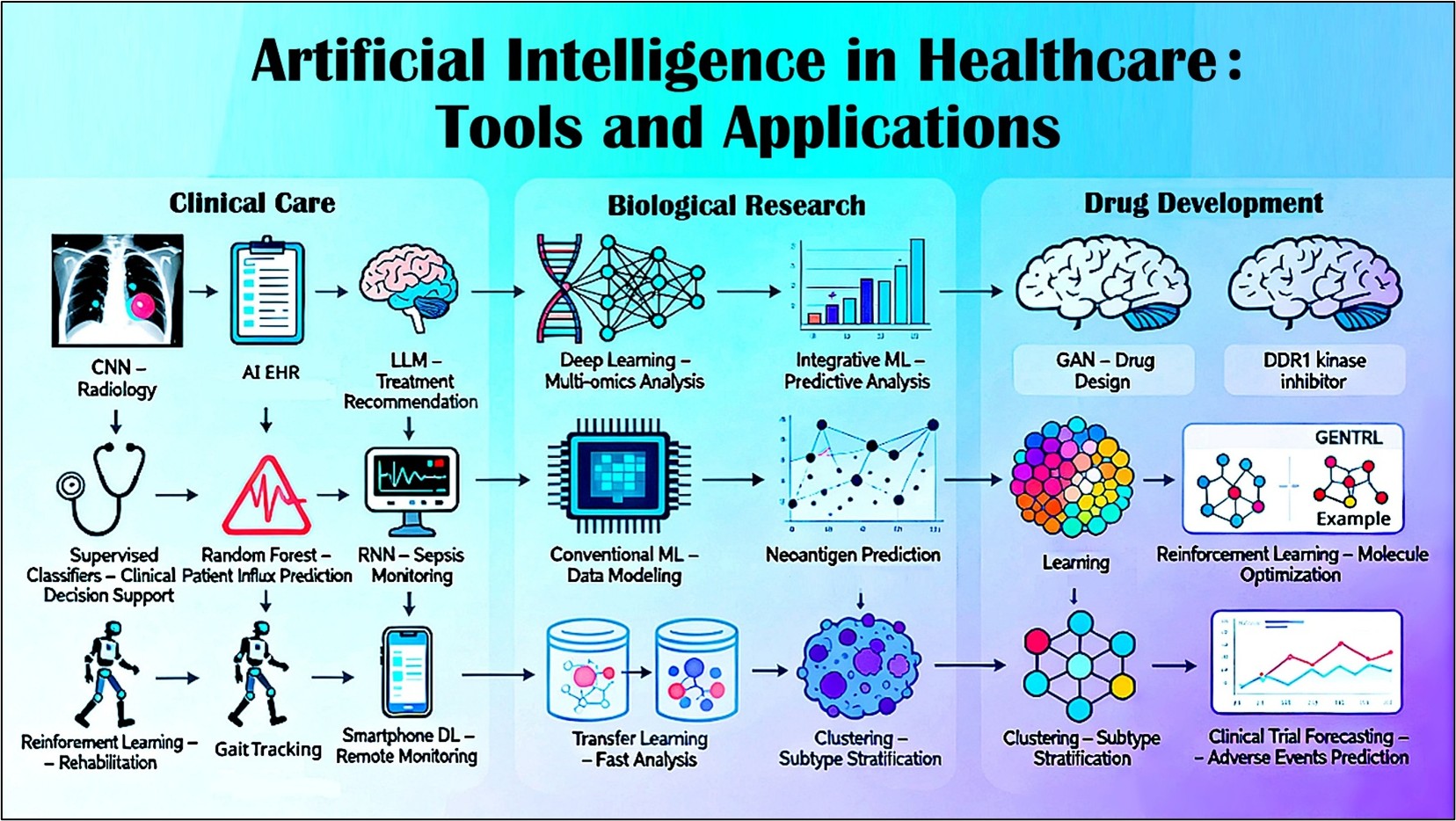
摘录自冯博士《医学评论》期刊的学术论文图一
研发客:冯博士,现在医院里AI应用越来越多,但很多人还是觉得“听起来很玄”。能不能举些实实在在的例子,说明AI到底在医疗实践干了什么?
冯博士:
AI早已不是实验室里的概念,而是每天在病房和门诊“干活”的助手。比如,在影像科,卷积神经网络(CNN),它看肺部CT的速度和准确率,甚至超过了经验丰富的放射科医生,能快速揪出微小的肺结节。在急诊和重症病房,循环神经网络(RNN)通过持续监测患者的心率、血压等生命体征,提前数小时预警脓毒症风险,让干预抢在病情恶化之前。而在日常管理上,大语言模型(LLM)能实时解析电子病历,不仅给出个性化的脓毒症评估,还能推荐治疗方案;随机森林算法(Random Forest) 则预测明天急诊会来多少病人,帮医院提前调配医护和床位。此外,在康复科,基于强化学习的外骨骼机器人,能根据患者动作实时调整助力强度;连智能手机都能用深度学习远程监测帕金森患者的震颤和步态,让医生远程调药,不用患者跑医院。这些工具不是要取代医生,而是作为“认知增强器”,让诊断更快、照护更准、资源更公平。
研发客:大家也常听说AI能提升医院运营效率,但具体是怎么做到的?它真的能帮医生“抢时间”甚至“救命”吗?
冯博士:
在重症预警方面,AI驱动的临床决策支持系统(CDSS)能实时分析电子病历数据,在患者出现明显症状前就预测出脓毒症或心脏骤停的风险,提前发出警报。有大量研究证实,这类算法的准确率非常高,能提高抢救成功率。同时,这些系统还能自动检查药物过敏、禁忌症或偏离指南的用药,相当于给医生配了个24小时在线的“安全助手”,大大减少人为疏漏。
研发客:除了临床诊疗,AI在医院管理、资源调度这些“后台”环节也有作用吗?
冯博士:
作用非常大!现在很多顶尖医院都建立了AI“指挥中心”。比如,AI能精准预测未来几天ICU床位需求、急诊就诊高峰,甚至手术室会不会延误,从而提前调配医护人力和设备。还有智能排班系统,通过分析患者历史行为,把爽约率降低了高达70%,既节省成本,又让更多病人及时看上病。说白了,AI让医院从“被动应对”转向“主动预判”,整个运营更流畅,患者体验也更好。
研发客:现在可穿戴设备很普及,AI和这些设备结合,真能实现“预防为主”的个性化健康管理吗?
冯博士:
这正是AI最令人期待的方向之一。比如,智能手表搭载AI模型,已经能较准确地筛查中重度睡眠呼吸暂停;糖尿病患者的连续血糖监测仪结合LSTM神经网络,可以提前几小时预测血糖波动,提醒调整饮食或胰岛素用量。更前沿的是“数字孪生”技术,该技术为每位患者建立一个动态虚拟模型,整合穿戴设备、饮食记录、代谢数据等,实时模拟不同治疗方案的效果。临床试验显示,用这种方式管理糖尿病,患者的血糖控制明显改善。这标志着医疗正从“生病才治”转向“未病先防、因人施治”的创新模式。
研发客:AI在医学影像和诊断方面有哪些突破性的进展?它真的能像专家那样准确识别病变吗?
冯博士:
确实可以。比如,在放射科领域,AI现在能够自动识别肿瘤、骨折、出血以及肺结节等关键病灶,这对于早期癌症筛查特别重要。有些AI系统甚至能在非对比CT扫描中快速发现大血管阻塞,从而加速中风诊断。研究表明,AI检测肺结节的敏感度可达95%,且假阳性率更低,性能堪比资深放射科医生,并超越了传统的计算机辅助检测系统。此外,专门用于中风诊断的AI模型如Methinks LVO也展示了高准确性,减少了诊断延迟,提高了工作效率。
研发客:听起来AI不仅在影像学上有所作为,在病理学和其他专科也有广泛应用吧?具体是怎么帮助医生提高诊断精度的呢?
冯博士:
在病理学中,AI增强了全切片图像分析,能够更精确地进行肿瘤分级、量化肿瘤浸润淋巴细胞、检测微转移并简化Gleason评分。眼科方面,FDA批准的IDx-DR系统通过AI驱动实现了糖尿病视网膜病变的筛查,诊断准确性超过90%。皮肤科则利用AI通过智能手机应用程序对多种皮肤病变进行分类。心脏病学中,AI可以自动计算 “射血分数” (Ejection Fraction)、冠状动脉钙评分并通过超声心动图和CT评估 “心肌应变” (Myocardial Strain)。这些技术共同提升了诊断的敏感性和特异性,改善了患者的治疗效果。
研发客:除了上述领域,AI在基因组学和个性化医疗方面有什么贡献?
冯博士:
AI在基因组学中的应用正经历一场复兴。例如,DeepSEA、CADD和AlphaMissense这样的机器学习模型加速了致病变异的优先排序,加快了罕见病的诊断过程。AlphaMissense在预测错义变异致病性方面的准确率达到约90%,这在ClinVar分类中表现尤为突出。肿瘤学中,AI还用于评估肿瘤突变负荷和“微卫星不稳定性” (MSI),为免疫疗法的选择提供依据。药理基因组学创新则利用AI个体化调整药物剂量,比如华法林药物治疗。同时,单细胞RNA测序框架如scVI和SCALE揭示了细胞谱系、发育轨迹和调控网络结构,进一步推动了精准医疗的发展。这些进步使得我们不仅能更快找到病因,还能更精准地制定治疗方案,真正实现因人施治。
AI在医疗与制药领域的挑战及应对
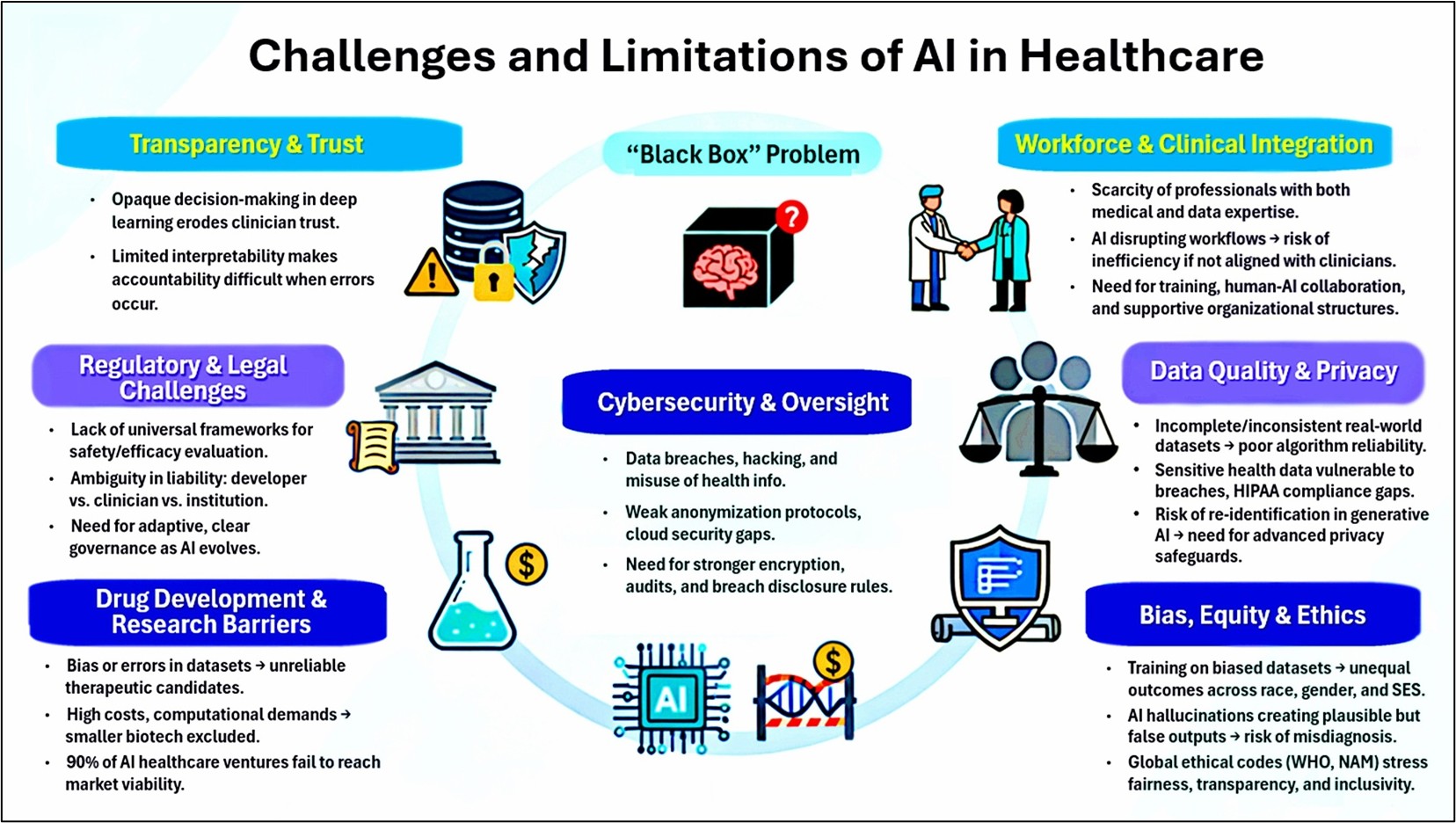
摘录自冯博士《医学评论》期刊的学术论文图二
研发客:AI在医疗中虽然前景广阔,但大家也常提到“黑箱”问题。这到底是什么意思?为什么它这么令人担忧?
冯博士:
所谓“黑箱”,就是指很多AI系统,尤其是深度学习模型,做出判断的过程完全不透明。医生和患者根本不知道它是基于什么逻辑得出结论的。比如一个AI说某位患者有90%概率患癌,但无法解释是哪张影像特征、哪项指标让它这么判断。这种不可解释性会削弱临床信任,一旦出错,责任也难以界定。正因如此,现在全球都在大力推动“可解释AI”(XAI),比如用SHAP、LIME等工具让模型“说出理由”,确保决策既智能又可信。
研发客:除了技术不透明,听说AI还可能“歧视”某些人群?这是真的吗?
冯博士:
非常真实,而且是个大问题。如果训练数据主要来自某一种族、性别或高收入群体,AI就可能在对其他人群的判断上表现不佳。2025年就有研究发现,某些AI辅助诊断工具对部分患者的肾功能评估系统性偏低,导致治疗延误。这类偏差不是算法“有意为之”,而是训练数据本身就有问题。因此,现在国际指南都强调:必须用多样化、有代表性的数据来训练AI模型,并在部署前后做公平性审计,否则AI的效果可能会大打折扣。
研发客:面对这些风险,监管机构和医院该怎么应对?有没有具体的解决路径?
冯博士:
有的,而且需要多管齐下。首先,建立严格的数据治理框架,确保数据高质量、去标识化、来源多元;其次,推行伦理审查机制,比如成立包含医生、数据科学家、伦理学家和患者代表的AI监督委员会;第三,强制要求开发者提交“可解释性报告”和“公平性评估”,就像药品要过临床试验一样。FDA、EMA现在都在试点这类制度。最关键的是,AI永远只能是“增强”人类判断的工具,最终决策权必须牢牢掌握在医生和监管机构手中。
研发客:人才短缺是不是也拖了AI落地的后腿?光有技术不够吧?
冯博士:
完全正确!目前最缺的就是“双栖人才”;既懂临床医学,又精通数据科学的人。很多医院买了先进AI系统,却没人才能调参、验证或融入内部的工作流。所以,未来医学院和计算机学院得联手培养复合型人才。同时,医院内部也要组建跨学科团队,包括临床医生、信息工程师、伦理顾问等,共同设计、测试和优化AI应用。否则,再好的技术也会“水土不服”,甚至打乱原有的诊疗节奏。
研发客:隐私泄露也是大家担心的重点。AI要用大量患者数据,怎么保证安全?
冯博士:
这是核心挑战。传统做法是把数据集中到一个平台训练模型,但这就成了黑客的“蜜罐”。现在新兴的联邦学习(Federated Learning)提供了一种新思路:数据留在本地医院,只共享模型参数更新。像NVIDIA Clara、Owkin这些平台就在这么做,既保护隐私,又能协作提升模型性能。此外,还得配合强加密、最小化数据采集、第三方安全审计,以及明确告知患者数据用途并获取知情同意,只有技术+制度双保险,才能重建信任。
AI在医疗制药领域的其他问题和未来方向
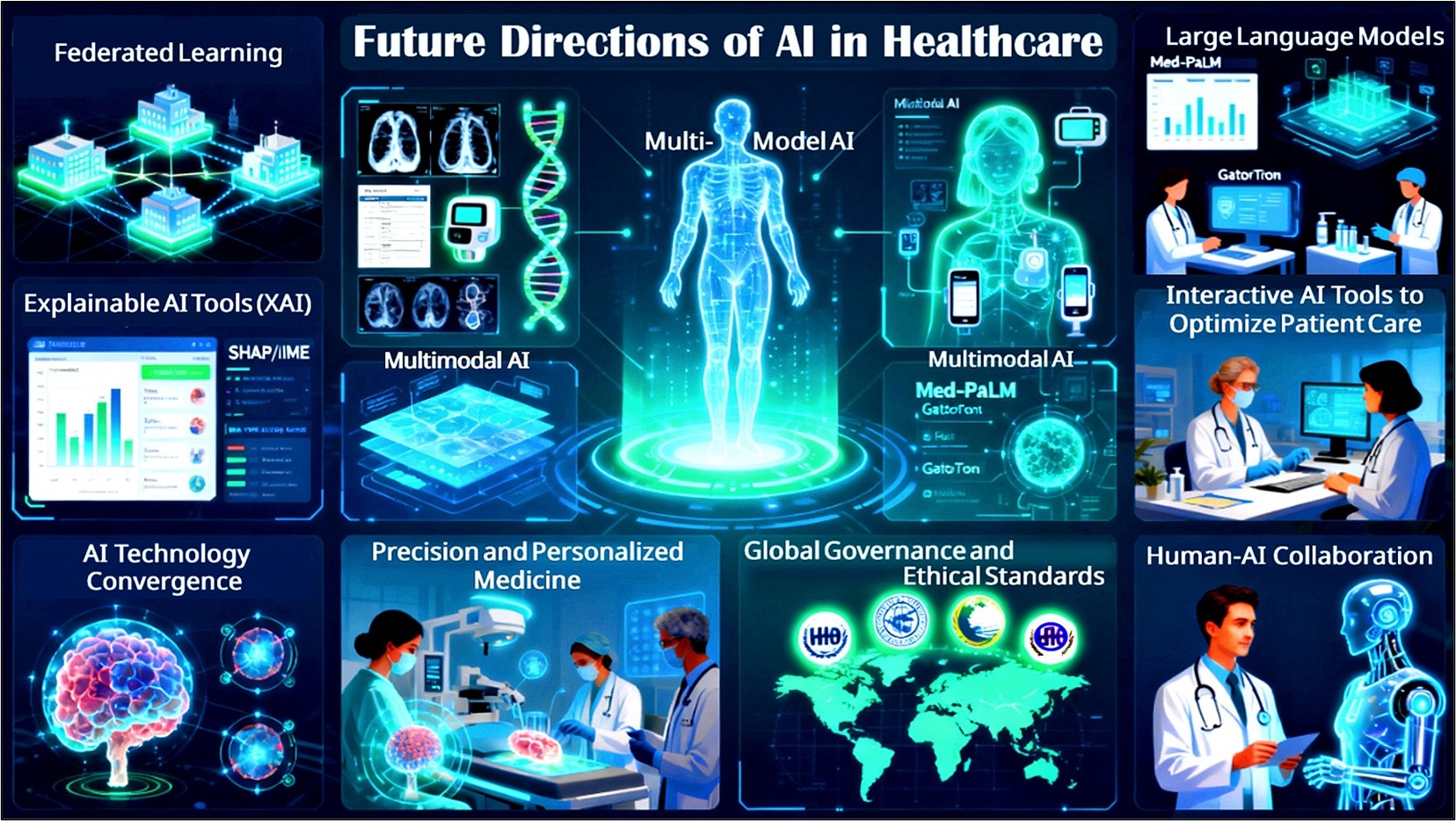
摘录自冯博士《医学评论》期刊的学术论文图四
研发客:既然AI这么强大,是不是意味着它很快就能取代医生?或者至少在某些领域“自主决策”?
冯博士:
我的观点很明确:AI是“增强智能”(Augmented Intelligence),不是“替代智能”。它擅长处理海量数据、发现隐藏模式,但医学和制药的核心始终是人。诊断需要结合患者的社会心理背景,治疗要考虑伦理、价值观和生活质量,这些都是AI算法无法完全捕捉的。更重要的是,目前很多AI模型还是“黑箱”作业,决策过程并不透明。如果出了问题,谁来负责——是医生、医院、AI供应商、或其它机构?所以,AI必须作为医生的“认知助手”,在人类监督下使用,而不是独立做临床决定。
研发客:听说很多AI医疗创业公司最后都失败了,为什么商业化这么难?
冯博士:
原因很复杂。首先是临床转化断层:实验室里准确率95%的模型,一到真实医疗和临床环境就“掉链子”,因为现实数据更杂乱、设备更老旧。其次是监管和支付机制滞后:即使AI通过审批,医保不一定买单,医院也不一定愿为未经长期验证的AI工具付费。再加上小公司缺乏资源做大规模前瞻性试验,导致90%的AI健康项目大多止步于原型阶段。破局关键在于:产学研医监多方共建生态;从研发初期就让临床和监管方参与,确保产品真正解决痛点、符合规范、能落地。
研发客:现在很多人都在谈论AIDD是否存在估值泡沫。您怎么看这个问题?
冯博士:
我认为与其说是“疯狂泡沫”,不如说这是一种理性的繁荣。每当一项伟大的技术刚刚兴起时,资本都会迅速涌入,带动估值上升和各种夸张的故事出现。这实际上是社会注意力和资源集中的一种表现。关键不在于有没有泡沫,而在于我们能否区分那些停留在PPT阶段的创新与真正能带来疗效突破的研究。真正的考验是看这些候选药物能否顺利进入临床试验,并且在临床试验时展示出可靠且可重复的数据。随着越来越多AIDD的药物进入II-III期临床,市场将会经历一个自然筛选的过程,那些无法解决实际问题如递送难题或未能发现全新靶点的公司将被淘汰,而经过临床验证的AI公司则会生存下来并在未来发展壮大。
另一方面,AI巨头与大药企的深度合作将是另一条极具前景的发展路径。一个极具代表性的案例,就是近日英伟达与礼来宣布携手成立一家专注于AIDD的合资企业。这一合作不仅标志着AI与医药两大领域的战略融合,更预示了AIDD未来演进的关键方向。这一模式若然成功,或将重塑整个制药行业的研发生态:未来领先的“AI原生制药公司”(AI-Native Pharma)很可能诞生于此类强强联合之中,真正实现“更快、更准、更省”的药物创新。
研发客:从长远来看,这种所谓的“泡沫”对整个行业有什么积极意义吗?
冯博士:
从长远角度讲,这种短期的过热和回调可以视为为真正创新预付的一笔学费。虽然短期内可能会有过度投资的情况,但这也加速了算力平台、数据基础设施以及实验自动化能力的发展,为下一代更加成熟的AIDD企业奠定了基础。评估是否存在泡沫的关键指标不应仅仅是看估值高低,而是要关注三个方面:第一,研发管线是否已经实质性地进入了临床阶段,尤其是到了II-III期;第二,在多个项目上是否反复证明了其“更快、更省、更准”的研发优势;第三,商业模式是否超越了简单的服务收费模式,转变为风险共担、收益共享的合作模式。对于投资者和业界来说,更重要的是识别那些将AI深度整合到药物研发全过程中的公司。从靶点发现到分子设计,再到合成路线优化、临床试验设计和患者分层。只有这样的“AI原生制药公司”才有可能穿越周期,成为改变行业的长期赢家。
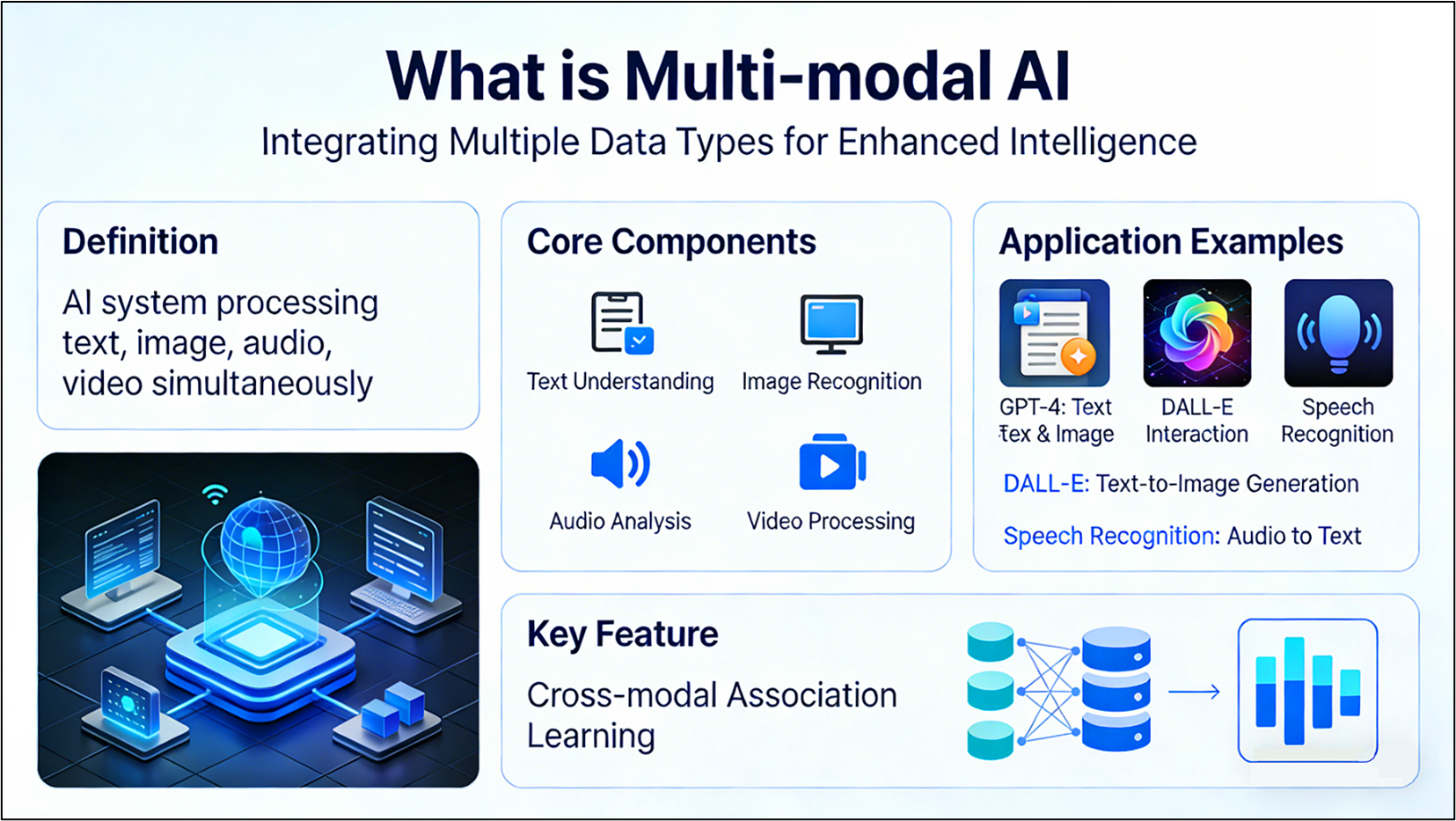
研发客:未来AI在医疗中最值得期待的新方向是什么?
冯博士:
我认为是多模态融合AI (Multi-Modal AI)。未来的系统不再只看CT片或只分析基因,而是把影像、电子病历、可穿戴设备数据、基因组、生活方式等全整合起来,构建每个人的“数字健康画像”。比如在癌症治疗中,AI可以同步分析肿瘤突变、免疫微环境、患者活动量和用药反应,动态推荐最优方案。大模型如Med-PaLM还能自动整理病历、生成随访建议,把医生从文书工作中解放出来。但前提是:数据要互通、算法要公平、使用要透明,否则精准医疗可能变成“精准偏见”。
研发客:冯博士,最后请您再重新展望一下:AI最终会如何重塑整个医疗体系?
冯博士:
我一直认为,AI不会取代医生、药企或其它医疗机构,但它将彻底改变“以疾病为中心”的旧模式,转向 “预测 - 预防 - 个性化 - 参与式”的新医疗范式。想象一下:你的智能手机若能提前一周预警你可能的心衰风险,AI帮你预约检查;就诊时,系统已整合你过去十年的健康数据,并给出定制方案;用药后,AI能持续监测治疗效果并调整剂量。而这一切背后,是联邦学习保障隐私、可解释模型赢得信任、全球标准确保公平。未来的医疗,将是人类智慧与机器智能深度协同的体系,它将使医疗变得更快、更准、更温暖,也更公平。但这需要我们今天就打好伦理、治理和人才的地基。未来已来,关键不在于我们是否相信AI,而在于今天如何负责任地构建它。