-
大中国区销售以固定汇率(CER)计算同比增长5%,主要由肥胖症治疗领域产品销售增长所驱动。
-
胰岛素产品销售以CER计算同比增长5%,主要由长效胰岛素驱动。
-
大中国区罕见病领域销售以CER计算同比增长84%,主要由罕见血液疾病领域销售增长所驱动。
-
诺泽优®在中国获批。中国国家药品监督管理局基于SELECT研究批准了诺和盈®的心血管适应症。诺和诺德已递交口服司美格鲁肽用于 2 型糖尿病患者的SOUL心血管结局试验数据,用于申请诺和忻®的说明书更新。
-
2025年12月31日,中国最高人民法院就司美格鲁肽化合物专利相关知识产权作出终审判决,支持北京知识产权法院关于维持司美格鲁肽化合物专利有效的判决。
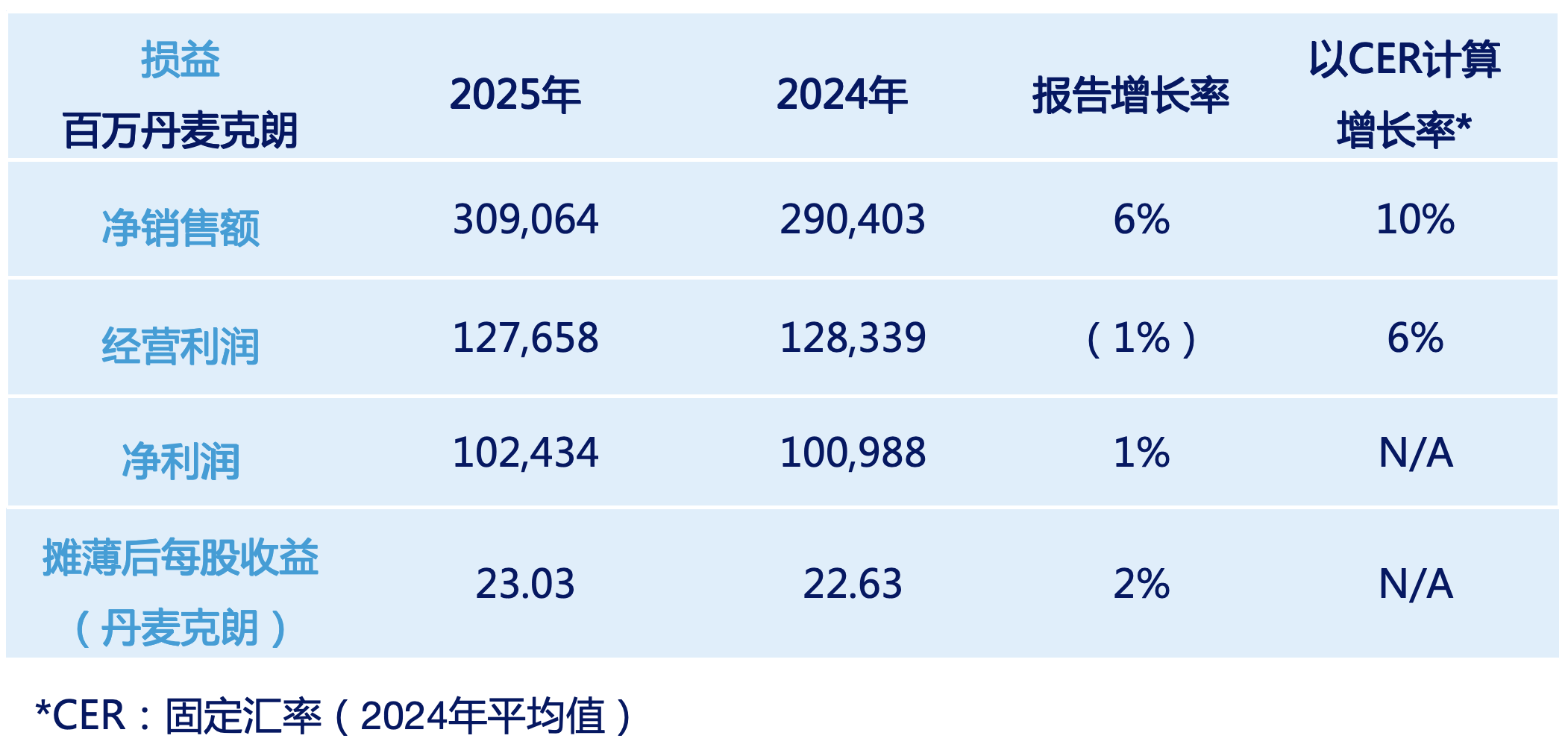
诺和诺德全球财报摘要
➤ 经营利润以丹麦克朗计算降低1%,以固定汇率(CER)计算增长6%,至1277亿丹麦克朗。若不计入约80亿丹麦克朗的公司转型相关成本,经营利润以丹麦克朗计算增长6%,以CER计算增长13%。
➤ 美国运营部销售以丹麦克朗计算增长3%(以CER计算增长8%),净销售额调整给美国区的销售带来积极影响。国际运营部销售以丹麦克朗计算增长10%(以CER计算增长14%)。肥胖症和糖尿病治疗领域销售以丹麦克朗计算增长7%,至2895亿丹麦克朗(以CER计算增长10%),增长主要由肥胖症治疗领域和GLP-1糖尿病治疗领域驱动,其中肥胖症治疗领域销售增长26%(以CER计算增长31%),GLP-1糖尿病治疗领域销售以丹麦克朗计算增长2%(以CER计算增长6%)。罕见病领域销售以丹麦克朗计算增长5%(以CER计算增长9%)。
➤ 12月22日,美国食品药品监督管理局(FDA)批准首个口服GLP-1药物用于肥胖症治疗:每日一次口服司美格鲁肽25 mg,其商品名为Wegovy® pill(Wegovy®片剂)。Wegovy®片剂已于2026年1月5日在美上市,截至1月23日,周处方量总计约达50000。处方量增长主要由自付渠道1.5 mg起始剂量所带动。
➤ 本季度重要的研发进展包括:zenagamtide(原amycretin)在2期临床试验中于2型糖尿病患者中显示出显著的降低体重效果及HbA1c降幅;同时,用于2型糖尿病的CagriSema 3期研究 REIMAGINE 2也已成功完成。在肥胖症领域,公司已向美国FDA递交司美格鲁肽7.2 mg及下一代产品CagriSema的注册申请。
➤ 若不计入340B准备金冲回影响,2026年调整后销售增长预计以固定汇率计算为-5%至-13%;以丹麦克朗计算的增长率预计将比以固定汇率计算的增长率低3个百分点。销售展望受到价格下降影响,其中包括美国“最惠国”(Most Favoured Nations)协议相关因素、司美格鲁肽分子在部分国际运营部(IO)市场的专利到期,以及市场竞争加剧等多重因素共同作用。预计全球GLP-1市场将持续扩容,随着诺和诺德推出包括Wegovy®片剂及更高剂量Wegovy®等新产品,公司有望进一步扩大患者覆盖范围并提升销量。调整后经营利润增速预计以固定汇率计算为-5%至-13%。以丹麦克朗计算的调整后经营利润增速预计将较固定汇率口径低5个百分点。此外,2026年的销售和营业利润将因美国340B药品定价计划相关准备金42亿美元冲回而获得积极影响。
➤ 在将于2026年3月26日召开的年度股东大会上,董事会将提议在2025年期末每股派息7.95丹麦克朗,使2025全年派息总额达到11.70丹麦克朗。董事会还决定启动一项高达150亿丹麦克朗的新股票回购计划。
诺和诺德全球总裁兼首席执行官(CEO)杜麦克(Mike Doustdar):“尽管2025年对公司来说充满挑战,诺和诺德仍实现了以固定汇率计算10%的销售增长,并将我们的创新治疗方案带给了近4,600万名患者。展望2026年,公司将在市场竞争加剧的环境下面临价格压力。然而,Wegovy®片剂在美国上市后的早期处方增长充满前景,令我们深受鼓舞,我们也对未来几年持续驱动销量增长保持信心。今年,我们同样期待多项新一代疗法的审批结果,包括用于血友病治疗的Mim8和用于肥胖症治疗的CagriSema,以及将陆续揭晓的多项令人振奋的研发数据,其中包括etavopivat和ziltivekimab的3期试验结果。”