苏州,中国——2026 年 2 月 27 日,信诺维医药宣布其自主研发的在研 1 类新药 EZH2 抑制剂——依格美妥司他(XNW5004)的最新临床数据在 2026 年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会(ASCO GU)上公布,彰显了信诺维在前列腺癌领域全球差异化竞争中的疗效优势。
摘要标题:A Phase 1b/2 study to evaluate the safety and efficacy of Igermetostat (XNW5004) in combination with Enzalutamide in patients with metastatic castration-resistant prostate cancer
摘要编号:169
展示形式:壁报
展示时间:2026年2月26日 11:30 AM - 12:45 PM(GMT-5)
依格美妥司他联合恩扎卢胺在既往接受过阿比特龙治疗的转移性去势抵抗性前列腺癌(mCRPC)治疗中展现出良好的疗效及安全性。
在本次公布的依格美妥司他联合恩扎卢胺治疗 mCRPC 的 Ib/II 期临床研究中,截至 2026 年 1 月 28 日,共入组 87 例既往接受过新型内分泌治疗的 mCRPC 患者,整体安全性和耐受性良好,无 DLT 事件发生,最终选择 Igermetostat 1200mg, BID 作为临床 II 期推荐剂量(RP2D)。
研究纳入 56 例既往接受过阿比特龙治疗的患者进行疗效分析,中位随访时间为 17.5 个月。疗效结果显示,整体阿比特龙治疗失败以及 1200mg 剂量组患者的中位影像学无进展生存期(mrPFS)均为 18.6m,mOS 均未达到(95% 置信区间:18.56 - 未达到)。在 1200mg 剂量下,12 个月 rPFS 率为 71.8%。在 16 例基线存在可测量病灶的患者中,最佳总体缓解率为 25.0%,其中包含 4 例部分缓解。35 例前列腺特异性抗原(PSA)可评估患者中,11 例(31.4%)达到 PSA 较基线下降 ≥50%。
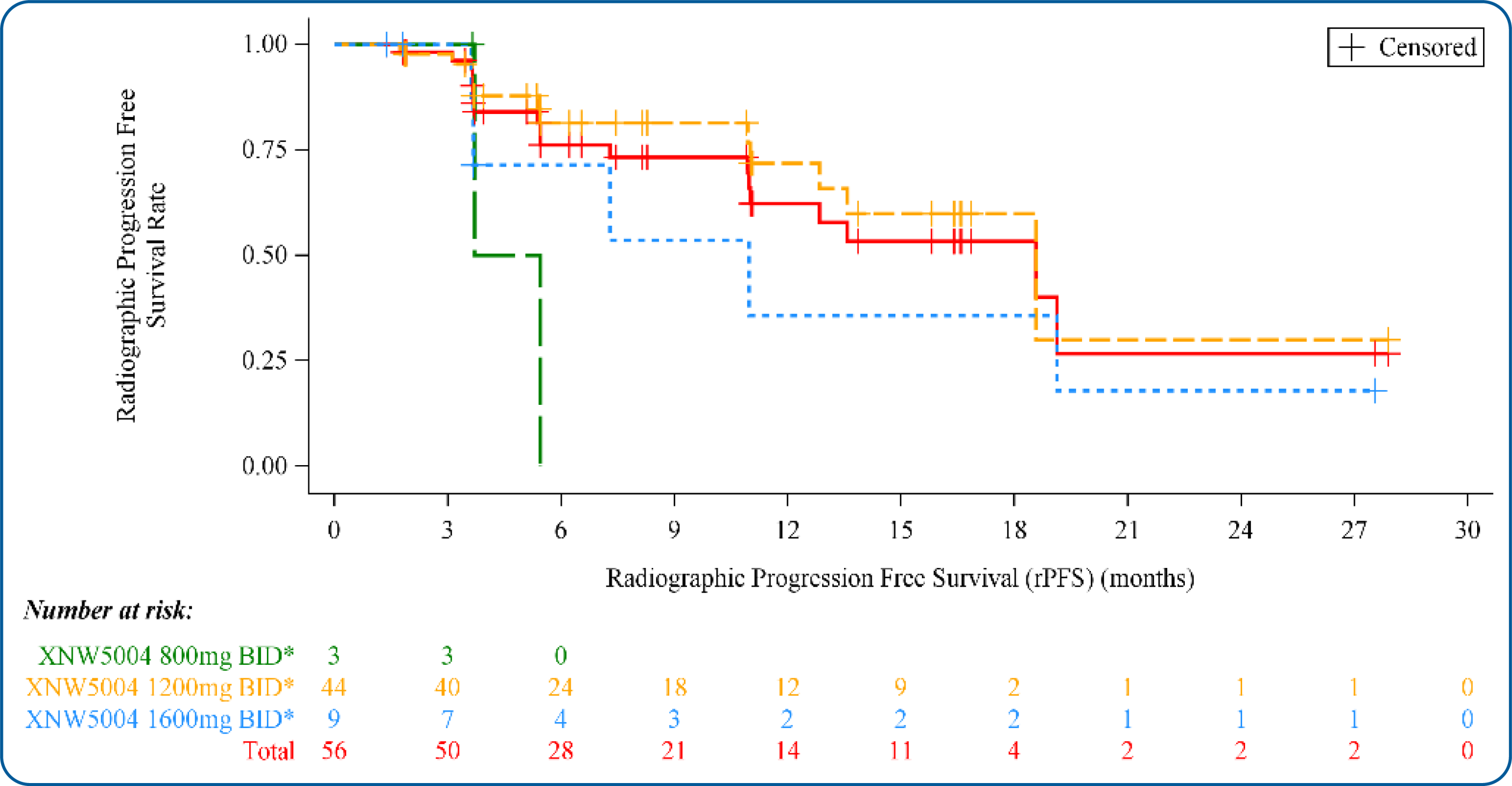
图1. 既往接受过阿比特龙治疗患者的影像学无疾病进展生存期(rPFS)
关于依格美妥司他(XNW5004)
依格美妥司他(XNW5004)是一款全球潜在疗效最佳、研发进度领先、针对表观遗传学靶点 EZH2 的小分子抑制剂,注册分类为化学药品 1 类。公司现阶段主要的适应症开发方向为外周T细胞淋巴瘤(PTCL)、滤泡性淋巴瘤(FL)及转移性去势抵抗性前列腺癌(mCRPC)。XNW5004 用于治疗“既往接受过二线系统治疗的 r/r PTCL” 以及 “既往接受过至少三线全身系统治疗的 r/r FL(EZH2 野生型)” 两项适应症均已被 CDE 纳入突破性治疗药物认定。截至本公告日期,公司已启动既往接受过二线系统治疗后 r/r PTCL、既往一线系统治疗后 r/r PTCL 和既往至少三线系统治疗后 r/r FL(EZH2 野生型)三项适应症的关键注册临床研究。
关于信诺维EVOPOINT
信诺维是一家以疾病为导向、聚焦于重大未满足临床需求的创新药公司。我们致力于将创新转化为临床价值,为全球患者提供疾病领域内最佳治疗方案。
基于“小分子靶向药物开发平台”、“复杂抗体药物开发平台(eMAB)”以及“靶向蛋白降解药物开发平台(eGLUE)”三大核心技术平台,信诺维在肿瘤精准治疗、多重耐药菌感染等市场空间广阔的重大疾病领域深度战略布局,现已有多款产品进入临床III期/ NDA阶段,并屡次获得国内外突破性治疗药物认定/快速通道认定。此外,凭借优秀的临床试验数据,信诺维已与多家国内外知名企业达成重要授权及合作协议,交易总金额超过20亿美元。我们正全力构建从药物发现、临床研发、生产制造到商业化等各环节的创新药全流程体系,瞄准全球化发展的路径,致力于成为国内一流,国际知名的创新药企业。