• 首款新药已获批,并收到默克1.55亿美元首付款;
• 匹米替尼第二项适应症GVHD的Ⅱ期临床基本完成;
• FGFR4选择性抑制剂针对晚期肝细胞癌临床试验有较大突破;
• 研发触角伸向自身免疫疾病、心血管疾病和肥胖,多个小分子项目快速推进,差异化优势明显;
• “市场波动不可避免。虽然股价现在还是低谷,但我们唯一能做的,就是把公司做好,把产品做好。”
在资本寒冬季里,故事总是相似的:管线停滞、资金见底、股价低迷、团队精简。财务赤字,成了大多数Biotech难以挣脱的枷锁。
同一片天空下,一家低调的中国公司,用了不到10年的时间,完成了一场近乎“教科书式”的精准突围:
首款best-in-class新药完成从临床前到获批的全流程,并成功将全球商业化重任交由制药巨头默克全权负责;靠BD连续两年扭亏为盈,产品进入商业化更是让持续盈利成为可能;身后还有10余个管线处于不同临床梯队,其中2款已分别进入NDA和注册性关键临床的新药……
港交所二级市场正在谱写这家小型Biotech的强势逆袭,两年时间里,其股价从最低点飙涨超4倍。
这张成绩单的缔造者,正是和誉医药。当部分同行还在为“活下去”苦苦挣扎时,和誉已悄然完成“研发-上市-商业化-盈利”的完整闭环,实现无数创业者梦寐以求的“自我造血”。它的快速成功,是偶然的幸运,还是一种可复制的、属于中国Biotech的新范式?
为了探寻答案,研发客前往位于上海张江药谷的和誉总部,拜访了这家公司的掌舵人——徐耀昌博士。
“过去近十年,国内生物医药行业变化很大,公司也经历很多起起伏伏,但我们追求best-in-class、first-in-class的理念一直没有变。我们坚信,把事情做好,把好的产品开发出来,后续的事情自然水到渠成。”在总裁办公室,这位一路引领企业发展的创始人一语道出和誉的生存密码。

和誉医药董事长兼CEO 徐耀昌博士
徐耀昌毕业于南京大学化学系,后取得芝加哥大学化学博士学位。他在肿瘤及其他疾病领域拥有30多年研发经历,曾促成礼来在华组建化学CRO公司,牵头筹建诺华中国研发中心,并助力豪森药业从仿制药向创新药转型。
启珂论坛本月开幕,请扫码报名及了解详情。

“要做全球新药,而不是光指中国”
回顾和誉首款新药匹米替尼(ABSK021)的开发历程,像极了这家Biotech厚积薄发的成长史。
该分子从2016年公司成立时就立项,直至2020年才获CDE批准进入临床。期间,和誉研发团队花了大量时间在化合物筛选和分子设计上,最终锁定一款口服生物利用度好、能穿透血脑屏障、兼具高选择性和高活性的CSF-1R抑制剂。
彼时,全球首款CSF-1R抑制剂已在美国获批,却因肝毒性问题被附上黑框警告,其他同靶点在研产品也大多存在选择性差、疗效有限等短板。
“要做全球层面都有价值的BIC、FIC新药,而不是光指中国。”徐耀昌早在十年前便敏锐意识到,创新唯有建立在全球坐标系上,才能走得更远。
因此,匹米替尼临床伊始便确定要走中、美、欧全球同步开发路线,并在众多潜在适应症中选择了腱鞘巨细胞瘤(TGCT)为首个适应症,区别于大多数CSF-1靶向药首选的渐冻症。
“我们也知道这个适应症并不像肥胖之类的拥有很大市场,却存在巨大未满足的临床需求。”徐耀昌说。
据介绍,TGCT虽不致死,但病人常年饱受疼痛和行动不便的困扰,中国每年新发患者约6万人,大多是中青年家庭支柱,给家庭带来沉重负担。传统手术治疗易复发,无法手术的患者则往往面临无药可用的困境。
“我们做任何事情的时候,都要把病人放在首位。”徐耀昌回忆,在匹米替尼开发期间,常有患者及家属来咨询“药物何时获批”“能否尽快用药”。这份迫切的期待让整个研发团队不敢有丝毫懈怠,直接推动药物研发驶入快车道:
-
2021年正式启动 Ⅰ 期国际多中心试验;
-
2022年获中国CDE批准进入关键 Ⅲ 期临床;
-
2023年先后获美国FDA和欧洲EMA批准进入 Ⅲ 期临床;
-
2024年超额完成国际多中心 Ⅲ 期临床全部患者入组给药;
-
2025年6月在中国申报上市,6个月后实现零发补批准;
-
2026年在美国申报上市并获FDA受理……
作为中国第一个自主研发并获批上市的CSF-1R抑制剂,以及中国首个TGCT药物,匹米替尼的到来填补了该领域的治疗空白。
根据和誉新闻稿,该药在所有TGCT系统性治疗的Ⅲ期研究中,实现了迄今基于RECIST v1.1标准评估的最高ORR(54.0%)。中位随访14.3个月时,研究初始即接受治疗的患者ORR提升至76.2%,其中4例实现完全缓解。
出色的疗效也为匹米替尼赢得了各种绿色通道,包括CDE突破性治疗品种和优先审评,FDA突破性疗法认定和快速通道资格,以及EMA优先药物资格(PRIME)和孤儿药资格。这进一步加速了这款BIC新药的全球开发进程。
“一家小公司,把一款对标全球的BIC新药,从早期一直推进到全球 Ⅲ期,最终在中国获批,甚至做到全球获批,这是开创性的。”徐耀昌言语中充满自豪,“匹米替尼的成功对公司而言意义非凡,表明我们具备了做创新药的能力,也让研发团队更加自信。”
“做交易不能追求眼前利益”
酒香不怕巷子深,匹米替尼便是如此。早在Ⅰ期临床结束后,该分子就吸引了许多药企的关注,其中不乏国内企业和MNC。
“那时候资本寒冬已经来了,我们尽管手上有资金,但如果要筹建生产和销售,这个投入是很大的,也会占用公司很多资源。通过合作方帮助生产销售,能够让我们把精力和资金都放在早期研发上,而这些正好是我们擅长的。”徐耀昌表示。
据悉,和誉曾在匹米替尼的BD谈判中拿下来自美国、法国和德国的三家国际公司的offer。但和誉考虑的不仅是offer的高低,还有合作方的全球销售能力。
“我们的创新药是全球的。我们希望只选择一家公司就能够把国内外的销售全部解决,这样可以尽量减少合作过程的精力损耗。”徐耀昌说。
在他眼里,BD交易绝非简单的卖产品:“有时候做交易不能追求眼前利益,而要看长远价值。”
最终,和誉精挑细选了海外渠道成熟、中国销售名列前茅的默克,并先后将匹米替尼在中国和全球的商业化权益授予对方。这笔交易也为和誉赢得了最多6.055亿美元的潜在款项及未来持续的销售提成。截至2025年底,该公司已收到1.55亿美元首付款。
拓展阅读
5亿首付!和誉医药与默克达成pimicotinib商业化独家许可协议
自2025年底产品获批后,默克一直在紧锣密鼓准备商业化事宜,涵盖生产、定价、市场推广、进院、进医保等。
徐耀昌透露:“他们正夜以继日地工作,相信很快就能把这个药给到病人使用。”
此外,和誉正与默克就匹米替尼的后续适应症开发展开交流。
CSF-1在许多肿瘤及炎症部位均有过表达,这让CSF-1R抑制剂拥有广泛的潜在适应症,如肌萎缩侧索硬化症(ALS)、特发性肺纤维化(IPF)、移植物抗宿主病(GVHD)、老年痴呆及多种实体瘤等。其中,匹米替尼第二项适应症GVHD的Ⅱ期临床已基本完成,数据“非常漂亮”。
“和誉对这个靶点的了解很多,但默克也有自己的考量。双方合作就像婚姻,需要共同商议一起开发哪些适应症,携手努力把产品经营好,这是一个长期的过程。”徐耀昌说。
站在今天回看这笔交易,他依旧坚信“当时的决定是对的”,“我们资金有限但却非常专注,将近20个早期项目的研发一点都没耽搁”。
下一个十年:突破边界再出发
匹米替尼获批,只是和誉发展的一个起点。对于即将开启的第二个十年,公司后续一系列具备全球竞争力的BIC、FIC产品管线,才是核心增长引擎。
其中,徐耀昌重点介绍了其FGFR管线。作为拥有全球FGFR管线最多的公司,和誉的泛FGFR抑制剂与靶向特定亚型的FGFR选择性抑制剂互为补充,可实现适应症全覆盖;针对FGFR4突变及1-3突变的新一代FGFR抑制剂,能为一代FGFR耐药患者提供序贯治疗方案,从而达到深度覆盖。
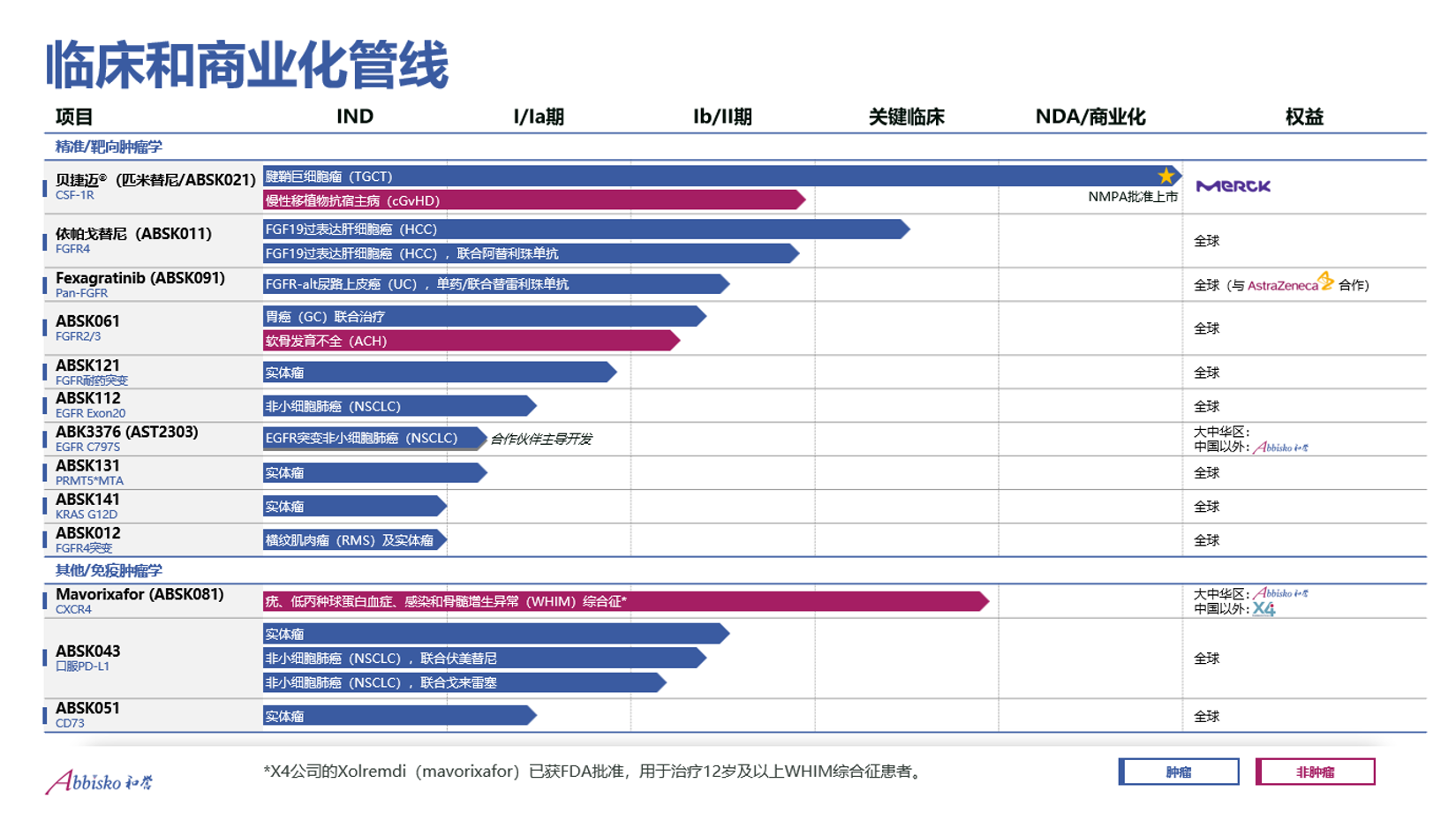
来源|和誉官网
“相比EGFR,FGFR是‘比较难啃的骨头’,包括诺华、阿斯利康等跨国药企在内,很多公司都曾尝试开发但并未成功,原因是FGFR家族的1、2、3、4四个亚型类同性极高,开发高选择性抑制剂的难度极大。”不过徐耀昌认为,越是难以突破的领域,一旦形成技术突破,越能构建难以撼动的竞争护城河。
这份差异化坚守已初见成效:和誉研发的FGFR4选择性抑制剂依帕戈替尼(ABSK011)在针对晚期肝细胞癌的临床试验中,单药ORR达到46.7%,联合PD-L1单抗阿替利珠单抗后ORR超50%。
“这对于肝癌来说是非常大的突破。”徐耀昌解释,之前诺华、incyte、blueprint等公司也曾开发FGFR4抑制剂用于肝癌治疗,但ORR往往局限在7%~16%之间,其他疗法单药或联用的应答率最多也只能做到20%多。
基于临床上优异的表现,ABSK011已获得CDE突破性疗法认定和FDA快速通道资格。目前该产品正在推进中国关键注册临床,预计2026年底完成病人入组,并有望在2027年申报上市。
“这款产品战略稍微不一样,我们采取‘中国优先’的策略。因为全球大约50%的肝癌患者在中国,政府也非常支持创新药。我们希望借助中国丰富的患者资源、更快的临床速度和药监局的加速审批通道,尽快解决国内巨大未被满足的临床需求。”他说。
另一款FGFR2/3双抑制剂ABSK061,则瞄准儿童软骨发育不全(ACH)及胃癌、膀胱癌、肺癌等实体瘤。
其中,ACH适应症开发已进入Ⅱ期关键阶段,预计今年下半年有数据读出,由于没有同类产品中常见的高磷血症副作用,该药有望成为全球BIC、中国FIC产品。实体瘤适应症上,首个适应症锁定亚洲高发的胃癌,数据显示其与PD-1和化疗联用效果显著。
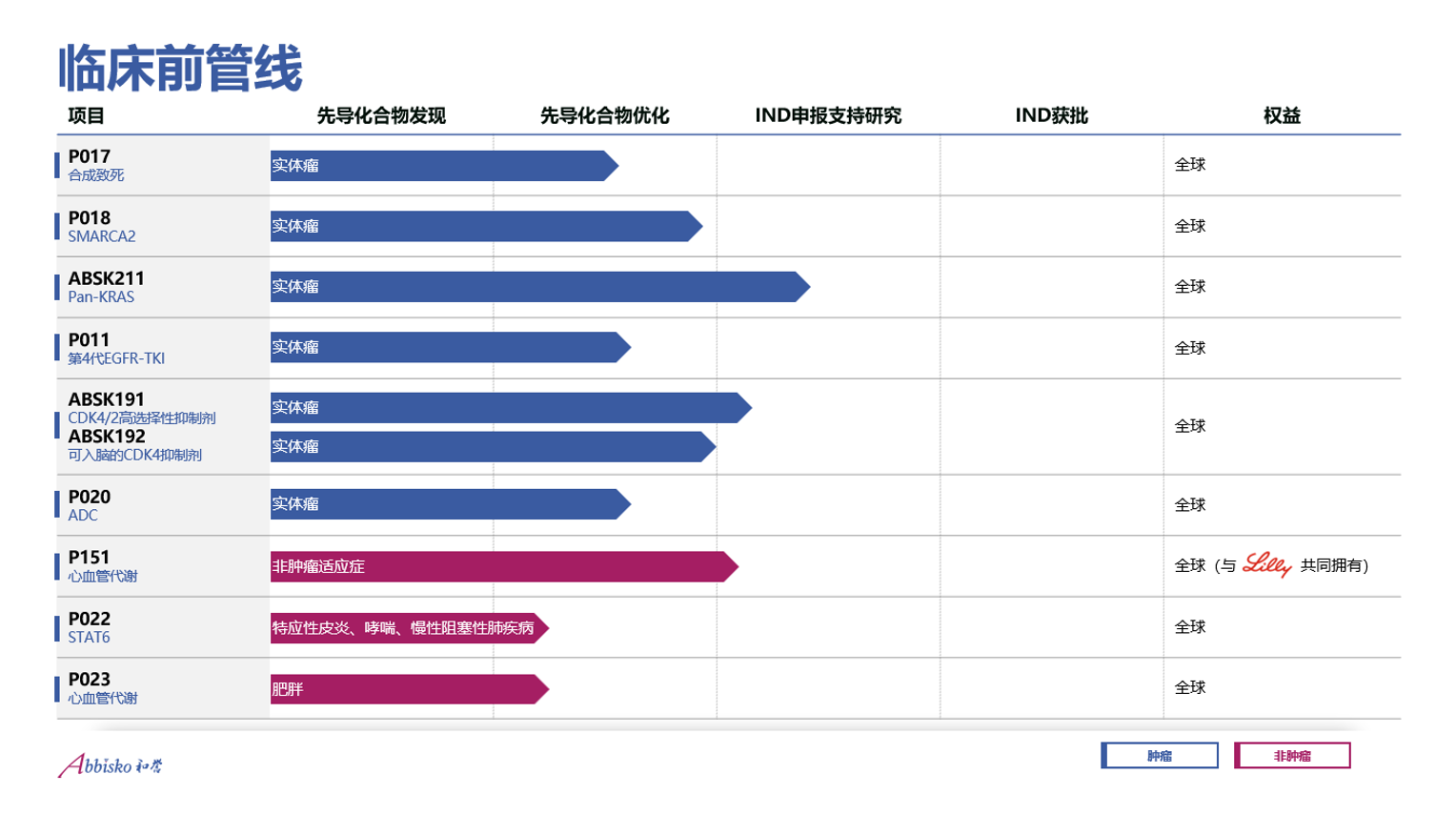
来源|和誉官网
值得关注的是,首款产品的获批让和誉研发团队信心大增,他们正突破原来只做肿瘤免疫和靶向药的边界,并尝试将研发触角伸向自身免疫疾病、心血管疾病和肥胖,目前多个小分子项目正在快速推进中,与当前主流的注射疗法相比差异化优势明显。
站在成立十周年的关键节点,徐耀昌总结了和誉穿越行业周期、实现稳健发展的关键,正是把产品做好的朴素理念——从靶点选择、早期研发,到临床前研究,再到全球临床Ⅰ、Ⅱ、Ⅲ期,直至最终获批与销售,公司一步一个脚印走完了这条最难走的路,实现了从研发到商业化的完整闭环。
“我一直跟团队强调,公司上市后大家关注股价是正常的,市场波动也不可避免。虽然股价现在还是低谷,但我们唯一能做的,就是把公司做好,把产品做好。”
他坚信,只要持之以恒把精力放在产品上,不断探索,不断创新,投资方迟早会看到和誉的潜力。
拓展阅读