2026年3月2日,艾伯维宣布其3期、随机、安慰剂对照、双盲AFFIRM研究取得了积极结果。该研究评估了risankizumab(SKYRIZI®)在中度至重度活动性克罗恩病成人患者中,皮下 (SC) 诱导治疗与安慰剂相比的疗效和安全性。
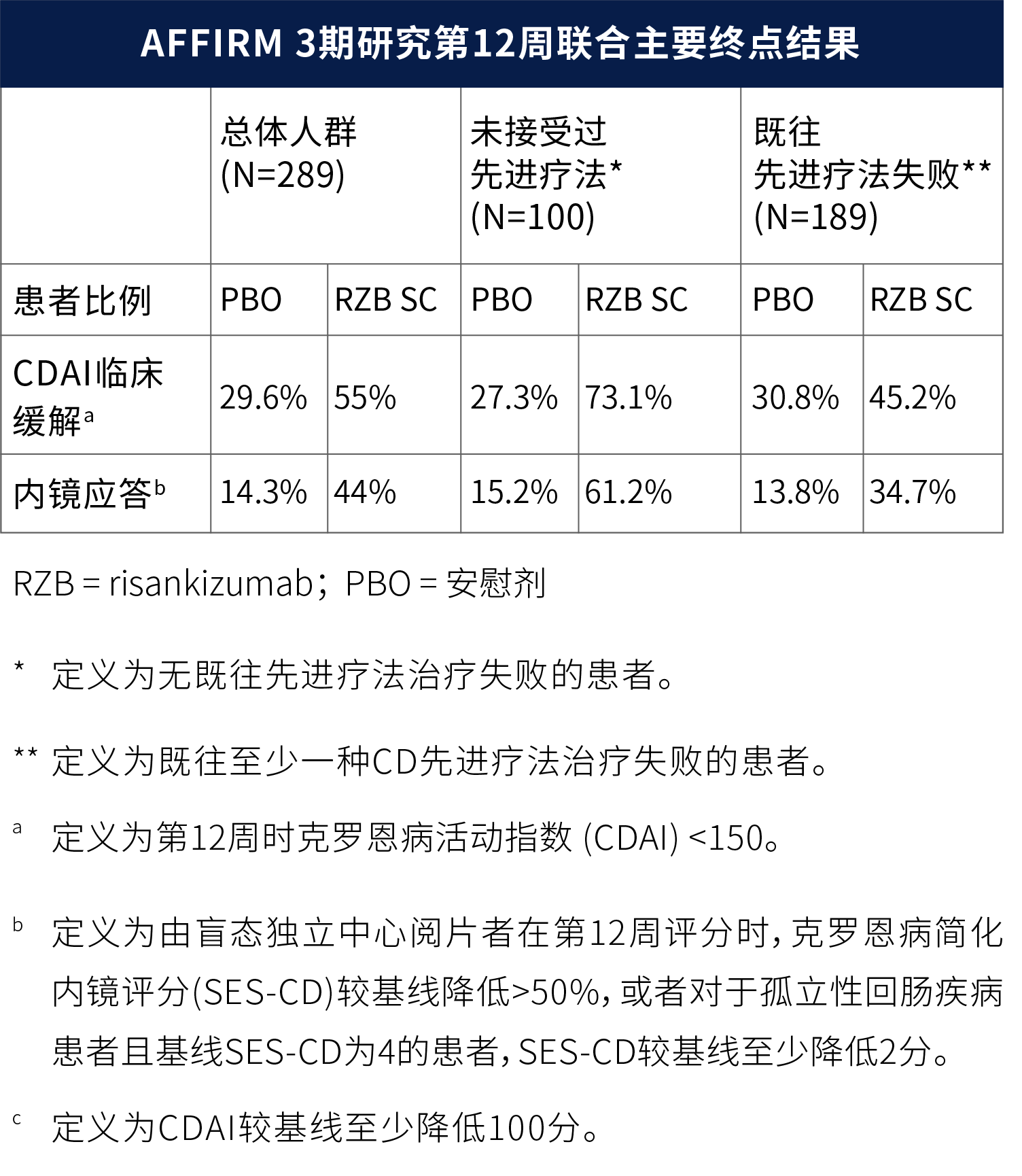
AFFIRM研究结果显示,与安慰剂组相比,risankizumab皮下诱导治疗在第12周达到联合主要终点——达成克罗恩病活动指数(CDAI) 临床缓解(55% vs.30%;p<0.0001)以及内镜应答(44% vs.14%;p<0.0001)的患者比例显著更高。在接受risankizumab皮下诱导治疗12周后获得临床缓解,继而接受12周维持治疗的患者中,67%的患者在第24周达到CDAI临床缓解,57%的患者在第24周达到内镜应答。
这项3期研究入组的患者主要为难治性人群**(65%),其中50%的患者既往使用两种或以上先进疗法治疗失败,23%的患者既往使用ustekinumab治疗失败,12%的患者既往使用Janus激酶抑制剂 (JAKi) 治疗失败。
艾伯维免疫学临床开发全球副总裁Kori Wallace博士:“本研究评估正对的是难治性克罗恩病患者人群,其中大多数患者是既往使用先进疗法后治疗失败的人群。这些数据进一步证实了risankizumab是这类患者领先的有效治疗选择。对于克罗恩病患者而言,达到如此水平的内镜应答是一项特别有意义的成果;而对艾伯维来说,这些结果突显了我们为提升治疗标准而持续进行的创新与研究。”
北卡罗来纳大学教堂山分校胃肠病学和肝病学系主任、公共卫生硕士、AFFIRM研究主要研究者Millie D. Long博士:“克罗恩病是一种复杂且常常令人身心俱疲的疾病。它不仅仅影响患者的消化系统健康,还会打乱患者的工作、人际关系和日常生活。这些在不同患者群体中取得的高内镜应答率,尤其是在那些既往无先进疗法治疗失败的患者中,展示了risankizumab皮下给药诱导治疗在克罗恩病中的有效潜力。”
在12周、双盲、安慰剂对照期间,risankizumab皮下给药的安全性特征与在克罗恩病中观察到的安全性特征一致,未观察到新的安全性风险。在接受risankizumab治疗的患者中观察到的最常见不良事件为上呼吸道感染、腹痛和关节痛。risankizumab皮下给药组0.5%的患者发生了严重不良事件,而安慰剂组为3.1%。
完整结果将在即将出版的医学期刊中发表,并在未来的医学大会上分享。
关于克罗恩病
克罗恩病是一种慢性、全身性疾病,表现为胃肠道内的炎症,最常见于小肠(回肠)和结肠之间的区域,导致持续性腹泻和腹痛。克罗恩病是一种进行性疾病,会随着时间的推移而恶化导致出现威胁生命的并发症或者需要手术。由于克罗恩病的体征和症状不可预测,它给患者带来了身体、情感及经济上的巨大的负担。
关于AFFIRM研究
AFFIRM是一项全球、3期、随机、安慰剂对照、双盲研究,旨在评价risankizumab皮下 (SC) 给药作为中度至重度活动性克罗恩病成人患者的诱导治疗的疗效和安全性。联合主要终点为第12周时达到CDAI临床缓解 (CDAI<150) 的受试者百分比以及达到内镜应答的受试者百分比。共有289例患者以2:1的比例随机接受risankizumab皮下给药或安慰剂治疗。risankizumab皮下给药组和安慰剂组之间的关键人口统计学和基线特征大致平衡;65%的受试者既往使用CD先进疗法后治疗失败。本研究包括3个治疗阶段:安慰剂对照阶段A(基线至第12周),旨在评价risankizumab皮下诱导治疗的疗效和安全性;扩展阶段B(第12-24周),患者根据其第12周的临床应答接受盲态或开放性治疗;52周开放性扩展阶段C,所有患者均接受获批的risankizumab维持治疗。关于本试验的更多信息,请参见www.clinicaltrials.gov(NCT06063967)。
声明:本文所列信息涉及尚未在中国获批的产品和适应症。本文章仅作信息分享用途,不应被理解为这些产品或适应症将在中国注册或获批。
关于艾伯维
艾伯维的使命是发现和提供创新药物,解决复杂且棘手的疾病难题和未来的医学挑战。我们不懈努力,凭借在多个关键治疗领域的科研创新为人们的生活带来深远影响,包括免疫学、肿瘤学、神经科学、眼科学、病毒学、胃肠病学,以及艾尔建美学产品组合中的产品和服务。
艾伯维在中国的总部位于上海,专注于在免疫学、肿瘤学、眼科学、麻醉学、神经科学和美学等领域为人们发展和提供创新的医疗方案。