-
在接受奥妥珠单抗联合标准疗法治疗的患者中,有超过四分之三实现了SRI-4应答,该指标用于评估疾病严重程度与症状。
-
奥妥珠单抗有望成为系统性红斑狼疮(SLE)新的标准治疗方案。
-
如获批,奥妥珠单抗将成为首款直接靶向B细胞的II型抗CD20单抗的系统性红斑狼疮治疗药物,B细胞是引发炎症和疾病活动的关键驱动因素[1]。
-
系统性红斑狼疮是一种可能危及生命的自身免疫性疾病,全球患者超过300万。
中国上海,2026年3月10日——罗氏制药宣布,佳罗华®(通用名:奥妥珠单抗)治疗成人系统性红斑狼疮(SLE)的III期ALLEGORY临床研究详细分析结果已发表于《新英格兰医学杂志》(NEJM)。该研究在主要终点上展现出具有统计学意义和临床价值的获益:奥妥珠单抗联合标准疗法治疗组中超过四分之三(76.7%)的患者,在治疗第52周时,实现系统性红斑狼疮应答指数4(SRI-4)应答,而安慰剂联合标准疗法组该比例为53.5%(校正差异23.1%,95% CI:12.5-33.6,p<0.001)。相关数据已于欧洲时间3月6日在第15届欧洲狼疮大会(SLEuro)上公布。
奥妥珠单抗在所有主要研究和次要研究终点均优于安慰剂。研究显示,以不列颠群岛狼疮评估组(BILAG)指数定义的首次疾病发作中位时间得到显著改善(奥妥珠单抗组尚未达到评估值,安慰剂组为52.3周,HR=0.58,95% CI:0.40-0.82,p=0.002);以狼疮缓解定义(DORIS)定义的疾病缓解率较安慰剂组提升超一倍(35.1% vs 13.8%,校正差异21.2%,95% CI:11.8-30.5)。
诺斯韦尔医疗系统风湿病科主任范斯坦医学研究所分子医学研究所教授Richard Furie博士:“奥妥珠单抗的ALLEGORY研究是近年来系统性红斑狼疮后期临床最具说服力的成功研究之一,为靶向B细胞治疗可显著降低疾病活动度提供了重要证据。通过该研究,我们看到奥妥珠单抗有望实现更强效、持久的疾病控制,同时减少患者对激素的依赖。这些获益对患者、医生和家属而言意义重大,也标志着狼疮这一自身免疫性疾病的治疗迈出了重要一步。”
罗氏首席医学官罗氏全球药品开发负责人Levi Garraway博士:“数十年来,系统性红斑狼疮患者一直面临疾病活动不可预测、治疗选择有限、长期承受激素副作用的困扰。ALLEGORY试验结果表明,奥妥珠单抗能为患者带来显著、具有临床意义且持久的疾病控制,这对预防重要器官发生致命性损伤至关重要。我们期待与全球卫生监管机构合作,尽快将这一具有变革性潜力的新疗法带给狼疮患者。”
罗氏正与包括美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)等在内的卫生监管机构沟通相关数据,力争让奥妥珠单抗这一有望成为狼疮新标准治疗方案的创新药物尽快惠及患者。若获批,奥妥珠单抗将有望成为首款直接靶向B细胞的II型抗CD20系统性红斑狼疮治疗药物。[2]
奥妥珠单抗的安全性与其已知的良好特征一致,未发现新的安全信号。研究达到了全部五项关键次要终点,包括52周时基于不列颠群岛狼疮评估组的复合狼疮评估(BICLA)应答,以及从第40周至52周持续将糖皮质激素剂量降至≤7.5毫克/天(泼尼松或等效剂量)。
所有关键及额外次要终点的研究结果见下表,这些终点是评估系统性红斑狼疮疾病控制效果的重要指标。
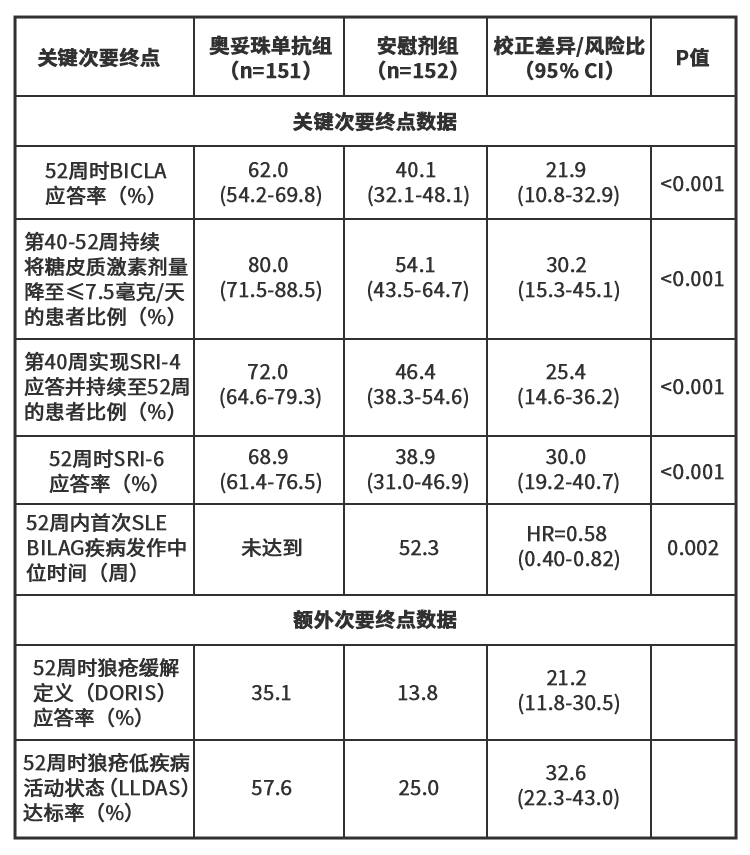
注:BICLA为不列颠群岛狼疮评估组复合狼疮评估;SRI-6为系统性红斑狼疮疾病活动评分6分改善;DORIS为狼疮缓解定义;LLDAS为狼疮低疾病活动状态。
系统性红斑狼疮全球患者超300万,患者多在15-45岁期间确诊,其中有色人种女性患病比例更高。[3-5]疾病的频繁急性发作会引发多器官炎症和不可逆损伤。约半数患者在确诊后5年内会进展为狼疮性肾炎——这是一种潜在致命的肾脏并发症。[6-8]实现更好的疾病控制能够减少疾病发作和器官进一步损伤的风险,并减少狼疮性肾炎的发生。[9,10]
ALLEGORY研究是奥妥珠单抗在免疫介导性疾病领域取得阳性结果的四项III期研究之一,其余三项分别为治疗狼疮性肾炎的REGENCY研究、原发性肾病综合征的INShore研究,以及原发性膜性肾病的MAJESTY研究。不断积累的证据证实,奥妥珠单抗有望用于控制多种免疫介导性疾病的疾病活动度。
基于REGENCY和NOBILITY研究数据,奥妥珠单抗已在美国和欧盟获批用于治疗成人活动性狼疮性肾炎,目前其治疗儿童和青少年狼疮性肾炎的全球II期研究也在开展中。[11,12]在中国,奥妥珠单抗已于今年2月被中国国家药品监督管理局纳入优先审评,用于治疗2岁及以上原发性肾病综合征。除奥妥珠单抗外,罗氏拥有丰富的研发管线,并致力于成为免疫学,尤其在免疫性肾病和风湿性疾病领域的领导者。
参考文献:
[1] Yap DYH, Chan TM. B Cell Abnormalities in Systemic Lupus Erythematosus and Lupus Nephritis-Role in Pathogenesis and Effect of Immunosuppressive Treatments. Int J Mol Sci. 2019 Dec 10;20(24):6231.
[2] Clinicaltrials.gov. A study to evaluate the efficacy and safety of obinutuzumab in participants with systemic lupus erythematosus (ALLEGORY). [Internet; cited 2026 February 11]. Available from: https://clinicaltrials.gov/study/NCT04963296.
[3] Tian J, et al. Global epidemiology of systemic lupus erythematosus: a comprehensive systematic analysis and modelling study. Ann Rheum Dis. 2023 Mar;82(3):351-56.
[4] Bindroo MA, et al. Late Onset Systemic Lupus Erythematosus - Clinical and Autoantibody Profile and its Comparison with Young Onset Systemic Lupus Erythematosus. Mediterr J Rheumatol. 2023 Jul 29;34(4):454–59
[5] Barber MRW, et al. The global epidemiology of SLE: narrowing the knowledge gaps. Rheumatology (Oxford). 2023 Mar 29;62(Suppl 1):i4-9
[6] Mahajan A, et al. Systemic lupus erythematosus, lupus nephritis and end-stage renal disease: a pragmatic review mapping disease severity and progression. Lupus. 2020 Sep;29(9):1011-20.
[7] Bechler KK, et al. Predicting patients who are likely to develop Lupus Nephritis of those newly diagnosed with Systemic Lupus Erythematosus. AMIA Annu Symp Proc. 2023 Apr 29:2022:221-30.
[8] Anders HJ et al. Lupus nephritis. Nat Rev Dis Primers. 2020 Jan 23;6(1):7.
[9] Kandane-Rathnayake R, et al. Association of Lupus Low Disease Activity State And Remission With Reduced Organ Damage And Flare in Systemic lupus erythematosus Patients With High Disease Activity. Rheumatology (Oxford). 2025 May 1;64(5):2741-48.
[10] Adamichou C, et al. Flares in systemic lupus erythematosus: diagnosis, risk factors and preventive strategies. Mediterr J Rheumatol. 2017 Mar 28;28(1):4-12.
[11] Furie RA, et al. B-cell depletion with obinutuzumab for the treatment of proliferative lupus nephritis: a randomised, double-blind, placebo-controlled trial. Ann Rheum Dis. 2022 Jan;81(1):100-07.
[12] Furie RA, et al. Efficacy and safety of obinutuzumab in active lupus nephritis. N Engl J Med. 2025 Feb;392:1471-83.