• BBB(血脑屏障)递送技术已成为MNC重塑CNS研发风险结构的关键:2025年相关交易额达93亿美元,占神经领域交易总额45%,递送技术从辅助工具升级为战略壁垒。
• TfR1已成为行业共识靶点,单价结合设计是成败关键。多个成熟递送平台均聚焦TfR1,单价结合策略可提高跨内皮转胞吞效率,减少受体交联、过强内吞后滞留、溶酶体分选、受体下调,罗氏研究显示单价TfR Fab较双价设计脑内结合能力提升55倍。
• 三大典型平台各具突破,覆盖抗体、siRNA等多元载荷。罗氏Trontinemab脑内暴露达前代12.4倍;BioArctic脑血比提升10倍;Arrowhead实现首个皮下给药CNS RNAi,mRNA敲低达65%~85%。
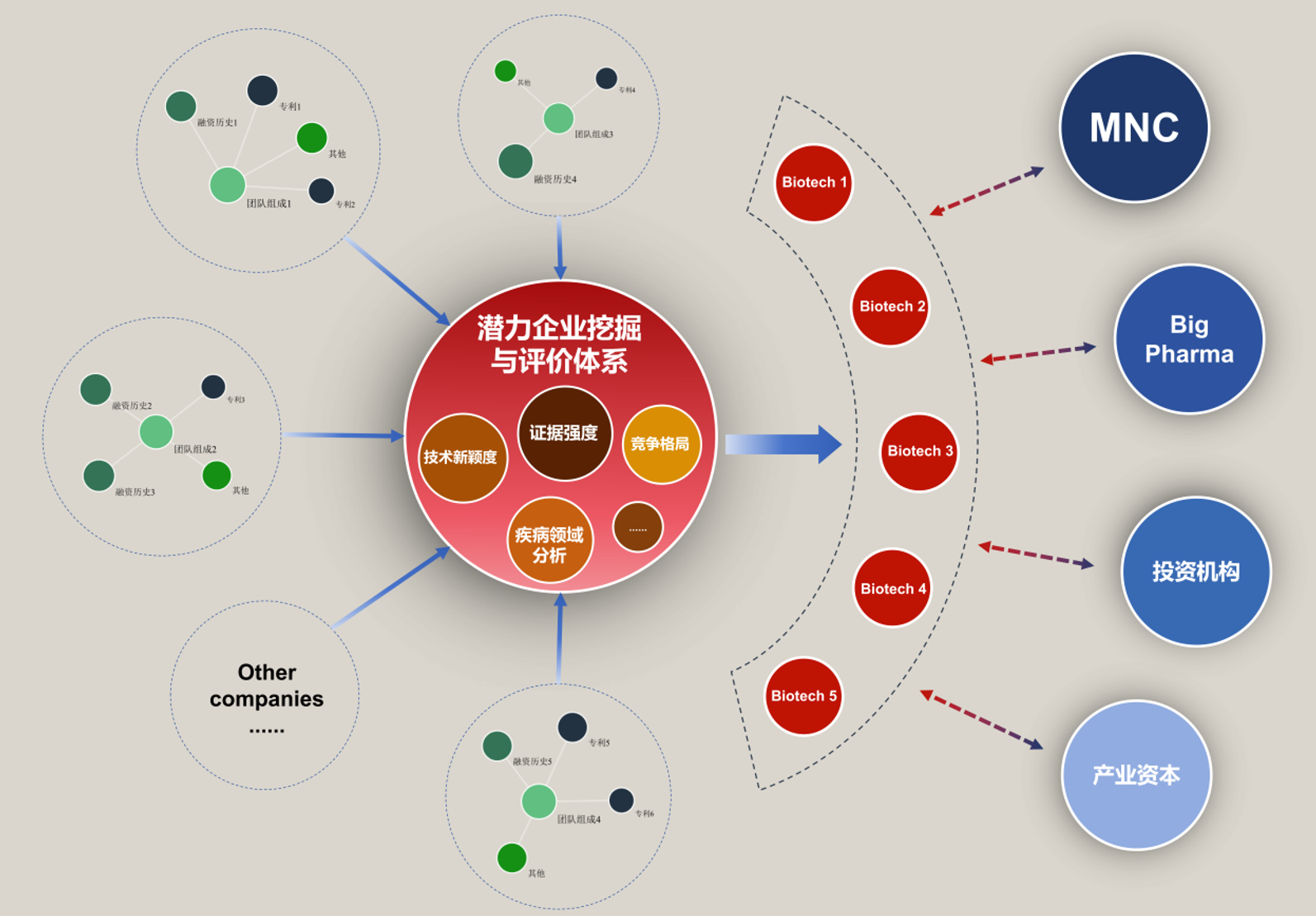
• 濠麦科技构建系统评估框架,赋能产业合作:通过对交易的15家平台技术解析,建立了五大维度CNS递送技术评估体系,通过濠麦科技建立的数据处理矩阵,进一步挖掘与筛选中国本土潜力平台。
撰文|濠麦科技技术挖掘与研判部
在全球医药产业格局中,CNS疾病长期被视为拥有极高未被满足临床需求和巨大市场潜力的战略赛道。然而,与其潜在商业价值形成鲜明对比的,是该领域研发所面临的高成本、高失败率及极长回报周期。历史数据显示,无论小分子还是大分子药物,CNS领域整体成功率均低于肿瘤、自免及代谢等领域,使其成为跨国药企研发组合中风险最高、确定性最低的赛道之一。
深入剖析失败经验可以发现,神经科学领域的高风险不仅源于靶点复杂性或疾病机制尚未阐明,更深层的结构性约束来自血脑屏障带来的递送瓶颈。BBB作为CNS长期演化形成的高度选择性生理屏障,极大限制了外周给药后药物进入脑实质的渗透效率与空间分布。大量临床失败案例表明,即便候选药物在体外和动物模型中验证了明确药理活性,在人体内仍可能因无法跨越BBB、或仅在脑脊液等“旁路空间”形成有限暴露,而难以在决定疾病进程的脑区和细胞类型中达到有效浓度。这一问题直接导致CNS药物研发中经典的“剂量—暴露—疗效”关系被系统性削弱,使临床研究结果高度不稳定且难以复制。
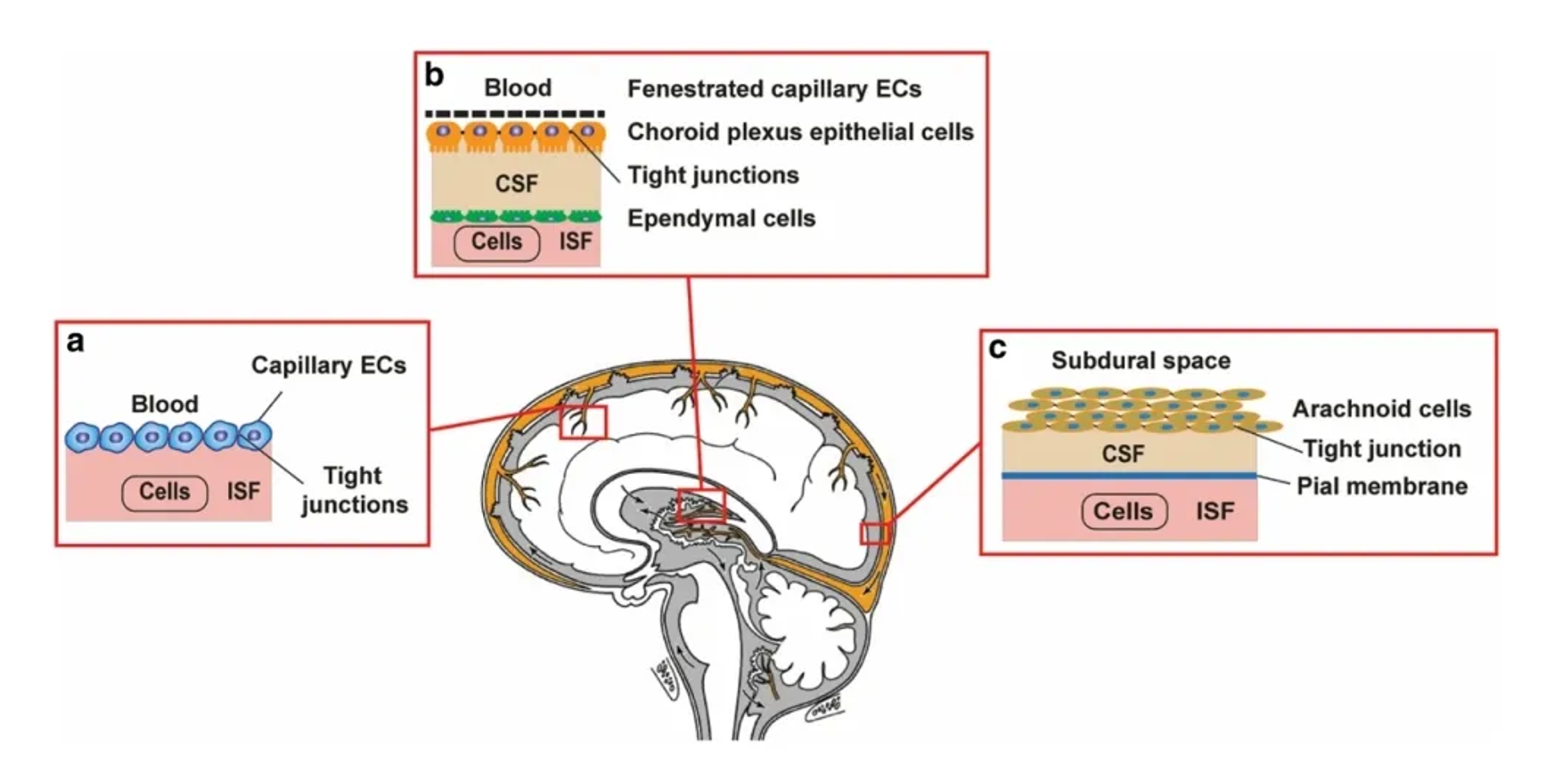
图1 血脑屏障的结构和功能
MNC战略分化,递送技术成为新壁垒
跨国制药公司对CNS领域的战略判断正加速分化。一方面,部分企业(如阿斯利康)经系统性评估后认为,在既有技术范式下,仅通过增加投入或扩大管线规模难以提升神经科学项目成功率,因而选择收缩布局,将有限资源重新配置至确定性更高的治疗领域。另一方面,另一些企业则形成共识:CNS研发的关键在于是否具备突破血脑屏障递送瓶颈的能力。在这一逻辑下,神经科学的竞争焦点已从靶点与分子本身,转向能够从根本上改变药物进入大脑方式的上游递送技术。
这一战略判断的变化,直接映射于近年来MNC在神经领域的投资与交易行为。相较于早期以单一候选分子为核心的引进模式,当前的资本运作更聚焦于具备平台属性、可跨适应症复用的CNS递送技术,尤其是围绕血脑屏障的受体介导转运、工程化抗体/融合蛋白及多模态递送解决方案。通过引入或内化此类平台,MNC试图从源头上重构CNS药物研发的风险结构,使靶点与机制的创新建立在更具确定性的递送基础之上。
递送技术成MNC神经领域并购标的
2025年,跨国药企在神经领域发起多起交易与并购,血脑屏障递送技术成为核心标的。已披露交易总价值达326.76亿美元,其中最大一笔为诺华以120亿美元收购Avidity。在剩余206.76亿美元中,以BBB递送技术平台为核心的交易额达93亿美元,占比约45%,涉及诺华、礼来、罗氏及葛兰素史克。
值得关注的是,诺华收购Avidity的核心资产为其抗体寡核苷酸偶联物平台,该平台主攻肌肉递送,但其递送靶点转铁蛋白受体1,恰与当前最热门的脑部递送靶点高度一致。
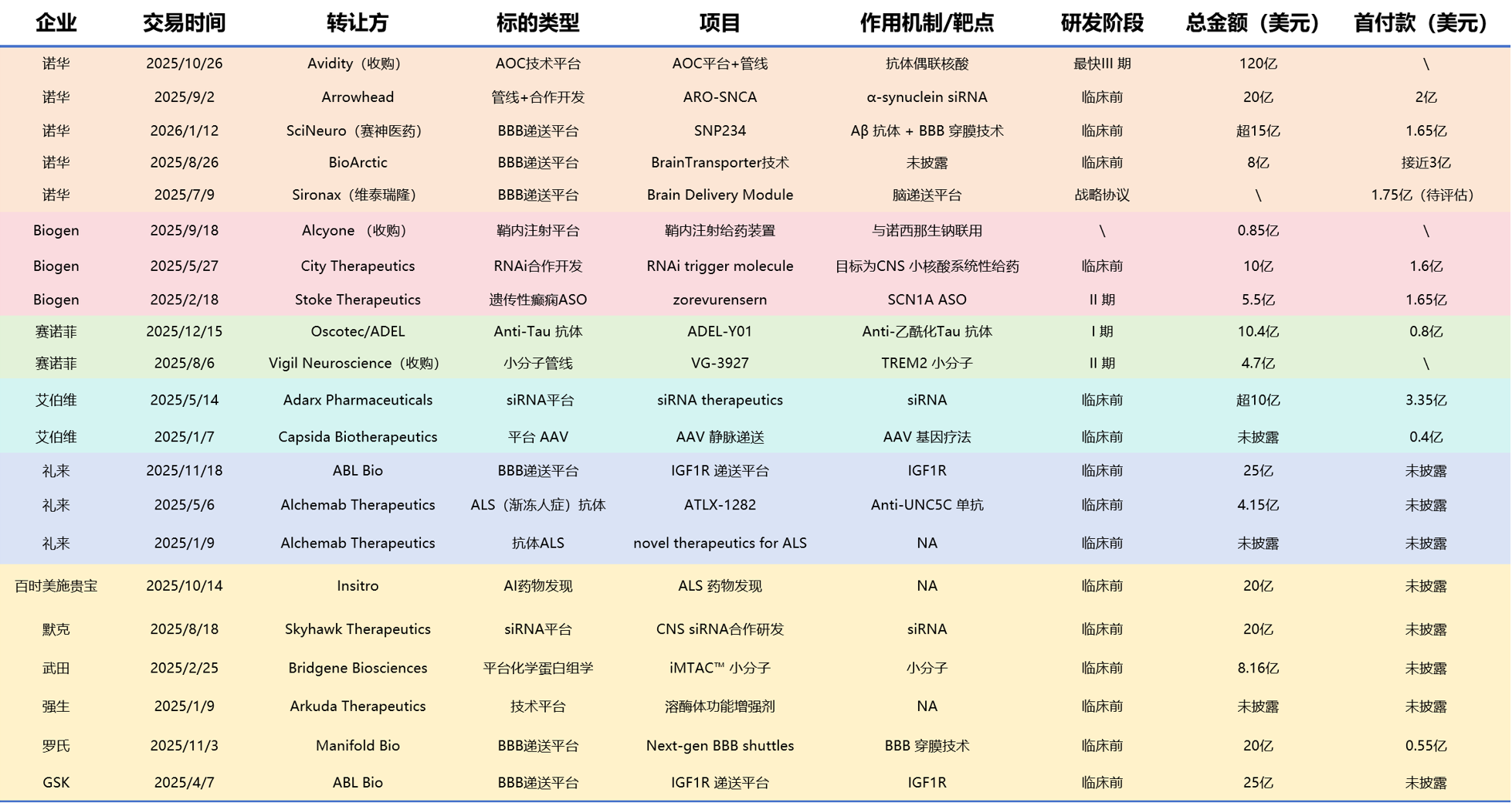
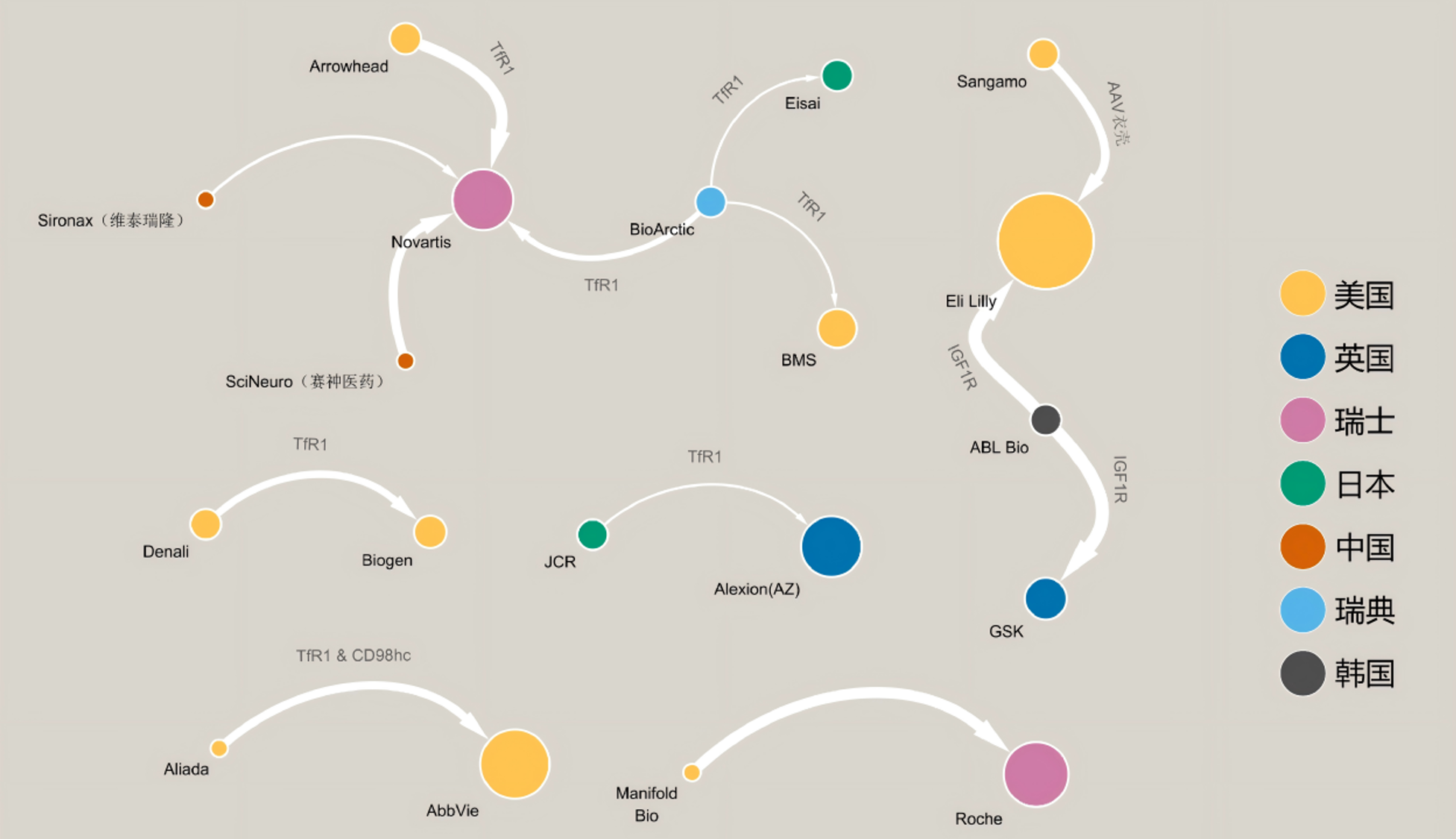
跨国公司BBB递送技术交易网络图
上图呈现了跨国公司在血脑屏障递送技术领域的交易网络格局。图中节点颜色代表公司所属国家,节点大小反映公司市值;箭头方向指示技术/资产交易流向,连线粗细对应交易总金额,连线标注显示相关转运靶点。Sironax、SciNeuro、Aliada及Manifold Bio为未上市公司。BioArctic–Eisai、BioArctic–BMS及Alexion–JCR三项交易的金额未公开披露。
聚焦跨国药企的血脑屏障递送技术及管线布局,转铁蛋白受体1已成为行业共识性靶点。除罗氏自主研发的Brainshuttle技术外,多家MNC均通过与外部公司合作引入递送平台,靶点涵盖TfR1、CD98hc、IGF1R等。此外,AAV衣壳技术也被用于递送非抗体类药物至脑部,进一步丰富了跨BBB递送的技术路径。(见下图)
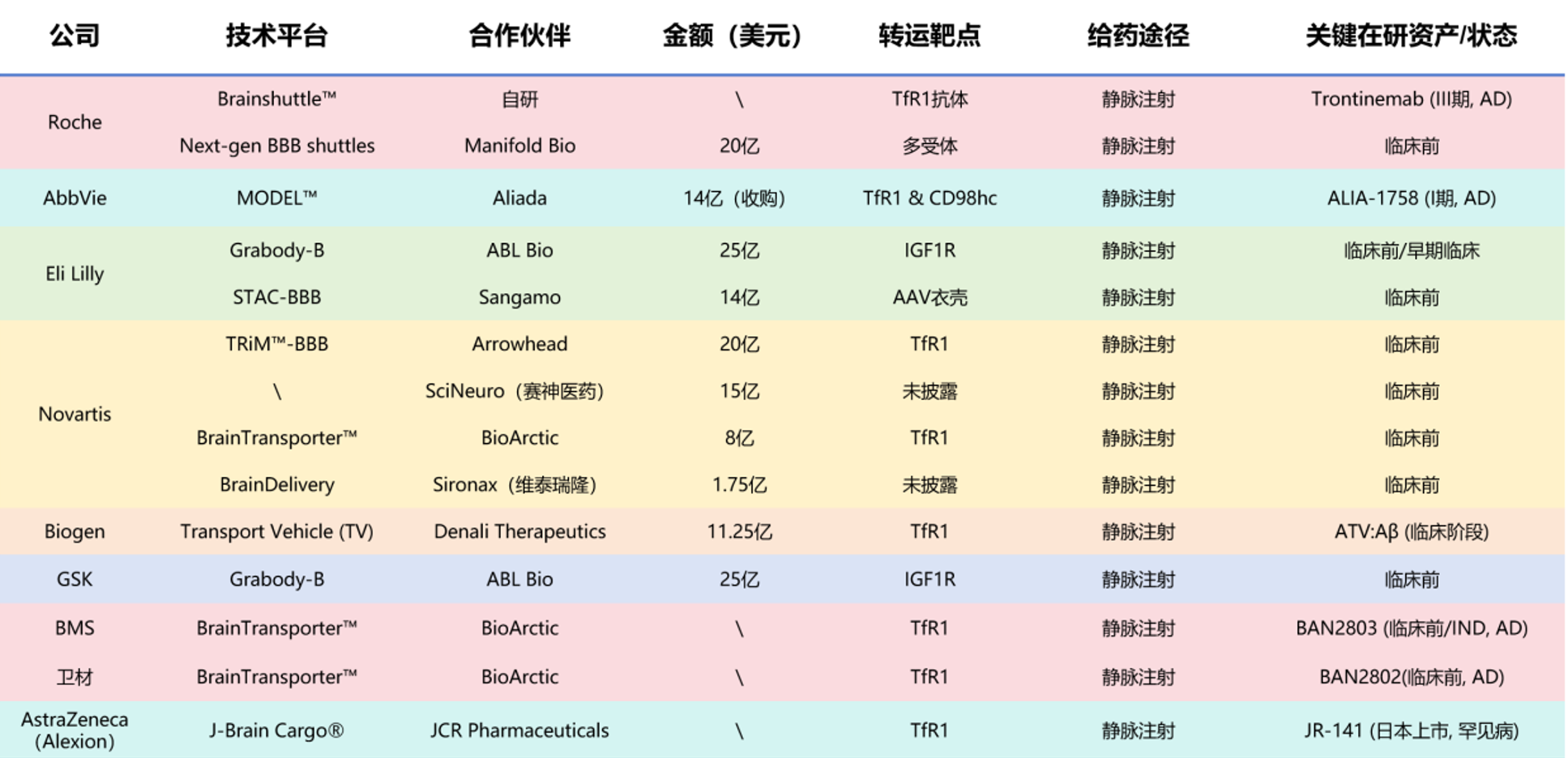
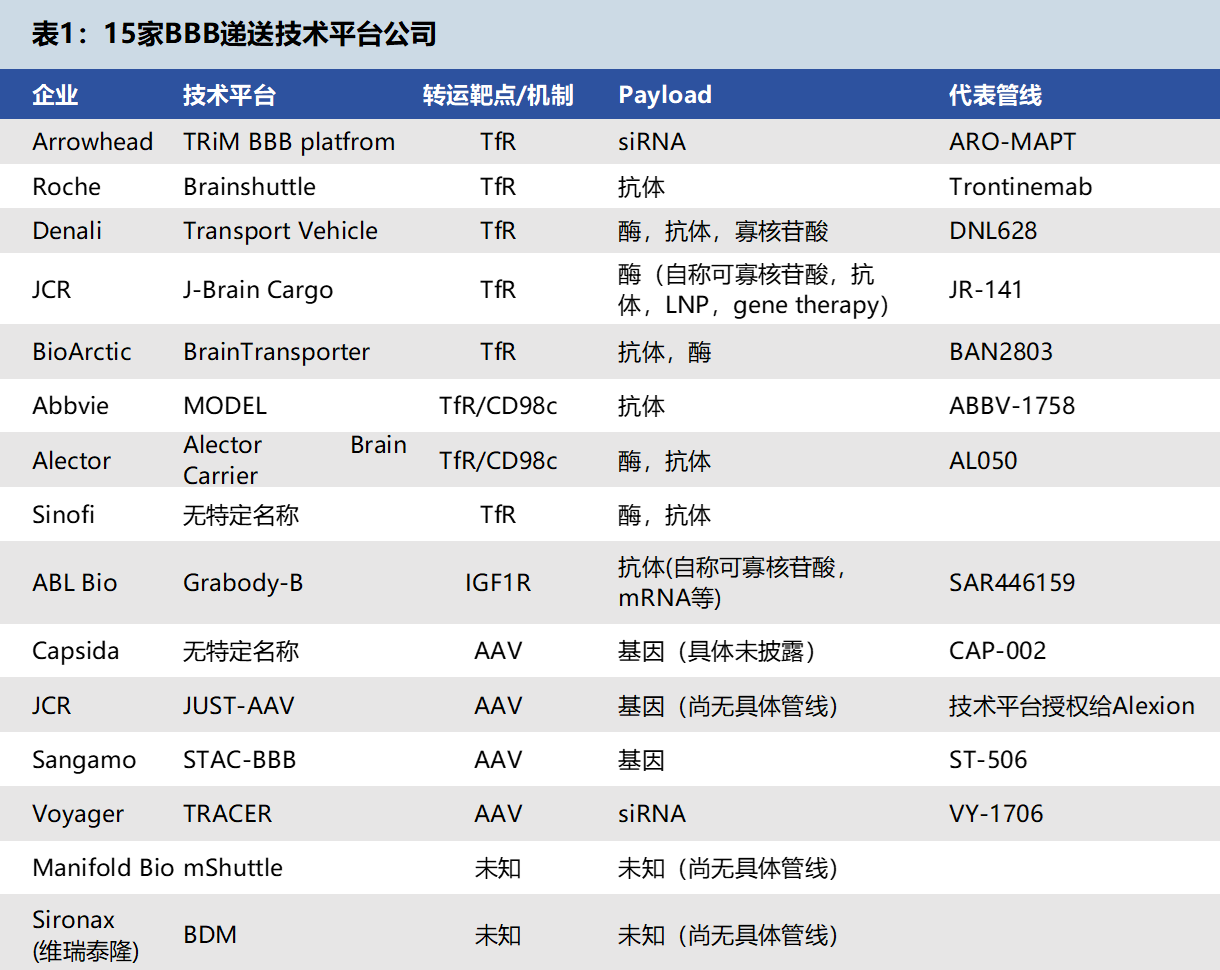
基于上述趋势,濠麦科技技术平台组对BBB递送技术领域开展了系统调研,涵盖15家企业。表1汇总了各企业的技术内容、技术类型及代表管线等信息。下文将重点解读其中三个典型技术平台:罗氏Brainshuttle、BioArctic BrainTransporter及Arrowhead TRiM™-BBB。
案例一
罗氏Brainshuttle™技术
罗氏Brainshuttle是基于受体介导转运的血脑屏障递送平台。其核心设计是在治疗性抗体/蛋白上引入可结合脑微血管内皮细胞受体TfR1的“穿梭模块”,使药物先在血管内皮侧结合受体、经内吞跨细胞转运,最终在脑实质侧释放,从而提升大分子药物的脑内暴露水平。
该平台的作用机制可概括为“两段式”递送:(1)递送段:通过TfR1触发跨BBB转胞吞作用,提高药物在脑组织及间质液中的有效浓度与分布范围;(2)作用段:进入脑内后,治疗分子按其本体机制发挥药效(如抗Aβ抗体促进斑块清除、抗tau抗体阻断病理传播)。Brainshuttle本身不具治疗功能,而是通过突破BBB限制,将生物制剂的脑内药效“释放出来”。
Trontinemab(RG6102)是基于Brainshuttle平台开发的阿尔茨海默病在研抗体药物。该分子采用“2+1”双特异性设计:两价结构靶向聚集态Aβ/淀粉样斑块,一价结构结合TfR1介导跨BBB转运,旨在以较低外周剂量实现更快、更充分的脑内斑块清除。
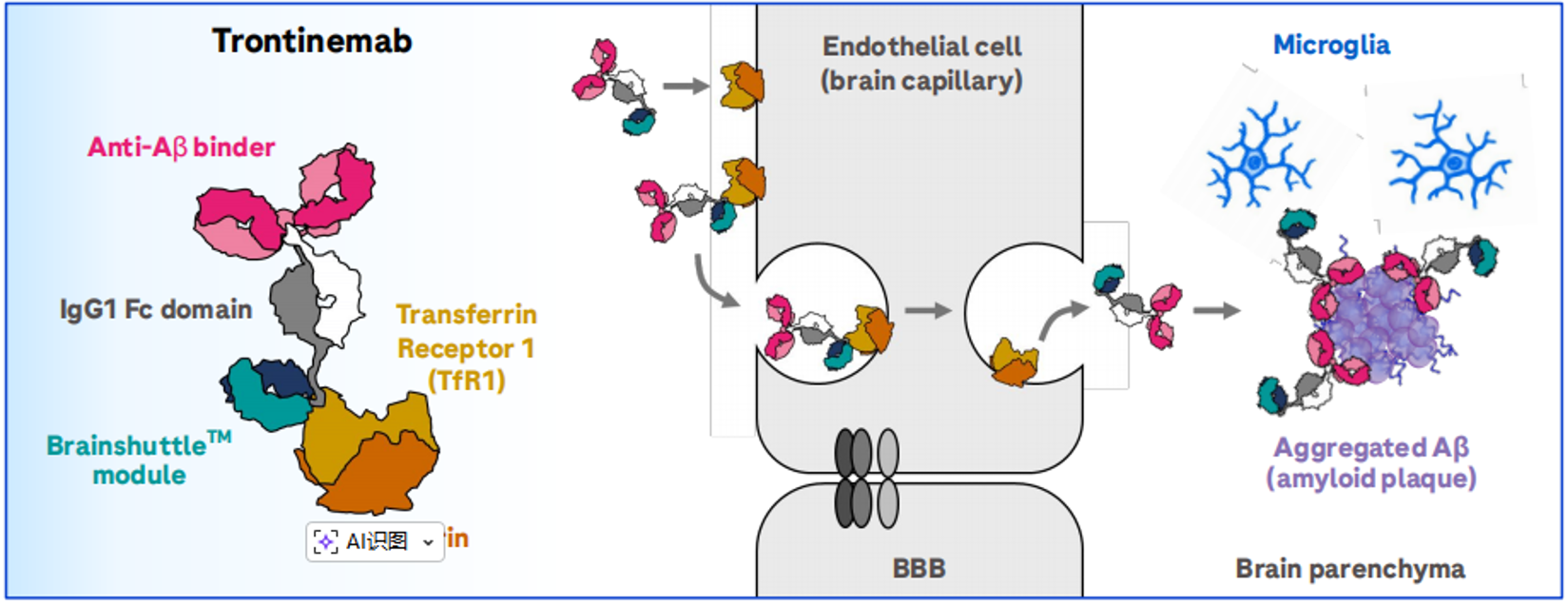
图2 Trontinemab作用机制图
Trontinemab的研发历程与另一款药物Gantenerumab的失败紧密交织,正是后者积累的教训,促使罗氏早在2014年便前瞻性启动了针对血脑屏障递送技术的系统研发。以下梳理了其中最为关键的九个时间节点。
2014年1月,罗氏/基因泰克团队在《神经元》期刊首次提出Brainshuttle技术概念,核心思路是利用转铁蛋白受体1介导的跨BBB转运提升抗体入脑效率,通过精细调控TfR1的结合方式与价态,在实现更高脑暴露的同时维持外周安全性窗口。
2017年,前代药物Gantenerumab在SCarlet RoAD III期研究中遭遇关键挫折,结果显示在当时剂量与方案下临床获益不足。这一失败为罗氏后续策略形成巨大压力,迫使其寻求更高效的淀粉样蛋白清除能力与更优的暴露-安全平衡。
2018年,《细胞报告》发表研究,系统讨论了Brain Shuttle-mAb架构设计与Fc功能、安全性相关的工程要点,这些讨论与后续Trontinemab的“2+1”双特异性架构设计、降低外周负担及潜在风险的策略直接衔接。
2019年至2020年,Trontinemab启动首次人体试验,在健康志愿者中开展单次递增剂量研究,用以评估早期药代动力学、耐受性及入脑相关指标。
2021年3月,在AD/PD大会上,罗氏首次集中披露Trontinemab的早期人体及转化数据,展示血浆与脑脊液暴露关系,强化“入脑增强”的证据链,标志着该分子从技术概念进入临床可验证的公开叙事阶段。
2022年11月,Gantenerumab遭遇最关键失败,其GRADUATE I/II两项III期研究均未达到主要终点,即便淀粉样蛋白负荷有所下降。这一节点实质上将罗氏研发重心进一步推向“更强入脑效率、更好安全性窗口”的新一代方案。
2023年,Trontinemab的关键转化及临床前证据体系逐步成型,在非人灵长类模型中的入脑数据及暴露-效应外推框架公开发表,为剂量选择与临床策略提供了可引用的科学依据,强化了“同类抗Aβ机制下,通过BBB穿梭提升中枢有效暴露”的论证逻辑。
2024年3月,AD/PD大会上,罗氏公布Trontinemab的期中研究结果,显示在低系统剂量下实现快速、剂量依赖的淀粉样斑块清除,PET影像学指标改善,同时公开讨论其安全性特征,尤其是ARIA发生率,构成该分子的差异化核心卖点。
2025年7月,阿尔茨海默病协会国际会议上,罗氏宣布Trontinemab的TRONTIER研究推进至III期并披露关键摘要指标,较高比例患者达到“淀粉样PET阴性”等具有传播力的结果,同时强调较低的ARIA-E发生率,标志着该分子正式进入决定性注册性开发阶段。
•TfR单价结合设计:实现高效BBB穿透的关键
抗体穿越血脑屏障需要经历多步骤过程:首先被脑微血管内皮细胞表面受体捕获并内化,随后需逃逸溶酶体降解途径,最终跨内皮细胞膜释放至脑实质。因此,抗体与受体的结合亲和力成为决定性因素,亲和力过弱(如无递送设计的裸抗体)无法有效进入内皮细胞;亲和力过强则难以从内皮细胞中逃逸进入脑实质。
为优化这一平衡,罗氏构建了三种抗Aβ抗体分子进行系统比较:裸抗体mAb31(Gantenerumab母体抗体)、双价TfR结合抗体(dFab)及单价TfR结合抗体(sFab)。研究结果显示,dFab因双价结合导致TfR受体交联,优先进入溶酶体降解途径,TfR被大量消耗,难以实现跨内皮细胞转运;裸抗体几乎无法通过内皮细胞进入脑组织;而仅与TfR单价结合的sFab则展现出最优的跨BBB穿透能力。
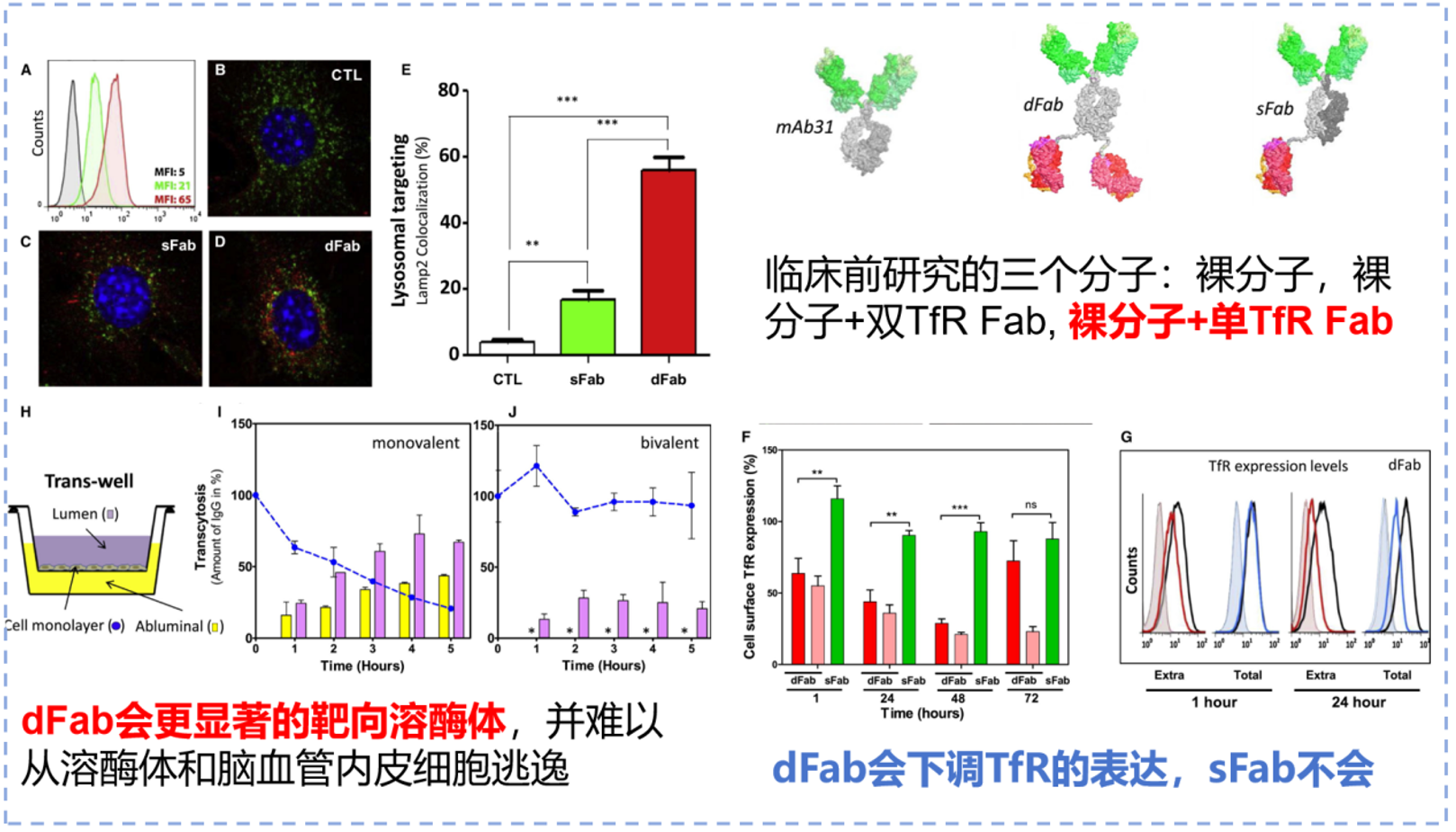
图3
• 单TfR Fab实现高效斑块结合并降低负荷
罗氏从两方面评估了单TfR1 Fab的体内药效:脑内Aβ结合能力及斑块负荷影响。结果显示,等摩尔剂量下,sFab较dFab和裸抗体的结合能力提升55倍;即使在治疗剂量(低剂量sFab)下,其结合能力仍可实现3倍提升。后续皮质及海马体分析证实,sFab能有效降低斑块负荷。
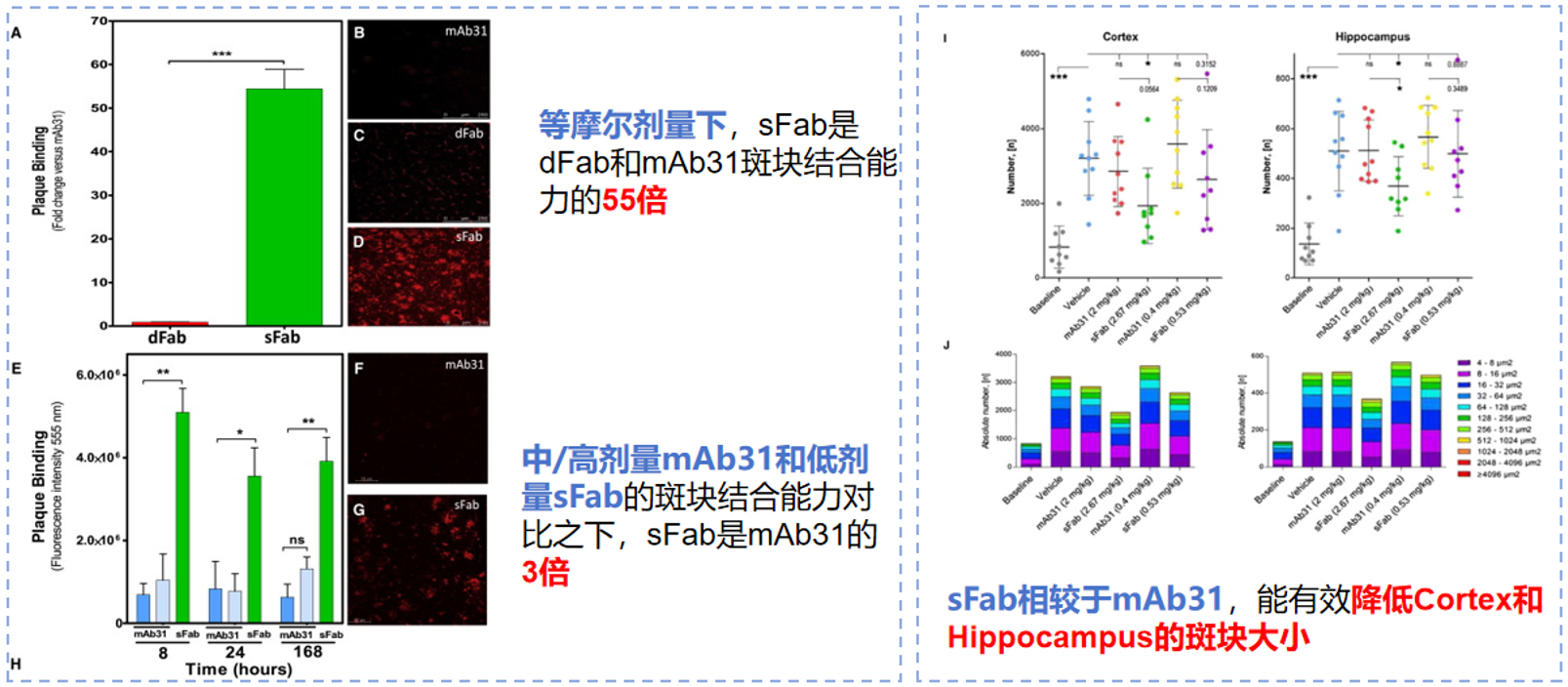
图4
• 安全性验证:TfR1靶向未引入明显不良反应
Trontinemab是在Gantenerumab基础上引入TfR1脑穿梭模块的改造抗体。由于Gantenerumab的安全性已在临床中得到充分验证,评估重点集中于TfR1靶向的潜在风险。研究表明,单价TfR Fab不会干扰转铁蛋白与TfR1的天然结合,亦未诱导明显的ADCC效应,从而降低了初次输注反应的风险。
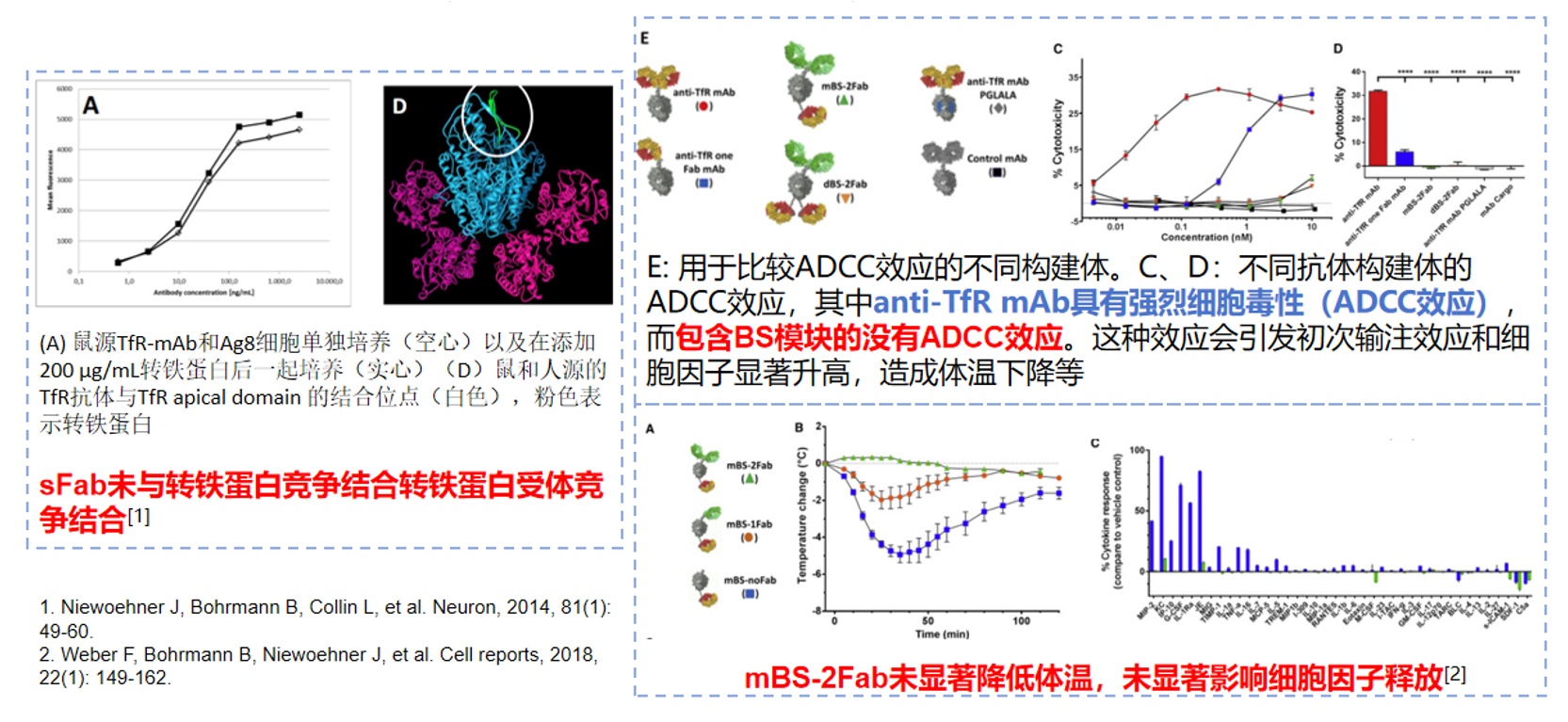
图5
• Trontinemab的药代动力学特征
与Gantenerumab相比,Trontinemab的血浆暴露水平降低,主要归因于其TfR1 Fab结构可与外周TfR1结合,加速外周清除。然而,在脑组织分布方面,Trontinemab在多个脑区均显示出更高的暴露水平。7天重复给药研究表明,其脑内暴露量可达Gantenerumab的12.4倍。
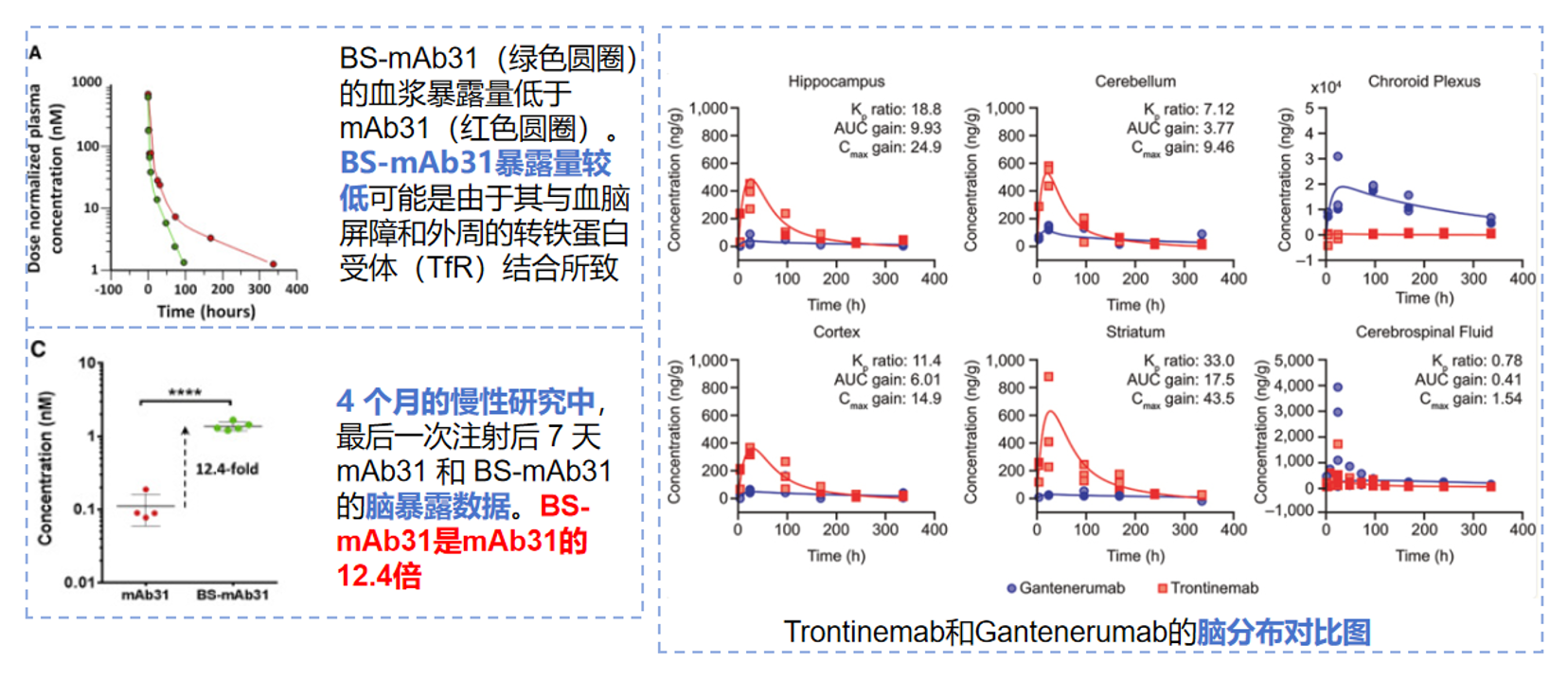
图6
同期,Gantenerumab临床试验失败:
尽管Gantenerumab在多项临床试验中证明了其对于斑块的清除作用,但在临床Ⅲ期GRADUATE I 和GRADUATE II 中未达主要临床终点。Gantenerumab的失败并未完全否定Aβ靶向治疗策略,脑内有效暴露不足可能是其重要原因之一。
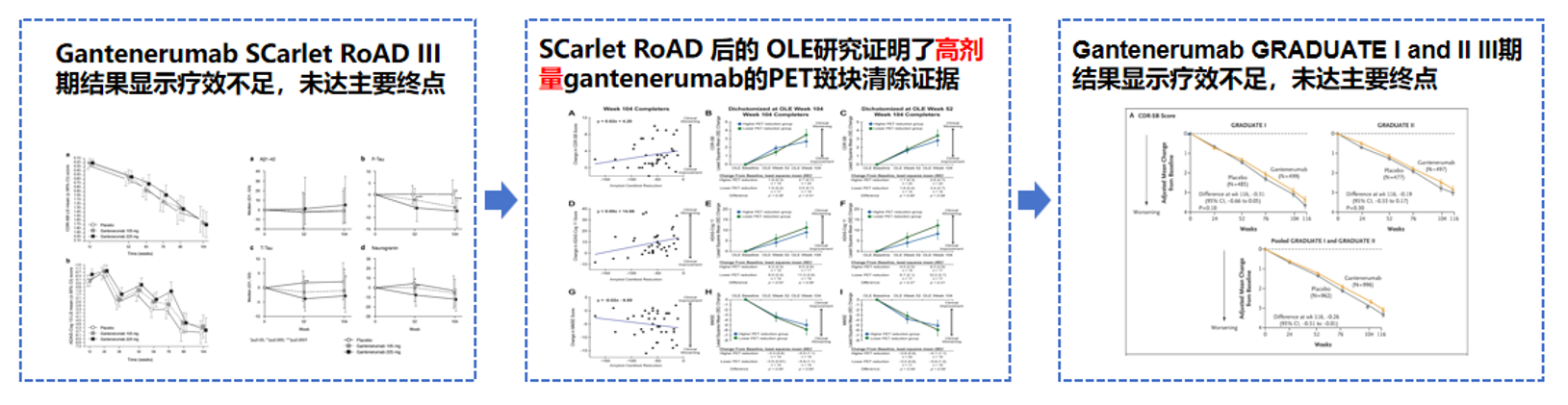
图7
Trontinemab Phase I,Phase Ib/IIa成功:
Trontinemab的临床Ⅰ期获得成功,相比于Gantenerumab,脑/血浆暴露比提升近8倍。在Ib/IIa期临床试验中,91%的受试者的Aβ斑块减少,且有更低的ARIA发生率。目前罗氏已宣布启动III期临床试验。
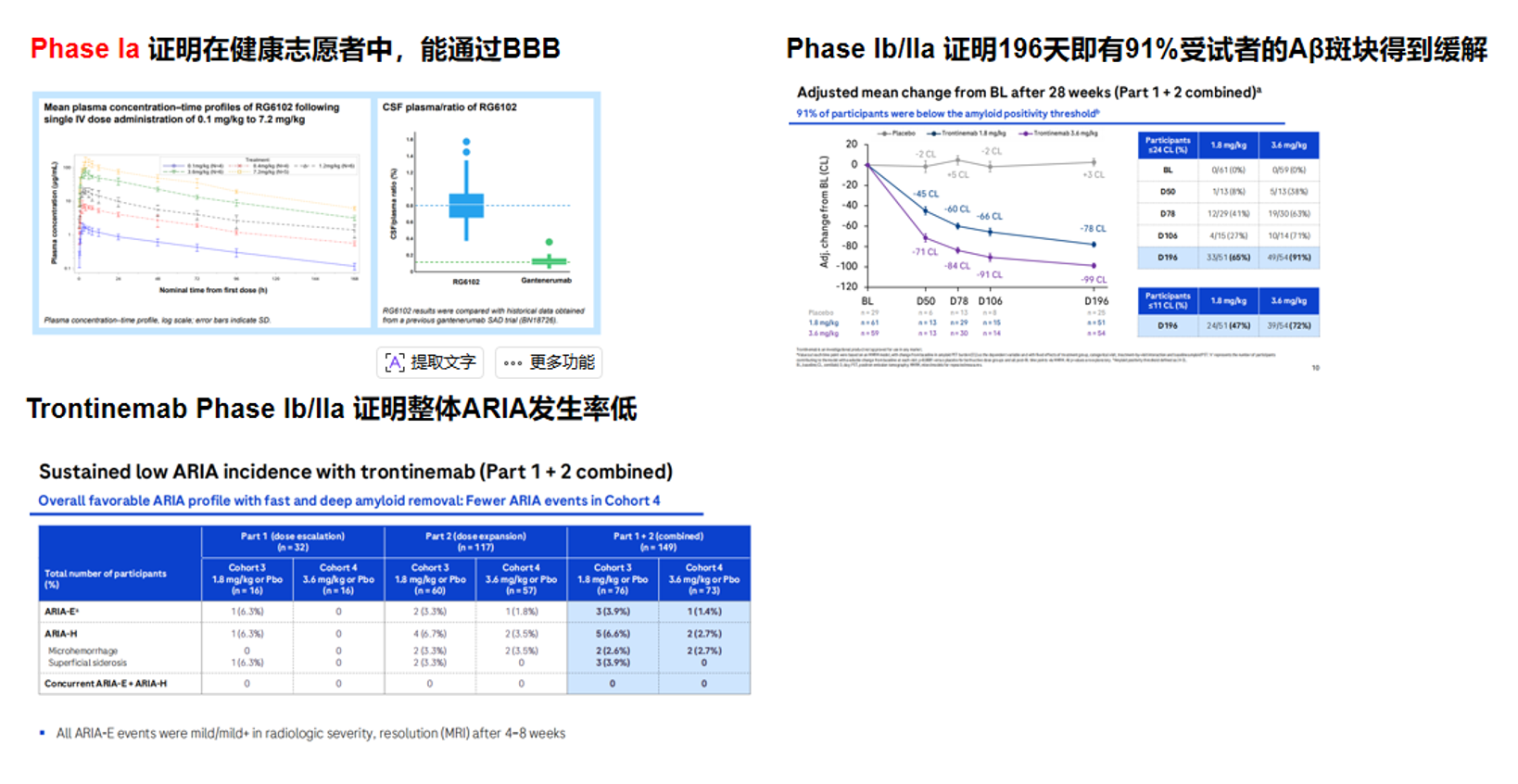
图8
案例二
BioArctic:BrainTransporter技术
BioArctic成立于2003年,由Lars Lannfelt教授基于其在阿尔茨海默病发病机制中Aβ寡聚体的突破性研究创立。公司早期以抗体药物研发为核心,并于2005年与卫材建立长期战略合作,共同推进阿尔茨海默病抗体药物的开发,最终促成全球近20年来首款获完全批准的阿尔茨海默病药物Lecanemab(伦卡奈单抗)的临床试验与全球商业化落地。
2020年后,公司战略重心从单一抗体资产拓展至血脑屏障递送这一关键工程难题,成功推出BrainTransporter技术平台。其美国核心专利(US11498974)有效期至2037年。近年来,BioArctic先后与多家大型制药巨头达成合作,包括2024年与卫材签署研究评估协议,旨在验证该平台在未公开的阿尔茨海默病候选药物中的脑内递送能力。
增效能力;同年 12 月,公司与BMS达成全球独家许可协议(首付款1亿美元,总金额12.5亿美元),将 BrainTransporter™ 应用于 PyroGlu- Aβ 抗体项目 BAN2803。2025 年,与Novartis签署研究合作与许可选择协议,将该平台用于其未披露的神经退行性疾病抗体项目,BioArctic获得 3000 万美元预付款,潜在里程碑总额最高可达 7.72 亿美元。
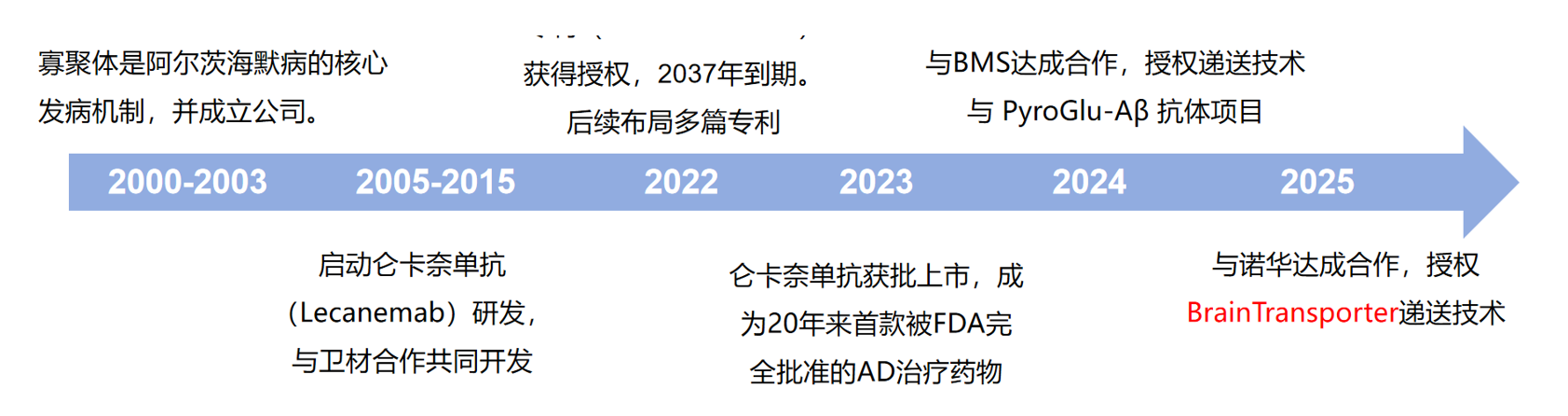
图9 BioArctic发展时间线
BrainTransporter™的独特结构设计:
图10展示了BrainTransporter™核心专利中披露的分子结构设计与机制验证数据。从分子工程视角,该技术呈现清晰的设计逻辑:在保持治疗性抗体结构完整性与靶点亲和力的前提下,于抗体C端对称融合两个anti-TfR单链抗体片段,实现与血脑屏障TfR的功能性单价结合。
该设计的精妙之处不在于“能否结合TfR”,而在于通过空间构象限制确保任一时刻仅允许单个scFv与TfR单体发生1:1结合,从结构层面规避二价交联可能诱发的受体聚集与溶酶体降解途径。专利及结构示意图显示,短而柔性的连接肽在空间上有效限制了双scFv同时参与结合的可能性,使分子在BBB内皮细胞侧呈现“低亲和、可逆结合—快速解离—跨膜转运”的理想动力学特征。
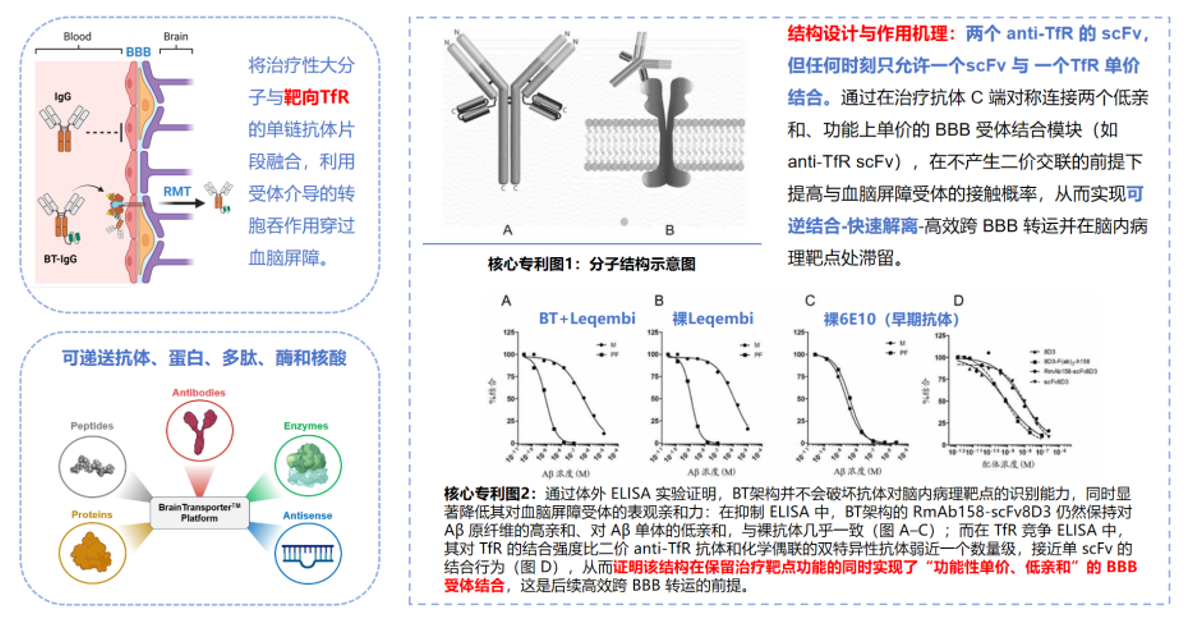
图10 BrainTransporter™的结构设计与机制验证(专利数据)
图11数据显示,BrainTransporter™架构下的抗体相较裸抗体,脑摄取效率提升,且未因与BBB受体结合过紧而快速内吞降解,实现了稳定、可持续的脑内滞留。同时,肝脏、脾脏、肾脏等外周器官未见异常富集,表明该技术未引入明显的非特异性组织蓄积风险。上述药代分布特征从体内层面支持了BrainTransporter™作为系统给药生物药递送平台的安全可行性。
BrainTransporter™的脑摄取特性和安全性:
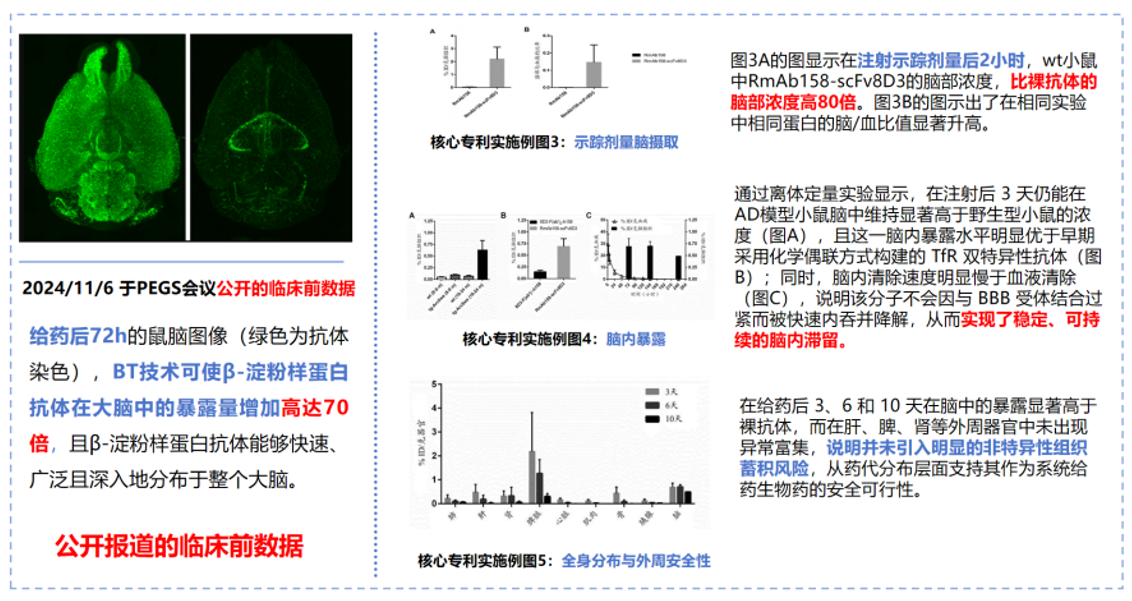
图11
BrainTransporter™脑分布特性和药效:
图 12 所呈现的实验结果证实,在 BrainTransporter™ 架构赋能下,所涉及的抗体能够在脑实质内实现均匀且广泛的分布,而非仅仅局限于脑血管或脑室周围等局部区域。
进一步开展定量分析,结果显示该分子在阿尔茨海默病关键病理区域,如海马体(海马)、大脑皮层(皮层)等部位所检测到的信号强度高于小脑区域。这一数据差异表明,该分子在成功穿透血脑屏障进入脑内后,具备与特定病理靶点特异性结合的能力,并能够在靶点所在区域实现选择性富集与保留。
与此同时,通过离体放射自显影技术结合 Aβ 免疫染色实验发现,该分子在阿尔茨海默病模型小鼠脑实质中的空间分布模式与 Aβ 病理区域的分布呈现出高度一致性,即二者在脑内的分布范围存在重合区域。这一发现为该分子在阿尔茨海默病靶向治疗中的潜在应用提供了坚实的实验依据。

图12
图13比较了示踪剂量与治疗剂量下的脑摄取情况。结果显示,治疗剂量下BrainTransporter™仍能提高脑内暴露水平。尽管其在外周血中的半衰期较裸抗体有所缩短,但单位系统暴露所带来的脑内保留效率显著提升。根据专利说明书实施例数据推算,相较于裸抗体,脑血比提高约10倍。

图13
BrainTransporter™技术的有效性验证遵循系统递进的研究路径:首先,通过分子构建与体外功能实验,确认其工程化设计的可行性。在体内验证阶段,采用示踪剂量系统比较BT抗体与裸抗体在给药后早期及中期时间点的脑摄取情况,证实该架构显著增强了跨BBB转运效率。随后,将观察窗口延伸至给药后3天、6天及10天,对脑内信号进行定量分析,评估其脑内滞留的可持续性。结合PET成像对不同脑区进行分区定量,并通过离体放射自显影与Aβ免疫染色对照分析,验证其脑内分布与病理区域的相关性。
最终,系统比较示踪剂量与治疗剂量下的脑摄取表现。结果显示,BT抗体在治疗剂量下仍能维持显著的脑内暴露提升,未出现因TfR饱和导致的转运效率衰减,同时外周器官未见异常富集或非特异性蓄积。
案例三
Arrowhead TRiM™-BBB技术:实现皮下给药的CNS RNAi递送平台
Arrowhead Pharmaceuticals成立于2003年,是RNA干扰治疗领域最早实现系统性平台化与临床验证的公司之一。在肝脏递送领域,Arrowhead凭借GalNAc平台推动多款候选药物进入临床阶段,验证了其在药代动力学可控性、组织选择性及长期给药安全性方面的工程可行性。
2023年起,Arrowhead将TRiM™平台系统性拓展至中枢神经系统递送领域,并在研发日首次披露TRiM™-CNS技术路线及非人灵长类数据。然而,初代技术仍局限于鞘内给药路径。2025年1月,Arrowhead进一步提交TRiM™-BBB皮下给药平台的关键专利(WO2025160275),首次实现CNS RNAi疗法的皮下给药突破。

图14
TRiM™-BBB核心设计:单价TfR介导的siRNA脑内递送
根据专利披露,TRiM™-BBB平台的核心工程设计为:通过单价结合TfR的Fab片段,将化学修饰的siRNA以不可逆共价方式偶联,构建具备系统给药能力的BBB转运RNAi分子。
该平台采用单价TfR配体作为递送模块,其设计目标并非最大化受体结合强度,而是精确控制结合—解离动力学,以避免二价交联引发的内吞-溶酶体降解通路。Fab与siRNA之间通过化学稳定且不可逆的连接子偶联,在维持血液循环稳定性的同时,最大限度减少体内非特异性释放。
这一设计逻辑与当前主流的单价TfR抗体穿梭策略保持一致,但载荷由大分子抗体转变为siRNA。分子入脑后,siRNA可直接作用于神经元及胶质细胞内的mRNA靶点,实现基因沉默。
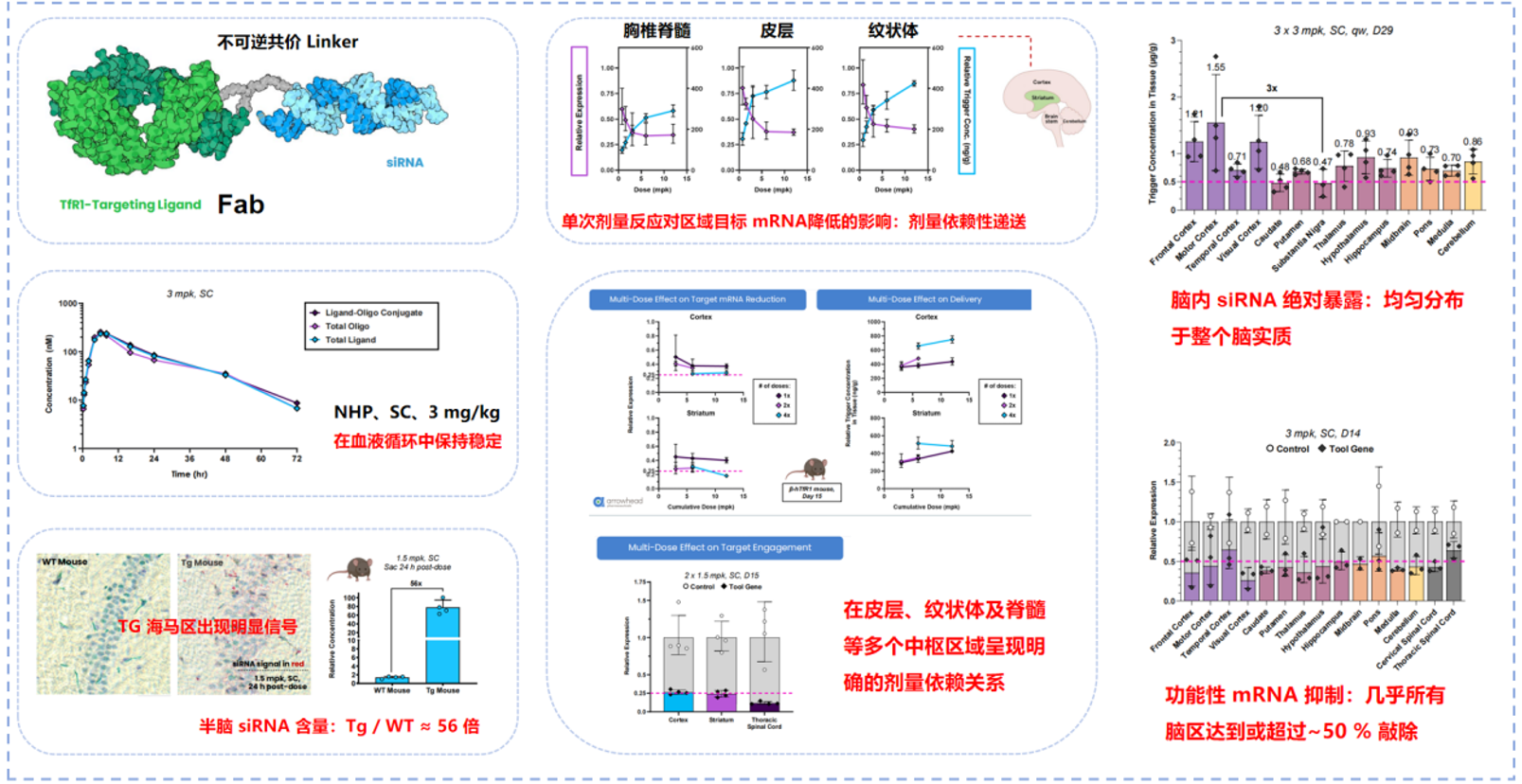
图15
Arrowhead在非人灵长类模型中系统评估了TRiM™-BBB的脑内递送效率与功能性药效。数据显示,皮下给药后,siRNA在皮层、纹状体、丘脑、海马及脊髓等多个CNS区域实现广泛且均一的分布。单次给药条件下,各脑区的目标mRNA敲低水平呈现明确的剂量依赖性;多次给药研究进一步表明,累积剂量的增加可持续提升TRiM™-BBB的脑内暴露水平,并增强mRNA抑制效果,各脑区间的响应趋势高度一致,沉默效率达约50%。
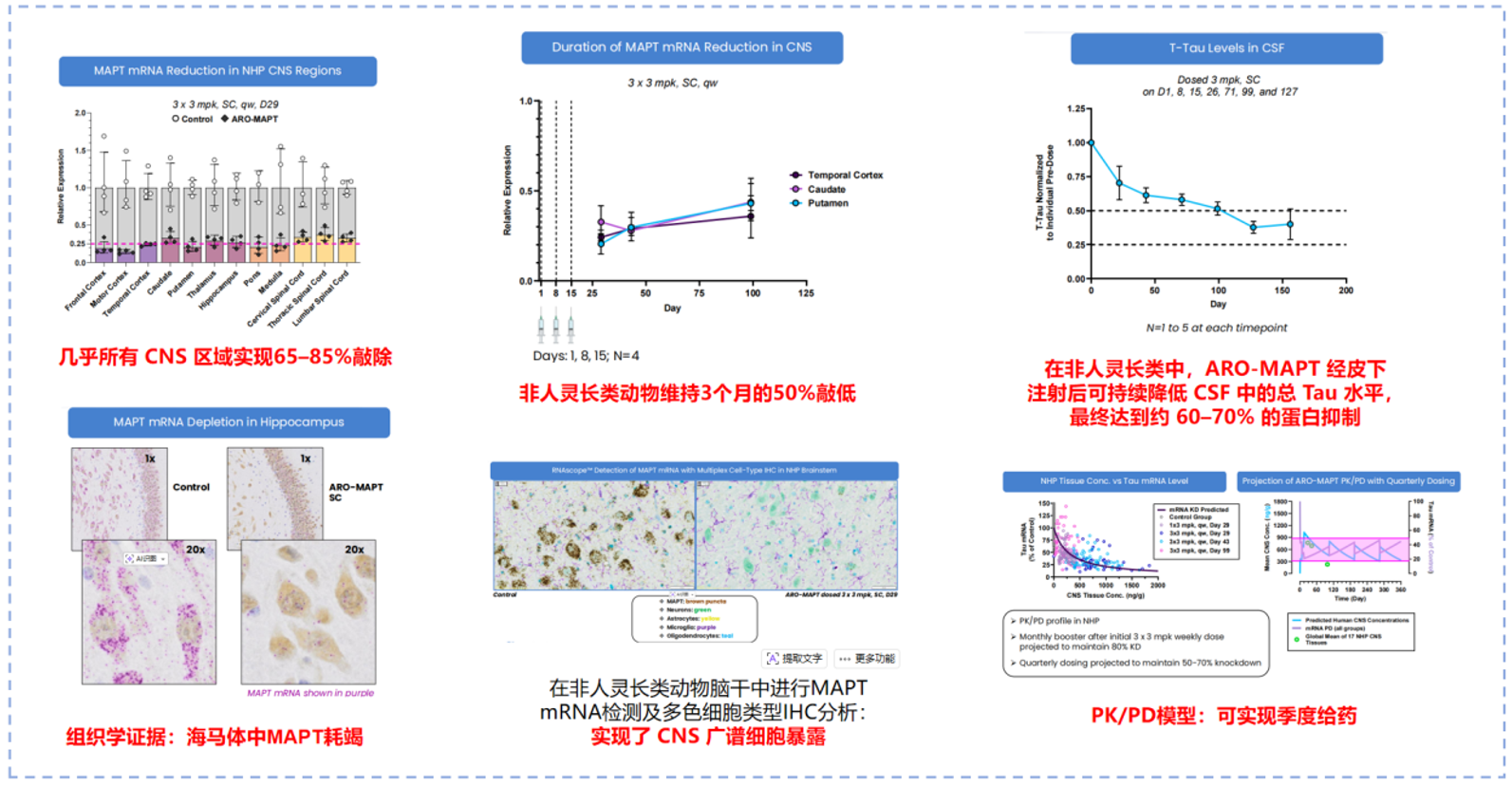
图16
ARO-MAPT:TRiM™-BBB平台的功能性验证
基于TRiM™-BBB平台,Arrowhead开发了靶向MAPT(Tau)的候选药物ARO-MAPT,作为CNS递送能力的功能性验证模型。在非人灵长类动物中,ARO-MAPT经皮下给药后,在几乎所有检测的CNS区域实现65%–85%的MAPT mRNA敲低,效应可持续至少3个月。脑脊液层面,总Tau蛋白水平下降约60%–70%,证明mRNA抑制可有效转化为可测量的蛋白终点。组织学与原位检测显示,MAPT mRNA的降低覆盖神经元及多种胶质细胞类型,表明TRiM™-BBB具备广谱细胞暴露能力,而非局限于单一细胞亚群。
基于NHP数据构建的PK/PD模型显示,TRiM™-BBB分子在外周循环中维持可控暴露的同时,脑内siRNA浓度与mRNA抑制程度呈现良好相关性。模型推演表明,完成初始加载剂量后,通过季度给药有望维持CNS内50%~70%的持续mRNA抑制水平,这一给药频率在慢性神经退行性疾病中具有临床可行性优势。
欢迎交流|BBB递送平台研究与合作对接
技术平台组研判,BBB递送技术正步入价值放大的战略窗口期:递送效率、安全性与可制造性一旦实现工程化突破,将提升CNS项目的成药概率,有望实质性缓解该领域长期存在的转化鸿沟。
除已重点解析的三个典型平台外,我们系统覆盖了另外12个BBB递送技术平台,构建了包含临床前数据解读、核心专利版图、管线与适应症布局、交易并购条款线索在内的一体化情报库。基于公开及可验证资料,我们进一步抽取关键指标,建立了临床前评估参数表与评分框架,用于对不同平台在递送效率、脑区分布、靶点占有、安全窗口及转化可行性等维度进行横向对比,形成初步筛选标准。期待与业内专家交流探讨。
与此同时,我们正依托该框架持续挖掘并更新中国本土BBB递送平台公司图谱,筛选早期具备投资与合作开发潜力的机构。
关于濠麦科技
濠麦科技专注于生物医药领域,致力于通过大数据挖掘与分析、生物化学信息深度建模,结合人工智能工具,为药物发现提供深度技术服务。公司已建立靶点价值评估、资产价值评估关联、专利核心化合物预测等多个研发模型,至今服务超过30家医药上市企业及近100家生物医药企业,助力客户把握创新药发展机遇。团队成员中博士占比超过70%,学术背景覆盖药物化学、药理学、生物信息学及分子生物学等关键领域。
依托技术积累与创新团队,濠麦科技发展出三大业务方向:
濠麦咨询:聚焦创新药管线规划、靶点挖掘与立项评估。通过大数据分析与专家战略洞察,为企业提供立项筛选、研发策略优化及风险评估,发现差异化机会,规避专利与投资风险。
濠麦孵化:依托大数据预测与全球BD资源,挖掘与评估早期生物医药资产及技术平台,提供从立项到研发策略的全方位孵化服务,助力成果转化与价值落地,精准对接潜在合作方。
濠麦会员:依托自研技术矩阵及专家网络,提供跨国药企及肿瘤、自免、代谢等核心领域的深度立项与交易研究报告,助力会员低成本获取高价值的立项与投资洞见。
欢迎交流探讨
蔡鸿
电话:18578675942
邮箱:alex@hq-haomai.com