近日,中国生物制药(1177.HK)核心企业正大天晴自主研发的PDE3/4抑制剂TQC3721混悬液用于慢性阻塞性肺疾病(COPD)的Ⅱ期临床试验(PACER-Ⅱ)研究结果正式发表在国际呼吸领域知名期刊《CHEST》。“PACER”在马拉松比赛中意为“领跑者”,TQC3721混悬液的开发进度不仅为国产最快,用于COPD维持治疗的首个Ⅲ期临床试验顶线数据预计2026年底读出;TQC3721吸入粉雾剂的复方制剂也在同步开发,将进一步夯实集团在呼吸领域的重要治疗地位。

研究背景
COPD是一种以慢性呼吸道症状(呼吸困难、咳嗽、咳痰)为特征的肺部疾病,其病因是慢性气道炎症和持续性气流阻塞。COPD是全球范围内三大死亡原因之一,影响超过3.91亿人。尽管已经上市多种治疗药物,COPD患者仍面临治疗升级时的药物缺乏。
目前的COPD药物治疗,如长效毒蕈碱拮抗剂(LAMA)和长效β2受体激动剂(LABA),旨在改善肺功能,但在控制气道炎症方面疗效有限。吸入性糖皮质激素(ICS)是慢性炎症性气道疾病的主要治疗方法,与LABA或LAMA联用已被证明可以减少COPD急性加重。然而,ICS对于血嗜酸性粒细胞计数低的COPD患者获益有限,且增加肺炎风险。因此,有必要开发能够同时缓解气道炎症和气流阻塞的药物。
磷酸二酯酶(PDEs)是一个酶超家族,负责调控环磷酸腺苷(cAMP)和环磷酸鸟苷(cGMP)使其分解为失活形式。PDE3在气道平滑肌中高表达,而PDE4在几乎所有炎症细胞中表达,TQC3721混悬液作为一款PDE3/4双靶点抑制剂,通过调节气道平滑肌松弛改善通气和抑制炎症的双重机制,从而控制疾病进展。
研究设计
PACER-Ⅱ是一项Ⅱ期、多中心、随机、双盲、安慰剂对照试验,由四川大学华西医院李为民教授牵头、国内27家研究中心共同完成,旨在评价TQC3721混悬液在接受单支扩或双扩张剂背景治疗的COPD患者中的初步疗效和安全性。研究共纳入240例中重度COPD患者,且所有受试者均在接受LAMA、LABA/LAMA或三联进行维持治疗。
204名符合条件的受试者以1:1:1的比例随机分配在3mg、6mg TQC3721或安慰剂组进行治疗,每日2次,治疗期为4周。基线时肺功能严重程度55.4%和44.6%的患者分别属于GOLD 2级和3级;根据不同背景治疗,28.8%和71.2%的患者分别使用LAMA和LABA/LAMA作为背景治疗。主要终点是治疗4周期间,受试者第一秒用力呼气容积(FEV1)峰值较基线的变化。
研究结果
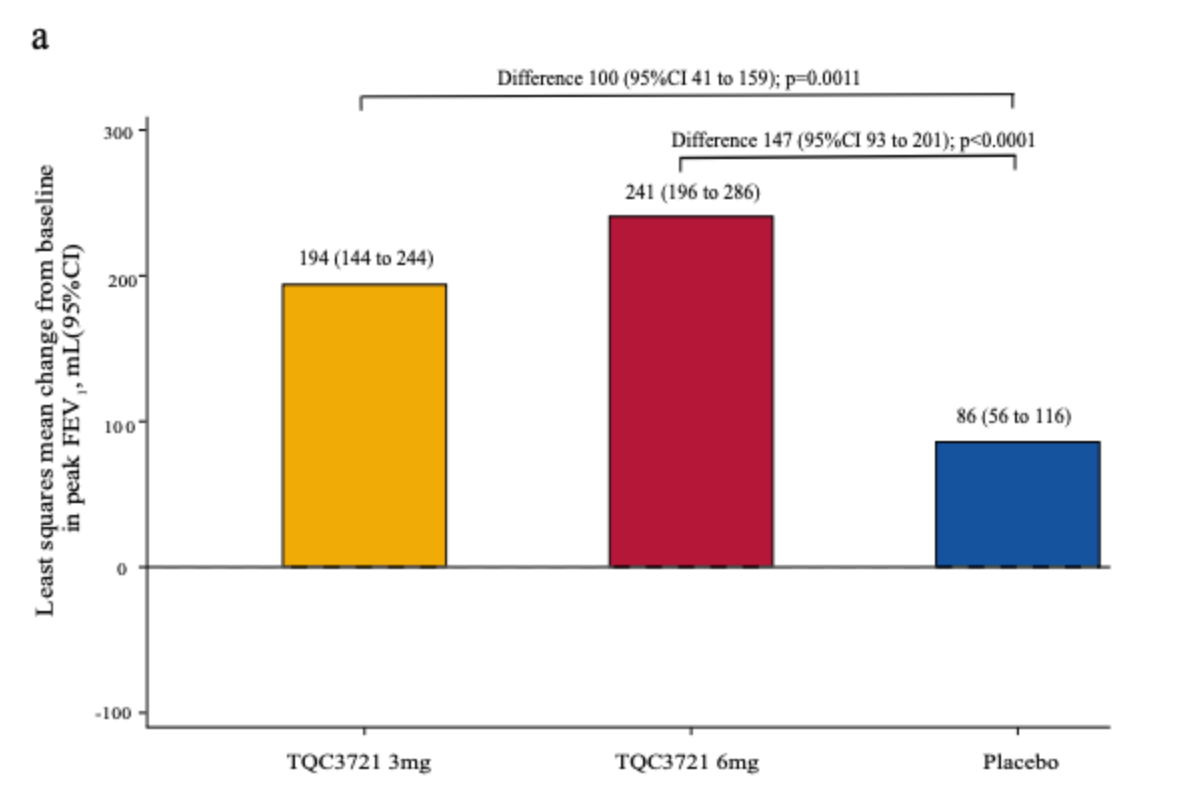
在TQC3721治疗第4周时,FEV1峰值较基线的变化显著改善(图a)。3mg剂量组的FEV1峰值平均提升194mL(95%CI:144-244,P<0.0001);6mg剂量组的FEV1峰值平均提升241mL(95%CI:196-286,P<0.0001)。与安慰剂相比,3mg和6mg TQC3721组均显著更优,差异分别为100ml(95%CI:41-159,P=0.0011)和147ml(95%CI:93-201,P<0.0001)。
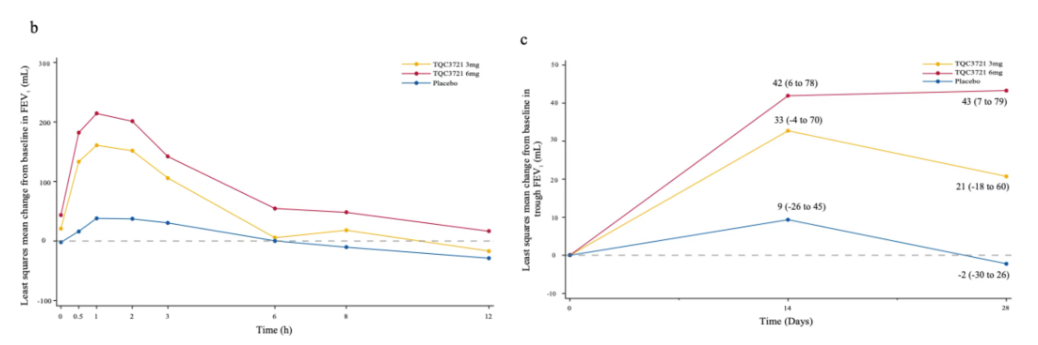
第4周给药后12小时FEV1曲线显示,6 mg剂量的TQC3721比3 mg剂量具有更好的支扩效应,提示治疗效应存在显著的量效关系(图b)。此外,FEV1谷值较基线的改变也显示出明显的量效关系(图c)。
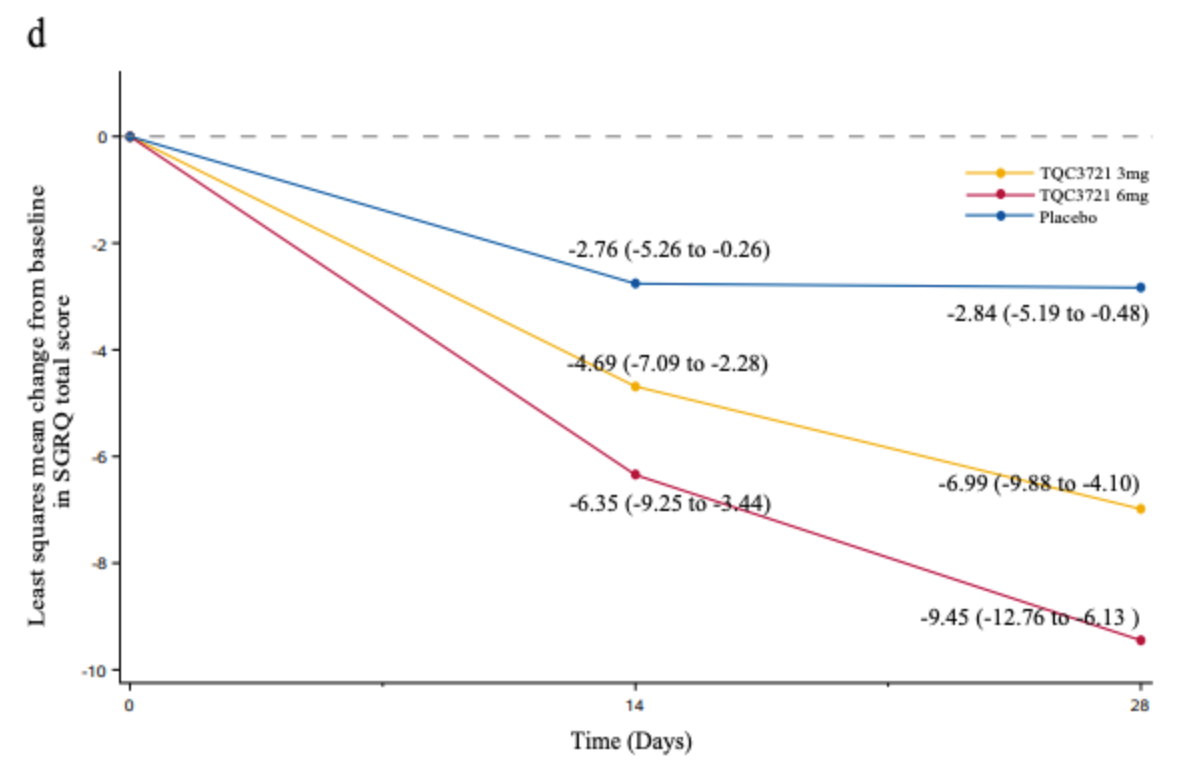
圣乔治呼吸问卷(SGRQ)评分进一步证明,在TQC3721治疗第4周时,患者的症状和生活质量得到显著改善。与安慰剂组相比,3mg剂量组评分平均降低3.56(95% CI:-6.52至-0.61,P=0.0185),6mg剂量组评分平均降低5.09(95% CI:-8.44至-1.74,P=0.0031)(图d)。3mg剂量组(-6.99 [-9.88,-4.10],P<0.0001)和6mg剂量组(-9.45 [-12.76,-6.13],P<0.0001)的平均SGRQ评分较基线的改善,均超过了-4分的最小临床重要差异阈值。此外,3mg和6mg剂量组中达到治疗应答者定义的患者比例分别为 51.85%、59.49%,均高于安慰剂组的33.75%(P=0.0040)。
在LAMA和LABA/LAMA背景治疗亚组以及GOLD 2和GOLD 3亚组分析中,也观察到了显著的临床获益。
安全性
本研究中TQC3721混悬液吸入给药安全性良好。TQC3721组和安慰剂组的不良事件总体情况和发生率相似。
这项研究被命名为“PACER(领跑者)”,寓意为引领COPD领域的创新药物研发。基于Ⅱ期研究的积极进展,TQC3721混悬液正在开展用于COPD维持治疗的Ⅲ期关键验证研究(NCT07147946)。2025年7月,监管部门批准了TQC3721混悬液在COPD治疗的突破疗法申请,首个Ⅲ期试验有望在2026年底获得顶线数据。
除吸入混悬液外,TQC3721吸入粉雾剂也已进入Ⅱ期临床试验阶段,预计于2026年年中获得顶线数据,届时将向监管沟通关键验证研究的开展。公司还在同步推进TQC3721粉雾剂复方制剂的开发,进一步夯实PDE3/4抑制剂在COPD治疗领域的地位。