2026年3月20日,复宏汉霖(2696.HK)发布2025年年度业绩。业绩期内,公司实现营收66.666亿元,同比增长16.5%;净利润8.270亿元,公司全年研发投入达24.919亿元,同比增长35.4%,在持续加大创新投入的背景下,研发投入前利润达23.425亿元,同比增长26.2%。这是公司自2023年首次实现全年盈利以来,连续三年实现营收、利润双增长,展现出稳健的盈利韧性和高质量增长能力。


2025年,复宏汉霖全球化增长动能持续释放,全球产品收入达到57.746亿元,同比增长17.0%。随着公司核心产品H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)及汉曲优®(曲妥珠单抗,美国商品名:HERCESSI™,欧洲商品名:Zercepac®)海外收入的持续增长及授权合作价值加速兑现,公司海外收入强劲攀升:2025年海外产品收入超过2亿元,同比增长翻倍;海外产品利润达0.939亿元。截至目前,公司共有10款产品在全球60个国家和地区获批上市,其中7款已在中国获批,4款获得美国FDA批准、4款获得欧盟EC批准,惠及全球超100万患者。

复宏汉霖执行董事、首席执行官朱俊博士表示“2025年不仅是复宏汉霖迈向全球化2.0的破局之年,更是创新管线加速兑现的一年。伴随海外业务的持续增长与管线突破,我们更加笃定地践行生物医药创新的第一性原理,回归对临床痛点的极致探索与解答。未来,复宏汉霖将继续依托一体化平台和全球化运营能力,推动更多优质生物药在全球落地,以高质量的创新兑现造福全球患者的长期承诺。”
产品收入再创新高,商业化矩阵协同发力
2025年,复宏汉霖创新药与生物类似药管线协同发力,推动整体产品收入再创新高。
公司核心产品H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)持续释放全球商业化潜力,于业绩期内实现全球销售收入14.926亿元,同比增长13.7%。2025年,H药在欧洲及多个新兴市场获批用于一线治疗广泛期小细胞肺癌(ES-SCLC),在印尼和泰国获批治疗鳞状非小细胞肺癌(sqNSCLC),并在德国、意大利、西班牙等7个欧盟成员国完成医保准入。截至目前,H药已在40余个国家和地区获批上市,并持续在肺癌和消化道肿瘤上取得突破,剑指多项“全球首个”。继成为全球首个获批一线治疗SCLC的抗PD-1单抗,H药也是全球首个胃癌围术期以免疫单药取代术后辅助化疗的治疗方案。同时,H药一线治疗转移性结直肠癌(mCRC)的国际多中心III期研究也已完成入组,有望成为首个一线治疗微卫星稳定型mCRC的免疫抑制剂。随着全球商业化势能与差异化临床价值的加速释放,H药目标成为下一款全球年销售额突破百亿人民币的国产创新药。
围绕更广泛的临床需求,H药在中国、欧盟、美国、日本及更多新兴市场的临床开发和注册进程全面提速。在中国,H药获得国家药品监督管理局突破性疗法认定用于胃癌围手术期治疗,相关上市申请已获受理并纳入优先审评,并有望于2026年获批;同时,H药治疗局限期小细胞肺癌(LS-SCLC)的适应症也计划于2026年递交上市注册申请(NDA)。在欧盟,H药治疗鳞状和非鳞状非小细胞肺癌及食管鳞癌(ESCC)的适应症也有望于2026年获批。在美国,H药一线治疗ES-SCLC的美国桥接试验已完成患者入组,计划2026年向FDA递交相应生物制品许可申请(BLA)。
通过自主研发与合作引进,公司已建立覆盖乳腺癌全程全域全球的治疗管线,业绩期内实现乳腺癌领域产品全球销售收入32.675亿元。核心产品汉曲优®(曲妥珠单抗,美国商品名:HERCESSI™,欧洲商品名:Zercepac®)全年实现全球销售收入29.645亿元,同比增长5.5%,目前已在全球50多个国家和地区获批上市,并已进入中、英、法、德等多国医保体系。汉奈佳®(奈拉替尼)实现销售收入3.012亿元,同比增长564.2%,持续巩固其在HER2阳性早期乳腺癌强化辅助治疗中的优势品牌地位。创新CDK4/6抑制剂复妥宁®(枸橼酸伏维西利胶囊)则于2025年下半年实现首批处方落地并纳入新版国家医保目录。HLX11(帕妥珠单抗)于2025年下半年获得美国FDA批准(商品名:POHERDY®),成为美国首款且唯一1的帕妥珠单抗生物类似药,并在欧盟获得EMA上市许可积极意见,以及在中国及加拿大递交上市申请。公司持续打造更完善的乳腺癌创新产品矩阵,新型内分泌疗法、新表位抗HER2单抗、HER2 ADC、KAT6A/B口服小分子抑制剂、HER2双表位ADC、LIV-1 ADC等正在加速布局。
公司成熟商业化品种亦持续贡献稳定现金流。汉贝泰®(贝伐珠单抗)实现销售收入3.564亿元,同比增长80.8%。基于与合作伙伴的约定,公司就汉利康®(利妥昔单抗)实现销售及授权许可收入6.117亿元,同比增长11.1%;汉达远®(阿达木单抗)实现销售及授权许可收入0.592亿元,同比增长47.6%。2025年下半年,HLX14(地舒单抗)两个规格产品分别以BILDYOS®(60mg/mL) 和 BILPREVDA®(120mg/1.7mL) 为商品名在美国、欧盟和英国获批上市,并于近期分别以BILDYOS®和TUZEMTY®为商品名在加拿大获批上市,成为首个出海的“中国籍”地舒单抗。目前,HLX14双规格产品已在美国及德国、西班牙、英国实现商业上市,并于业绩期内实现销售收入983万元。
全球化势头持续高涨,加速创新管线突破
2025年,公司持续拓展产品国际注册与商业合作边界,在全球范围内收获27项临床试验申请(IND)批准、28项上市注册申请批准,覆盖中、美、欧、日、加等60余个国家和地区,并在近30个国家和地区有序推进临床研究,加速产品全球化进程。同时,复宏汉霖全球商业“朋友圈”持续扩容。业绩期内,公司与Abbott、卫材、Lotus等多家国际领先合作伙伴就H药的权益达成合作;与Dr. Reddy’s和Sandoz分别就HLX15(达雷妥尤单抗)及HLX13(伊匹木单抗)开展授权合作。

作为公司的重要创新资产,新表位抗HER2单抗dulpatatug(HLX22)2头对头对比一线标准疗法治疗HER2阳性胃癌的国际多中心III期临床研究稳步推进,已在中国、美国、欧洲、日本、澳大利亚、韩国及拉美等多个国家和地区完成首例患者入组。其治疗胃癌的II期研究长期随访结果于2025年美国临床肿瘤学会年会(ASCO)发布,显示其疗效获益稳定且优于历史数据,总人群降低疾病进展和死亡风险80%。除胃癌外,dulpatatug亦加速向乳腺癌等更多适应症拓展。其治疗HER2低表达乳腺癌的II期研究已完成患者入组;同时,联合HER2 ADC HLX87一线治疗HER2阳性乳腺癌的II/III期研究已完成首例患者给药。
作为潜在同类最优(BIC)的广谱抗肿瘤PD-L1 ADC,HLX43“单药即管线”的潜力加速兑现。HLX43首次人体研究结果、多项实体瘤概念验证数据先后亮相多场国际学术大会,展现出“高效、低毒”的显著疗效,尤其在NSCLC人群中不依赖生物标志物筛选,有望覆盖所有亚型患者。除NSCLC外,HLX43已在妇科肿瘤、食管鳞癌等多个实体瘤中展现积极疗效信号。单药之外,公司也积极探索其与抗EGFR单抗pimurutamab(HLX07)、H药等药物的联合治疗潜力。2026年,公司将进一步加速HLX43在广泛实体瘤中的概念验证,并计划高效推进多项全球关键注册性研究。
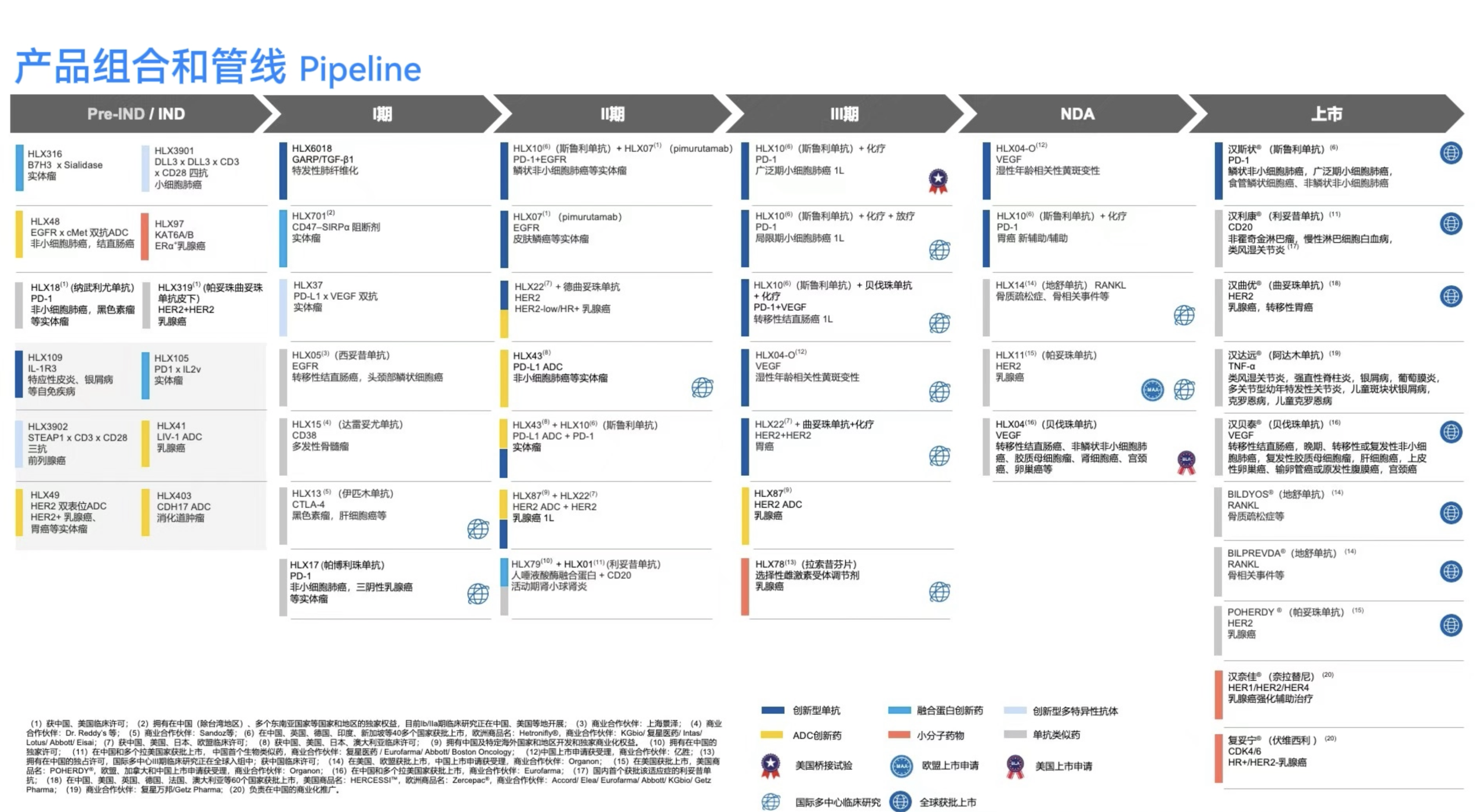
2025年,复宏汉霖持续强化平台化创新体系建设,形成涵盖下一代IO平台、Hanjugator™ ADC平台、三特性T细胞衔接器及AI驱动的一站式抗体药物早期研发HAI Club平台在内的多维技术平台。业绩期内,HLX37(PD-L1 x VEGF双抗)、HLX97(KAT6A/B小分子抑制剂)、HLX3901(DLL3 x DLL3 x CD3 x CD28四抗TCE)、HLX316(B7-H3唾液酸酶融合蛋白)等分子获得新药临床试验批准。同时,公司持续推进多款潜力候选分子研发,包括HLX3902(STEAP1 x CD3 x CD28三抗TCE)、HLX48(EGFR x cMET双抗ADC)、HLX49(HER2双表位ADC)、HLX109(IL-1R3单抗)等,持续丰富具备全球竞争力的创新管线。
作为全球化2.0的重要基础,复宏汉霖持续夯实生产与质量体系建设。徐汇基地、松江基地(一)及松江基地(二)三大生产基地现有总产能达84,000升,累计完成GMP商业化生产批次逾1,300批次,实现全球产品常态化供应。截至目前,公司商业化生产基地及配套质量管理体系已通过近百项来自各国药监机构及国际合作伙伴的实地核查与审计,均无重大发现项,核查通过率100%,并获得中、欧、美及多个PIC/S成员国GMP认证与ISO 9001、ISO 14001、ISO 45001认证。业绩期内,公司全球商业化供应能力进一步提升。H药、汉曲优®及双规格地舒单抗(HLX14)四款产品实现海外首批发货,覆盖美国、英国、德国、西班牙、印度等8个国家,全年累计完成逾30次海外发货。同时,公司持续完善国际化生产与质量体系建设。2025年,HLX14实现欧洲首发,公司首次代表上市许可持有人(Marketing Authorization Holder,MAH)身份完成欧洲获批全流程;日本MAH配套质量体系成功搭建。
以患者为中心,开启C-MNC时代
未来,复宏汉霖将继续坚持“以患者为中心”的理念,依托稳健的商业化基础、持续迭代的创新引擎与不断完善的全球运营体系,推动更多高质量生物药惠及全球患者。围绕2030年愿景,复宏汉霖将继续坚定迈向全球的步伐,并开启C-MNC生物制药企业(以中国为总部的跨国生物制药企业)时代,力争实现20+款产品全球上市,其中15+款登陆欧美市场,加速成长为具备全球影响力的国际化创新生物制药企业。
关于复宏汉霖
复宏汉霖(2696.HK)是一家国际化创新生物制药企业,致力于为全球患者提供高品质、可负担的生物药,产品覆盖肿瘤、自身免疫疾病、眼科疾病等领域。自2010年成立以来,公司已构建涵盖全球研发、临床、注册、生产及商业化的全产业链平台,拥有全球员工近4,000人,并在中国、美国和日本等多地设有运营及分支机构。依托生物类似药形成的稳健现金流反哺创新研发,复宏汉霖正稳步迈入“全球化2.0”阶段,持续打造可复制、可持续的全球增长模式。截至2026年初,公司共有10款产品在全球60个国家和地区获批上市,其中7款已在中国获批。在欧美主流生物药市场,复宏汉霖亦取得多项里程碑式突破,已有4款产品获得美国FDA批准、4款产品获得欧盟EC批准,充分体现了公司在研发体系、质量管理及生产能力方面已全面对标国际最高标准。
在创新驱动方面,复宏汉霖依托上海、美国等多地协同布局的研发体系,构建了多元化、平台化的创新技术矩阵,覆盖免疫检查点抑制剂、免疫细胞衔接器(包括多特异性TCE)、抗体偶联药物(ADC)以及AI驱动的早期研发平台等前沿方向。目前,公司拥有50余项处于早期阶段的创新资产,其中约70%具备同类最佳(Best-in-Class)潜力,并在全球同步推进30余项临床研究。核心产品H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)作为全球首个获批一线治疗小细胞肺癌的抗PD-1单抗,正加速全球布局,已在全球40余个市场获批上市;同时,多款潜力创新资产,包括PD-L1 ADC HLX43及新表位HER2单抗HLX22正全面推进全球关键性临床研究。依托通过中、欧、美三地GMP认证的生产体系,复宏汉霖已建成总产能达84,000升的生物药生产平台,形成覆盖全球六大洲的稳定供应网络。未来,复宏汉霖将始终坚持以患者为中心,聚焦未满足的临床需求,持续推动创新成果向临床价值与患者可及转化,在全球生物医药创新生态中创造长期而稳健的价值。
注释
1.U.S. FDA官网,访问日期:2026年3月20日
2.药品通用名处于pINN状态