云顶新耀(HKEX 1952.HK)是一家专注于创新药研发、临床开发、制造和商业化的生物制药公司,今日公布2025年度全年财务业绩报告(截至2025年12月31日)及业务进展。
公司2025年营收大幅增长,实现全年总收入人民币17.07亿元,大幅增长142%。报告期内,公司运营费用占收入比重同比下降90.1个百分点,国际财务准则下亏损大幅收窄71%,非国际财务准则下首度实现扭亏为盈人民币1.87亿元,整体经营质量稳步提升。2025年公司剔除非现金项目后毛利率为74.1%,体现产品组合结构的持续优化与规模效应增强。截至2025年12月31日,公司现金储备充裕,达人民币27.31亿元,有力支撑商业化拓展、自主研发及中长期战略布局。
云顶新耀董事会主席吴以芳表示:“2025年,公司凭借卓越的战略执行力取得令人瞩目的业绩表现,非国际财务准则下首度实现扭亏为盈,经营性现金流转正,现金储备保持充裕,这充分印证了云顶新耀持续将创新成果转化为商业价值的卓越能力,并为持续投入BD引进及研发管线建设、推进长期价值创造奠定了坚实基础。公司在商业化与自主研发方面取得的突破性进展,标志着公司已建立起可持续的自我“造血”能力,整体经营质量迈上新台阶,为长期稳健发展提供了有力支撑。
立足当下,随着2030年战略规划的发布,我们已明确未来五年的发展路径,依托已建立的能力与成果,云顶新耀致力于建设成为具有全球创新力的生物制药企业,打造中国创新药商业化的领先平台,推动具有重大临床价值的创新成果惠及全球患者。
围绕这一愿景,公司计划到2030年营收突破150亿元人民币,并将持续在肾科、心血管及代谢、自身免疫、眼科及急重症等重点战略领域构建“N+X”产品组合,把握蓝海大单品机遇。公司提出每年引进3至5个重磅产品,力争在2至3年内实现获批上市,5至6年内达成单品峰值销售超20亿元的BD合作引进目标。通过战略投资与独家商业化授权,公司持续扩大后期产品管线布局,同时强化对现有商业化平台的高效利用,将为公司的长期价值增长发挥核心作用。过去6个月,公司已引进及合作4款创新药和6款成熟原研产品,进一步拓宽治疗领域,增加管线厚度。
总体而言,2026年将是云顶新耀的“执行之年”和实现转型的关键之年。公司旨在拓展商业化产品组合,加速重点资产向重磅产品迈进,并持续提升自主研发管线在全球的竞争力。”
云顶新耀首席执行官罗永庆表示:“2025年,云顶新耀的卓越商业化平台得到验证,销售收入实现快速增长,内部研发管线稳步推进,同时BD合作取得显著成果。
商业化方面,耐赋康®全年销售收入突破14亿元,同比增长超过300%,依嘉®实现2.62亿元,院内销售同比增长44%。公司搭建的“准入、医学、市场、销售”(A2MS)系统化平台持续赋能维适平®等产品,助力其商业价值实现,维适平®有望成为下一个重磅大单品,预期峰值销售50亿元。
研发方面,希布替尼(EVER001)在原发性膜性肾病(pMN)的1b/2a期临床试验中取得积极结果,项目正推进后期临床开发及拓展适应症的篮式试验,进一步强化公司的全球研发管线。国际领先的自研mRNA肿瘤疫苗和In vivo CAR-T两大技术平台强化了公司的创新引擎。个性化mRNA肿瘤疫苗项目EVM16已完成研究者发起临床研究(IIT)初步剂量爬坡;现货型TAA mRNA疫苗EVM14实现中美新药临床试验申请(IND)“双获批”,并已实现中美首例患者入组给药。mRNA自体生成CAR-T项目EVM18在非人灵长类动物中完成概念验证并推进临床开发,加快构建具有全球竞争力技术平台的战略布局。
BD合作持续为公司的长期价值增长发挥核心作用。过去一年,公司深化BD布局,通过战略投资新桥生物并引进VIS-101,拓展眼科领域;与海森生物达成CSO合作并引进乐瑞泊®,强化心血管及代谢产品组合。2026年初,公司引进麦科奥特MT1013,完善肾科布局并拓展慢性肾脏病领域,显著丰富了后期产品管线,提升商业化平台的协同效应与运营效率。与此同时,公司从箕星药业引进艾曲帕米鼻喷雾剂,其新药上市申请已获中国国家药品监督管理局受理,预计将于2026年第三季度获批,进一步深化心血管领域战略布局。
未来,云顶新耀将持续以“双轮驱动”为核心,推进外部合作与自主研发,在此基础上,公司将巩固核心治疗领域的领先地位,稳步推进创新药商业化平台建设与全球研发布局,夯实长远发展,成长为立足亚太、面向全球的领先生物制药企业。”
最新主要产品亮点和预期里程碑
-肾病管线-
耐赋康®(NEFECON®)
耐赋康®(Nefecon®)是布地奈德肠溶胶囊,作为全球首个对因治疗IgA肾病的药物,是靶向肠道黏膜B细胞的免疫调节剂,能有效保护肾功能,用药一个疗程,在中国人群中能延缓肾功能衰退达66%,预计将疾病进展至透析或肾移植的时间延缓12.8年。同时布地奈德首过代谢程度达90%,具有良好的安全性。耐赋康®专为IgA肾病患者研制,每颗胶囊含布地奈德4mg,通过特殊的迟释及缓释双重制剂工艺,将布地奈德靶向释放于回肠末端的黏膜B细胞(包括派尔集合淋巴结),胶囊溶解后,三层包衣微丸持续稳定释放布地奈德,高浓度覆盖整个靶区域,从而减少诱发IgA肾病的半乳糖缺陷的IgA1抗体(Gd-IgA1)产生,进而干预发病机制上游阶段,达到治疗IgA肾病的作用。耐赋康®于2023年11月获得中国国家药品监督管理局(NMPA)批准用于治疗原发性IgA肾病,并于2024年5月在中国大陆上市。自2025年1月起,耐赋康®(NEFECON®)已正式纳入国家医保药品目录(NRDL),大幅提升了这一疾病首创药物的患者可及性,并成为首个在医保首年销售收入突破10亿的非肿瘤药物。
2025
-
2025年1月,耐赋康®开始执行国家医保价格,此前耐赋康®于2024年11月被纳入国家医保药品目录。患者可在定点医疗机构或定点药店购买耐赋康®,并享受医保价格。国家医保药品目录的正式实施提升了耐赋康®的可及性,减轻患者负担,使更多中国IgA肾病患者从这款创新药物中获益。
-
2025年5月,耐赋康®获得国家药品监督管理局批准,由附条件批准转为完全批准。这一里程碑意味着耐赋康®成为目前首个且唯一获得国家药品监督管理局完全批准的IgA肾病对因治疗药物。此次获批是基于NefIgArd III期临床研究的完整数据。NefIgArd III期临床试验是一项随机、双盲、全球多中心研究,在接受RAS抑制剂优化支持治疗的原发性IgA肾病成人患者中评估了耐赋康®(16mg,每日一次)与安慰剂相比的疗效和安全性。
-
2025年5月,耐赋康®被纳入《中国成人IgA肾病及IgA血管炎临床实践指南(预审版本)》,推荐对有疾病进展风险的IgA肾病患者进行9个月的布地奈德肠溶胶囊对因治疗,不受蛋白尿水平的限制,以降低致病性IgA(Gd-IgA1)(2B)。指南建议对于蛋白尿≥0.5 g/d(或同等水平)的患者进行肾活检并启动治疗。同时,指南首次提出针对免疫性损伤进行干预,包括采取减少致病性IgA等治疗措施。 减少致病性IgA的治疗,首选耐赋康®。达到短期治疗目标后,即蛋白尿缓解(蛋白尿<0.5 g/d,理想情况<0.3 g/d)及肾功能稳定,可以采取小剂量维持或重复安全有效的免疫治疗和继续维持支持治疗,以保证eGFR每年下降<1 ml/min。
-
2025年6月,云顶新耀在第62届欧洲肾脏协会(ERA 2025)大会上,展示了耐赋康®9项最新研究成果,包括8项口头报告和1项电子壁报。最新发布的研究结果涵盖了从疗效预测标志物到不同诊断时间、基线肾功能水平患者的疗效评估,以及长期治疗的可持续性分析,特别是对作用机制和安全性的探讨。研究表明,耐赋康®对不同eGFR基线和确诊时间的IgA肾病患者均具有显著的肾脏保护作用。此次会上公布的耐赋康®多项最新研究结果显示,在疾病早期使用耐赋康®可使患者获得更显著的肾功能保护和延缓疾病进展,为IgA肾病尽早开启源头干预提供了有力依据,为患者带来了更科学的治疗方案和更好的生活质量。
-
2025年8月,公司宣布耐赋康®扩大产能补充申请已获得中国国家药品监督管理局批准。此次扩产获批将进一步提升耐赋康®产能,增加产品供应,更高效地响应中国及亚洲地区对耐赋康®的持续增长的临床需求。
-
2025年8月,公司宣布中国台湾地区药政部门已批准耐赋康®的补充申请,适用于罹患原发性IgA肾病且病情有进展风险的成人病人,用以减缓肾功能下降。此前,耐赋康®已在中国大陆、新加坡、中国香港、中国澳门和韩国获得完全批准。至此,耐赋康®已在云顶新耀覆盖的所有授权区域实现完全批准,巩固了其在亚洲作为IgA肾病一线治疗基石的地位,推动IgA肾病治疗的标准化与规范化进程。
-
2025年9月,耐赋康®在第18届IgA肾病国际研讨会(IIgANN)盛会中展示了7项最新真实世界数据,进一步展现其在相关领域的深入研究进展。此次公布的最新数据来自中国多家顶尖医院的临床实践,从多个维度深入探讨了耐赋康®在IgA肾病治疗中的疗效与安全性,进一步支持“对因治疗、尽早治疗、长期治疗”的IgA肾病管理策略。
-
2025年9月,耐赋康®被纳入由改善全球肾脏病预后组织(KDIGO)发布的《2025 KDIGO IgA肾病和IgA血管炎临床管理实践指南》,推荐对所有有肾功能进行性衰退风险的IgA肾病患者进行9个月的耐赋康®治疗,明确其一线用药地位。指南同时也强调单次9个月的疗程可能不足以在长期降低蛋白尿和稳定估算肾小球滤过率(eGFR)方面维持持续的临床获益,因此需要延长治疗时间。
-
2025年10月,耐赋康®被纳入《中国成人IgA肾病及IgA血管炎肾炎临床实践指南(2025)》。新版指南推荐对有疾病进展风险的 IgA肾病患者进行9个月的耐赋康®对因治疗,以降低致病性IgA(Gd-IgA1)。耐赋康®是唯一获得新版指南推荐的已获批用于IgA肾病对因治疗的药物。这是耐赋康®继日前获改善全球肾脏病预后组织(KDIGO)指南推荐之后,再度获得重磅推荐,成为全球唯一同时获得国际与国内指南推荐的IgA肾病对因治疗药物。
-
2025年11月,在第58届美国肾脏病协会肾脏周(ASN Kidney Week 2025)上,耐赋康®展示了多项关于IgA肾病患者的最新研究结果。随着耐赋康®在中国人群中证据的不断积累,这些研究结果进一步证实了在“对因治疗、尽早治疗、长期治疗”IgA肾病新管理策略中的显著临床价值;耐赋康®对特殊人群的疗效也得到验证,巩固了其IgA肾病一线治疗的基石地位。
-
2025年12月,在第23届亚太肾脏病学大会(APCN 2025)上,耐赋康®共展示了11项最新研究成果,进一步丰富了耐赋康®在临床应用方面的证据。此外,在耐赋康®进入医保后,随着使用治疗时间的积累,临床医生逐步将目光从“蛋白尿的改善”移向“肾功能的保护”,以期为IgA肾病患者的长期管理提供重要参考。
2026
-
公司计划于2026年获得Gd-IgA1检测试剂的注册申请批准,旨在为IgA肾病患者提供一种无需活检即可辅助疾病诊断并追踪病程进展的检测方法。
EVER001(希布替尼)
EVER001(希布替尼)是新一代创新性的共价可逆BTK抑制剂,潜在用于治疗包括原发性膜性肾病、IgA肾病、微小病变性肾病、局灶节段性肾小球硬化和狼疮性肾炎等肾脏疾病在内的自身免疫性肾病。与共价不可逆BTK抑制剂相比,EVER001作为一款潜在的同类最佳产品,在保持高活性的同时具有高选择性,避免持续抑制带来的毒副作用。云顶新耀拥有这款产品用于肾病治疗的全球权益。
2025
-
2025年6月,云顶新耀在第62届欧洲肾脏协会(ERA 2025)大会上公布 EVER001在中国正在进行中的1b/2a期临床试验的积极结果,包括截至2024年12月17日收集到的更多患者的更长期数据。其中低剂量组10位患者随访至52周,高剂量组10位患者完成了24周治疗。相对于基线,抗-PLA2R自身抗体最小二乘法(LS)几何平均值在12周时低剂量组和高剂量组分别下降62.1%和87.3%,而在24周时两组降幅均增至93%左右。此外,低剂量组在36周蛋白尿水平较基线下降78.0%并于停药后维持到第52周;高剂量组在24周即出现蛋白尿70.1%的下降,其中80.0%的患者已达到临床缓解。两个剂量组的患者在治疗期间均保持了肾功能的稳定。EVER001临床总体安全性和耐受性良好,未观察到在其他共价非可逆BTK抑制剂上常见的一些有临床意义的不良事件。
-
2025年7月,云顶新耀宣布正在进行中的EVER001的1b/2a期临床试验最新阶段性数据取得积极结果,收集到的数据截至2025年3月21日,(低剂量组11位患者随访至52周,高剂量组分别有16位和12位患者完成了24周和36周治疗,并有7位患者随访至52周)。相对于基线,抗-PLA2R自身抗体最小二乘法(LS)几何平均值在12周时低剂量组和高剂量组分别下降62.1%和87.3%,在24周时两组降幅均增至93%以上,并维持到第52周。24周时,76.9%的低剂量组和88.2%的高剂量组患者已达到免疫学完全缓解。24小时蛋白尿LS几何平均值,在24周时低剂量组和高剂量组分别下降57.0%和67.6%,36周时降幅分别增至76.7% 和80.6%,并维持到第52周。与此前观察结果一致,24周时,38.5%的低剂量组患者和70.6%的高剂量组患者达到临床缓解,而在36周时这一比例进一步上升至69.2%和91.7%。两个剂量组的患者在治疗期间的平均血清白蛋白水平均达到了正常范围,同时保持了肾功能的稳定。总体而言,EVER001安全性和耐受性良好,与此前观察结果一致。绝大部分报告的不良事件均为1级或2级,未观察到在其他共价非可逆BTK抑制剂上常见的有临床意义的不良事件。
2026
-
公司计划将在2026年上半年的国际医学会议上公布EVER001的1b/2a期详细的临床研究数据。
-
公司计划将于2026年开展评估EVER001针对多种适应症的II期篮式试验。
MT1013
-
MT1013是一款全球首创的双靶点受体激动剂多肽,可同时靶向钙敏感受体(CaSR)及成骨生长肽(OGP)受体,开发主要用于治疗继发性甲状旁腺功能亢进症(SHPT)。云顶新耀于2026年2月与麦科奥特签署独家商业化许可协议,获得MT1013在中国及亚太区(日本除外)的独家商业化授权。此次合作将与云顶新耀现有肾科管线形成协同效应,强化产品布局,将产品覆盖从IgA肾病拓展至更广泛的慢性肾脏病领域,巩固公司在亚洲肾脏及自身免疫疾病领域的领导地位。数据显示,全球CKD患者人数已由2019年的9.1亿人增至2024年的10.7亿人,预计2030年将超12亿人,2035年将超15亿人;同期全球SHPT患者人数亦持续增长,预计2030年将达约1.9亿人,2035年将达约2.2亿人,临床需求亟待满足。
-
MT1013的III期临床试验已在全国范围内启动超过100家研究中心,计划招募约424名患者,主要针对慢性肾脏病维持性血液透析伴SHPT的患者群体(相关研发费用将由麦科奥特承担)。
-自身免疫性疾病管线-
维适平®(精氨酸艾曲莫德片, VELSIPITY®)
维适平®(精氨酸艾曲莫德片, VELSIPITY®)(VELSIPITY®,etrasimod)是一种每日一次口服的高选择性鞘氨醇-1-磷酸(S1P)受体调节剂,采用优化的药理学设计,与S1P受体1、4和5结合。维适平®目前已在美国、欧盟、加拿大、日本、澳大利亚、新加坡、英国、瑞士、以色列、大中华区等多个国家和地区获得新药上市批准。
2025
-
2025年2月,艾曲莫德的亚洲多中心III期临床研究的完整维持期数据,在第20届欧洲克罗恩病和结肠炎组织大会(ECCO 2025)上以口头报告形式公布。艾曲莫德是迄今为止在亚洲中重度活动性UC人群中唯一完成大样本随机对照关键性研究的UC先进疗法。ES101002研究结果为艾曲莫德在亚洲中重度活动性UC患者中的应用提供了强有力的证据支持。数据证实,经过40周的维持治疗后,艾曲莫德组具有显著的临床和内镜学方面的获益,包括黏膜愈合、内镜正常化和组织学改善。艾曲莫德安全性数据与已知特征一致,没有观察到新的安全性信号。
-
2025年3月,艾曲莫德位于嘉善工厂的生产建设项目正式启动。该项目总投资为7000万元,预计正式投产后艾曲莫德的年产能可达5000万片,计划供应地区覆盖云顶新耀授权区域。
-
2025年4月,中国香港卫生署正式批准艾曲莫德用于治疗中重度活动性溃疡性结肠炎成人患者的新药上市许可申请。
-
2025年6月,韩国食品药品安全部(MFDS)正式受理艾曲莫德用于治疗中重度活动性溃疡性结肠炎(UC)患者的新药上市许可申请。
-
2025年7月,艾曲莫德治疗中重度活动性溃疡性结肠炎患者的全球4年安全性随访数据在第13届亚洲炎症性肠病协会(AOCC 2025)年会上公布。数据显示,艾曲莫德长期治疗仍能保持良好的安全性和耐受性,其良好的安全性特征在长期治疗期间未发生改变。
-
2025年8月,中国台湾卫生福利部(TFDA)正式受理艾曲莫德用于治疗中重度活动性溃疡性结肠炎患者的新药上市许可申请。艾曲莫德获韩国和中国台湾受理,标志着继中国澳门、新加坡和中国香港获批之后,其在亚洲市场的准入取得重要进展。
-
2025年8月,艾曲莫德被纳入《2025 ACG 临床指南:成人溃疡性结肠炎》。新版指南强烈推荐将艾曲莫德用于中重度活动性溃疡性结肠炎患者的诱导缓解治疗(中等质量证据),并推荐在经鞘氨醇-1 -磷酸 (S1P) 受体调节剂诱导缓解后继续使用艾曲莫德以维持缓解(强烈推荐,中等质量证据)。这一重要进展不仅体现了国际权威医学指南对艾曲莫德临床价值的高度认可,也进一步彰显了其在满足UC患者未被满足的治疗需求方面的潜力,为全球UC患者提供新的治疗选择。
-
2025年9月,艾曲莫德的亚洲多中心Ⅲ期临床ENLIGHT UC研究(ES101002)结果发表在国际顶级期刊柳叶刀子刊《The Lancet Gastroenterology & Hepatology》(中文名称:《柳叶刀胃肠病学和肝病学》)。研究显示,艾曲莫德在快速起效、实现无激素缓解和深度黏膜愈合方面具有显着临床优势,为包括中国患者在内的亚洲UC患者提供坚实的临床证据支援。
2026
-
2026年2月,中国国家药品监督管理局(NMPA)批准维适平®(精氨酸艾曲莫德片, VELSIPITY®)的新药上市许可申请,用于治疗对传统治疗或生物制剂应答不充分、失应答或不耐受的中度至重度活动性溃疡性结肠炎成人患者。作为新一代高选择性S1P受体调节剂,维适平®每日一次口服,可实现快速起效和强效深度黏膜愈合,并具有良好的安全性特征,具备最佳药物(best-in-disease)潜质,为成人溃疡性结肠炎患者提供新的一线治疗选择。
-
2026年3月,维适平®中国大陆首张处方于中山大学附属第一医院开出,标志着该创新疗法正式进入中国临床应用阶段,为中重度溃疡性结肠炎患者提供了创新治疗选择,开启深度黏膜愈合与长期疾病控制的全新治疗篇章。
-
公司预计艾曲莫德将于2026年在中国台湾和韩国获得新药上市批准。
公司计划于2026年下半年参加维适平®的国家医保谈判。
-心血管/代谢产品管线-
2025年12月,公司通过与海森生物制药的战略合作进入全新的心血管╱代谢疾病领域,包括通过商业化服务协议(CSO)代理成熟的商业化产品(易达比®、必洛斯®、倍欣®),以及授权引进在大中华区开发与商业化新一代PCSK9抑制剂乐瑞泊®。该合作将充分利用公司现有的商业化平台,建立全生命周期、全管道的商业化能力并为高潜治疗领域建立基础性产品布局。2026年3月,公司授权引进艾曲帕米(Etripamil)鼻喷雾剂(拟定中文商品名:星必妥®)在大中华区的开发、商业化及产品地产化权益,进一步深化心血管领域战略布局。
乐瑞泊®
乐瑞泊®是一款新型小分子蛋白结合的第三代PCSK9抑制剂,旨在帮助患者达成并长期维持其 LDL-C 控制目标。作为首个PCSK9抑制剂融合蛋白,乐瑞泊®免疫原性低,安全性出众。乐瑞泊®经开发为更贴近患者需求、更加便捷,可由患者自行给药、每月一针、单次小体积皮下注射,并具有较长的室温稳定性(最长可达3个月),可使患者自行选择时间和地点用药,居家旅行皆可方便储存或携带。以上特点使乐瑞泊®成为已获批的PCSK9抑·代方案。在总计超过2,900例患者入组的多项全球大型3期临床试验中,结果显示,乐瑞泊®可使心血管疾病 (CVD) 患者或极高/高风险族群的LDL-C持续降低≥60%,并使LDL-C升幅更严重的HeFH患者降低59%。
2025
-
2025年12月,美国食品药品监督管理局(FDA)已批准LIB Therapeutics旗下心血管疾病领域产品乐瑞泊®注射液的生物制品许可申请(BLA),在饮食控制和运动的基础上,用于降低成人高胆固醇血症(包括杂合子型家族性高胆固醇血症(HeFH))患者的低密度脂蛋白胆固醇(LDL-C)水平。乐瑞泊®在中国用于治疗高胆固醇血症(包括HeFH)患者的关键注册性3期临床试验,目前已完成为期12周的随机、双盲、安慰剂对照治疗阶段的数据分析,已达到第12周 LDL-C 降低的主要疗效终点,并达到其他致动脉粥样硬化脂质及载脂蛋白改善的次要疗效终点,与安慰剂相比显示出良好的安全性和耐受性特征。
2026
-
我们预计于2026年上半年递交中国生物制品许可申请(BLA)。
艾曲帕米鼻喷雾剂
艾曲帕米鼻喷雾剂是Milestone Pharmaceuticals, Inc.研发的新型的钙通道阻滞剂,旨在为发作性心血管疾病患者提供一种快速起效的疗法。作为一种由患者自行给药的鼻喷雾剂,艾曲帕米鼻喷雾剂具有改变当前患者治疗体验的潜力,从急诊治疗转为院外治疗。2021年5月,箕星和Milestone达成独家许可协议,获得在大中华区开发和商业化在研药物艾曲帕米鼻喷雾剂(拟定使用的中文商品名:星必妥®)治疗PSVT和其它心血管疾病的独家权限。该药物于2025年12月获得美国食品药品监督管理局(FDA)批准,成为30多年来首款且唯一获批用于成人阵发性室上性心动过速(PSVT)急性症状性发作的疗法,开拓了PSVT治疗新场景。
2026
-
2026年3月,公司宣布与箕星药业香港有限公司达成资产收购协议,获得艾曲帕米(Etripamil)鼻喷雾剂在大中华区的开发、商业化及产品地产化权益。艾曲帕米鼻喷雾剂用于治疗PSVT的新药上市申请已于2025年1月17日获中国国家药品监督管理局正式受理,并预计于2026年第三季度获批,有望为PSVT患者提供全新的治疗选择。此次合作是公司深化心血管领域战略布局的重要举措,进一步丰富了公司的产品管线、增强协同效应,持续巩固公司在心血管疾病领域的发展。
-急重症产品管线-
在与海森生物达成战略合作后,公司拓展了急重症产品组合,进一步利用其高效、卓越的商业化平台,加强了在该领域的布局。在抗感染领域,产品组合包括依嘉®、罗氏芬®(头孢曲松)及头孢吡肟-坦尼硼巴坦,可覆盖从社区获得性感染的轻中度感染人群到院内获得性感染的中重度感染人群。依嘉®是公司抗感染领域的核心产品,常用于ICU、移植科、血液科等多重耐药菌感染所致的的重症患者治疗,与常用于社区获得性感染治疗药物罗氏芬®在呼吸科,儿科及神经外科,神经内科的覆盖优势形成互补。而罗氏芬®作为被临床广泛认可的第三代头孢菌素,已被纳入中国国家基本药物目录。急重症产品组合还包括思他宁®(生长抑素,用于急性胃肠道出血管理)和亚宁定®(用于快速血压控制),均为急重症患者提供有效治疗。
依嘉®(依拉环素)
依嘉®(依拉环素)是全球首个氟环素类抗菌药物,用于治疗临床常见致病菌包括革兰阴性菌、革兰阳性菌、厌氧菌、非典型病原体以及多重耐药菌引起的感染。依嘉®目前已在美国、欧盟、英国、新加坡、中国大陆、中国香港和中国台湾地区被批准用于治疗复杂性腹腔内感染(cIAI)。依嘉®是公司从Tetraphase制药公司(为Innoviva, Inc.的全资子公司)授权引进。
2025
-
2025年6月,《中华检验医学杂志》正式发表《依拉环素体外药物敏感性试验规范(2025)》,为规范开展依拉环素体外药敏试验和结果解读提供参考,以期“有据可依”地指导临床合理用药; 同时也有助于促进临床微生物学实验室对依拉环素药敏试验作方法的规范性和结果报告的准确性,“有依可靠”地支持依拉环素应对临床多重耐药菌感染和复杂感染的挑战。该规范由国家卫生健康委临床抗微生物药物敏感性折点研究和标准制定专家委员会(ChinaCAST)、中国医院协会临床微生物实验室专业委员会、欧洲临床微生物与感染病学会药敏委员会华人药敏试验委员会共同制定。此次发布的规范与2024年ChinaCAST发布的依拉环素中国临床折点相辅相成,形成“标尺合一”的完整技术体系。
2026
-
公司计划参加2026年下半年的国家医保谈判并积极推进本地化生产。
-眼科产品-
VIS-101
云顶新耀通过从新桥生物附属公司Visara引进产品VIS-101将其研发管线拓展至眼科领域。VIS-101是一种新型双功能生物制剂,靶向VEGF-A和ANG-2,其疗效较第一代治疗更为显着,可有望为湿性年龄相关性黄斑部病变(wet AMD)、糖尿病性黄斑部水肿(DME)及视网膜静脉阻塞(RVO)患者提供更持久的治疗效益。VIS-101进一步丰富了公司的后期产品管线,并将业务拓展至眼科这一临床需求尚未充分满足且具有创新机会的蓝海治疗领域,利用其在大中华区及部分亚洲市场临床开发经验和商业化能力为公司发展注入新的增长动能。VIS-101已在美国和中国完成初步安全性及剂量递增研究,目前正在中国进行随机分组的剂量范围II期临床试验。
2025
-
2025年10月,公司宣布已与Visara, Inc. 签订协议,获得独家许可,在大中华区、新加坡、韩国及若干东南亚国家进行临床开发、生产和商业化VIS-101。根据指定独家许可,云顶将支付700万美元(相当于约人民币4,970万元)的预付款,及不超过人民币2,400万元的自付费用报销;最高不超过8,900万美元(相当于约人民币6.32亿元)的潜在开发及销售里程碑款项;以及按净销售额的潜在特许权使用费。
2026
-
2026年3月,在研眼科管线VIS-101治疗湿性年龄相关性黄斑变性(湿性AMD)的IIa期研究取得积极顶线数据。数据显示,VIS-101展示出起效迅速、强效持久的治疗反应,及良好的安全性及耐受性,并验证了其作为潜在“同类最佳”持久性的临床价值。基于积极的临床数据,预计将于2026年下半年启动IIb期临床研究。
-mRNA技术平台-
作为公司“双轮驱动”战略的重要组成部分,云顶新耀已构建业内领先的、完全整合且本地化的AI+mRNA平台,并在此基础上多路径推进mRNA肿瘤治疗性疫苗和自体生成CAR-T管线平台,治疗肿瘤及自身免疫疾病。
EVM16基于AI驱动的“妙算”肿瘤新抗原算法,针对患者特异性突变设计mRNA序列,通过LNP递送激活T细胞免疫,已在小鼠黑色素瘤模型中验证疗效并展现与PD-1抗体联用具有协同作用。EVM14靶向5种肿瘤相关抗原,适用于多种鳞癌,临床前研究发现其具备诱导免疫记忆、降低肿瘤复发的潜力,2025年成功实现中国国家药品监督管理局(NMPA)和美国食品药品监督管理局(FDA)IND双获批。免疫调节肿瘤疫苗EVM15亦于2025年取得临床前概念验证,确定临床候选分子。
自体生成CAR-T平台也已在人源化小鼠与非人灵长类(猴)模型中验证有效,相较传统CAR-T疗法具备现货型、无需淋巴耗竭、剂量可控等优势,展现了开发用于肿瘤及自身免疫疾病的潜力,体现公司从“授权引进”向“自主创新”的转型升级。目前已确定临床候选分子并将启动临床试验。
2025
-
2025年3月,公司宣布自主研发的首款新型mRNA个性化肿瘤治疗性疫苗EVM16已在北京大学肿瘤医院顺利完成首例患者给药,标志着此项临床试验项目的里程碑进展。临床试验项目EVM16CX01是EVM16开展的首次人体试验,由北京大学肿瘤医院和复旦大学附属肿瘤医院发起,用于评估EVM16注射液单药及联合PD-1抗体治疗在晚期或复发实体瘤受试者的安全性、耐受性、免疫原性和初步疗效的剂量递增及扩展研究。
-
2025年3月,公司宣布其通用型的现货肿瘤治疗性疫苗EVM14注射液的新药临床试验申请(IND)获美国食品药品监督监督管理局(FDA)的批准。EVM14注射液是基于云顶新耀自主知识产权的mRNA技术平台研发。作为公司首个获得FDA IND批准的自主研发新药,EVM14标志着公司在mRNA肿瘤领域的创新实力获得国际权威机构的认可,是公司自主研发历程中的重要里程碑。
-
2025年6月,公司宣布其嘉善工厂已顺利完成通用型的现货肿瘤治疗性疫苗EVM14项目首批临床样品的放行。该批样品将用于支持云顶新耀在中美两地开展EVM14的临床试验。
-
2025年6月,公司成功举办“2025云顶新耀mRNA创新技术平台研发日”,系统集中展示了云顶新耀自主研发的AI+mRNA技术平台的最新进展,以及基于该平台开发的肿瘤及自身免疫疾病领域核心管线,标志着“双轮驱动”战略的进一步深化与升级。
-
2025年7月,通用型现货肿瘤治疗性疫苗EVM14注射液的新药临床试验申请获国家药品监督管理局药品审评中心(CDE)的正式受理。EVM14成为公司首个实现“中国国家药品监督管理局和美国食品药品监督管理局(FDA)双报”的mRNA肿瘤治疗性疫苗,标志着公司在全球创新布局上又迈出关键一步。
-
2025年10月,通用现货型肿瘤治疗性疫苗EVM14注射液的新药临床试验申请获国家药品监督管理局批准。EVM14成为公司首个实现中国国家药品监督管理局和美国食品药品监督管理局IND双获批的mRNA肿瘤治疗性疫苗。这一成果不仅标志着EVM14具备全球临床开发与转化的潜力,更展现出公司在全球临床开发与创新实力上的持续提升,是公司自主研发历程中的重要里程碑。
-
2025年10月,通用现货型肿瘤治疗性疫苗EVM14注射液的全球多中心I期临床试验在美国临床研究机构NEXT Oncology Virginia成功入组首例患者。这是继EVM14新药临床试验申请在美国食品药品监督管理局和中国国家药品监督管理局均获批准后的一项重要临床进展。
-
2025年11月,通用现货型肿瘤治疗性疫苗EVM14注射液的全球多中心I期临床试验已在美国临床研究机构NEXT Oncology Virginia完成首例患者给药,标志着其全球临床开发进程取得重要里程碑。
2026
-
公司预计2026年上半年,在国际医学会议上公布EVM16 IIT 研究的1a期数据。该试验已完成低、中、高剂量组的剂量爬坡。我们计划在2026年启动IIT 1b期试验,以进一步推进临床开发。
-
公司计划于2026年,通过多项研究者发起的临床试验(IITs),在多项自身免疫性疾病适应症中对EVM18进行临床评估,并力争在2026年递交全球新药临床试验申请。
-
公司预计于2026年完成EVM14 1期临床试验的剂量爬坡。
-
公司计划在2026年推进EVM15的新药临床试验申请准备工作。
产品管线
本公司通过授权引进与自主研发,已在CKM(心血管、肾脏及代谢)、自身免疫、眼科、急重症等疾病领域和mRNA平台上建立了丰富的产品管线组合,包括疾病首创或同类最佳资产,预计将为公司带来显着的收入增长,并为股东创造价值。
下表概列截至最后实际可行日期,我们的主要产品管线及各候选药物的开发状况:
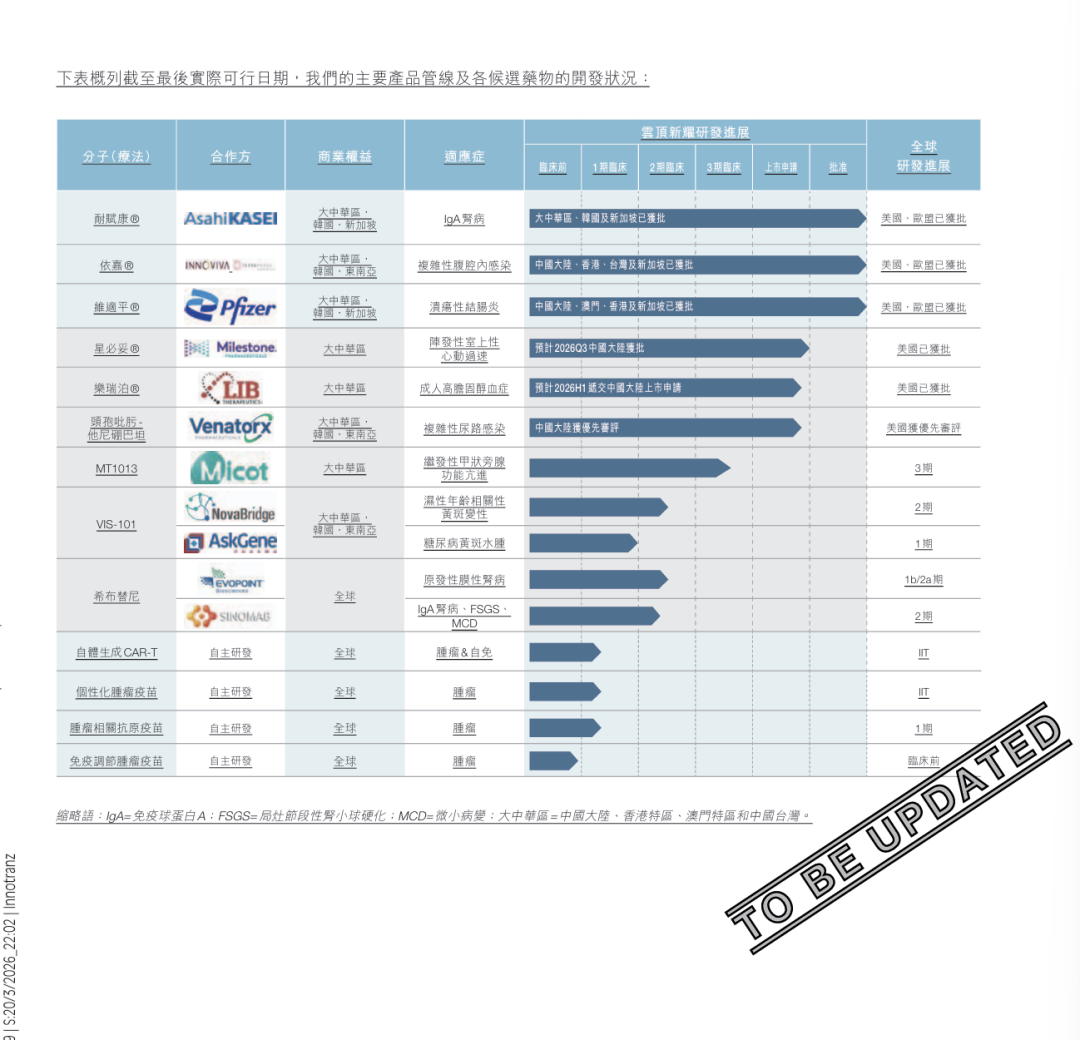
管线进展与展望
2025年,我们在多个治疗领域持续深化研发管线布局,显着拓宽了公司产品组合的覆盖范围。
在肾病领域,耐赋康®去年在包括大中华区、韩国在内的云顶全部授权区域均获得完全批准,实现了重要的里程碑,进一步印证了其卓越的临床价值,巩固了耐赋康®在亚洲作为IgA肾病一线对因治疗的领先地位。
在自身免疫性疾病领域,维适平®同样在去年实现一系列重要注册里程碑,先后在中国香港获得新药上市申请批准,并在韩国和中国台湾递交NDA,这些进展将加速维适平®在亚洲市场的持续拓展。最为重磅的是,2026年2月,维适平®获得中国国家药品监督管理局批准,用于治疗中重度活动性溃疡性结肠炎,这标志着公司在自身免疫疾病领域开启了商业化新篇章。
在我们临床阶段的肾病产品组合中,希布替尼(EVER001)用于膜性肾病的1b/2a期临床试验持续取得进展,其积极的疗效和安全性数据表明该药物在自身免疫介导的肾病领域具有广泛潜力。因此,我们计划在2026年上半年开启一项评估希布替尼在IgA肾病、局灶节段性肾小球硬化(FSGS)及微小病变肾病(MCD)等多种适应症疗效和安全性的II期篮式试验。
2025年,我们通过积极的授权引进进一步扩大了后期管线,在眼科、心血管疾病等领域新增多项资产,其中包括引进了眼科新型双功能生物制剂VIS-101,其在治疗湿性年龄相关性黄斑变性的IIa期研究中取得积极顶线数据,展示出起效迅速、强效持久的治疗反应及良好的安全性及耐受性,并验证了在给药周期上潜在的“同类最佳”临床价值。我们预计将在2026年推进VIS-101下一阶段临床开发的准备工作。
2025年12月,云顶的授权合作伙伴LIB Therapeutics获得美国食品药品监督管理局批准,其第三代PCSK9抑制剂LEROCHOL™可用于降低成人高胆固醇血症(包括杂合子型家族性高胆固醇血症(HeFH))患者的低密度脂蛋白胆固醇(LDL-C)水准。云顶计划于2026年上半年在大中华区提交LEROCHOL™的生物制品许可申请(BLA)。
2026年3月,本公司获得艾曲帕米(Etripamil)鼻喷雾剂在大中华区的开发、商业化及产品地产化权益。它是美国30多年来首款且唯一获批用于成人阵发性室上性心动过速(PSVT)急性症状性发作的疗法,而在中国,艾曲帕米鼻喷雾剂用于治疗PSVT的新药上市申请已于2025年1月获中国国家药品监督管理局正式受理,并预计于2026年第三季度获批。
在我们内部开发的mRNA平台管线中,个性化肿瘤疫苗EVM16去年完成了IIT Part 1a期的低、中、高剂量爬坡。针对我们的通用型肿瘤相关抗原(TAA)疫苗EVM14,我们分别在2025年3月和8月获得了美国FDA和中国CDE的新药临床试验批准,这标志着云顶首次在美中两国同时获得IND批准。我们还于2025年11月完成了美国首例患者给药。此外,mRNA自体生成CAR-T项目EVM18已于2025年确定临床候选分子并积极推进临床开发。
商业化平台
通过授权引进,云顶聚焦CKM(心血管、肾脏及代谢)、自身免疫、急重症等疾病治疗领域,已打造集全渠道商业化体系与药品全生命周期商业化能力于一体的商业化平台。目前,我们的商业化产品组合包括耐赋康®、依嘉®和维适平®。这三款产品均具备优异的临床特征,填补亚洲巨大未满足需求,拥有可观的长期收入潜力。同时,通过与海森生物的战略合作,云顶将为其六款成熟的急重症和心血管/代谢产品提供CSO服务,强化对现有商业化平台的高效利用。
耐赋康®
自2025年1月1日正式纳入中国国家医保药品目录以来,耐赋康®销售收入实现显着增长,并成为首个在进入国家医保目录后首年收入即突破10亿元的非肿瘤药物。这一成绩充分体现了公司在市场准入、市场策略、商业化覆盖与医患教育等关键环节的高效执行力。
2025年期间,我们通过一支约190名代表组成专业一线销售团队,将耐赋康®的覆盖范围扩展至约1200家核心医院,占市场潜力的80%以上。我们通过医院正式准入或双通道药房模式,快速推进医保落地,截至年中主要核心区域均完成耐赋康®医保价格覆盖,大幅提升了患者的可负担性与药物可及性。去年8月,中国国家药品监督管理局正式批准耐赋康®的扩产补充申请,有效保障产品供应,这为2025年下半年大幅的销售增长以及2026年的持续放量铺平道路。
临床应用推广获得了由改善全球肾脏病预后组织(KDIGO)发布的2025年IgA肾病临床实践指南和中国首部IgA肾病指南正式发布的双重助力。《2025 KDIGO IgA肾病和IgA血管炎临床管理实践指南》及《中国成人IgA肾病及IgA血管炎肾炎临床实践指南(2025)》均把耐赋康®列为首选对因治疗药物,耐赋康®成为目前全球唯一同时获得国际与国内指南推荐的IgA肾病对因治疗药物。指南推荐对有疾病进展风险的IgA肾病患者进行9个月的布地奈德肠溶胶囊对因治疗,不受蛋白尿水平的限制,以降低致病性IgA(Gd-IgA1);达到短期治疗目标后,即蛋白尿缓解(蛋白尿<0.5 g/d,理想情况<0.3 g/d)及肾功能稳定,可以采取小剂量维持或重复安全有效的免疫治疗和继续维持支持治疗,以保证eGFR每年下降<1 ml/min/1.73 m2。在耐赋康®全球III期研究、亚组分析及不断扩充的真实世界研究数据的支持下,我们制定了针对IgA肾病的市场及疾病管理策略,即“对因治疗、尽早治疗、长期治疗”。这些举措进一步提升了医生对耐赋康®作为IgA肾病一线基石疗法的认可,为其在临床实践中更早、更广泛地应用提供了坚实支援。
此外,40余篇关于耐赋康®的论文在权威医学期刊上发表,包括以下五篇全文发表:北京大学第一医院肾内科吕继成教授等发表的《布地奈德肠溶胶囊在IgA肾病中的免疫调节作用和研究进展》和《靶向释放布地奈德肠溶胶囊治疗IgA肾病时Gd-IgA1与多聚IgA发挥的预测价值研究》,长征医院肾脏病科毛志国教授等发表的《靶向释放布地奈德(TRF-budesonide)治疗IgA肾病的有效性与安全性:一项Meta分析》,中山大学附属第一医院肾内科陈崴教授等发表的《IgA肾病诊疗新进展》以及上海交通大学医学院附属瑞金医院肾脏科主任谢静远教授等发表的《布地奈德靶向释放制剂治疗伴严重肾功能损害的IgA肾病》。
依嘉®
在抗感染产品管线中,我们持续推动了依嘉®(依拉环素)在300家左右核心医院的渗透,特别是在具有较高市场潜力的医院中,来自于ICU及血液科等其他科室的患者需求稳步增长。与此同时,我们进一步优化了合同销售组织(CSO)模式,以扩展在非核心市场的覆盖。《依拉环素体外药物敏感性试验规范(2025)》在《中华检验医学杂志》正式发表后,依拉环素的中国折点也获CDE批准并更新进说明书,为检验科微生物室规范开展依拉环素体外药敏试验和结果解读提供参考,以期“有据可依”地指导临床合理用药。去年,依拉环素在国内外医学期刊上发表20余篇专业文章,并被纳入《血液肿瘤患者碳青霉烯类耐药肠杆菌科细菌(CRE)感染的诊治与防控中国专家共识(2025 年版)》、《高毒力碳青霉烯类耐药肺炎克雷伯菌感染诊治与防控专家共识》、《复杂性腹腔感染碳青霉烯类耐药细菌诊治专家共识(2025版)》等多部指南共识,为促进该产品更广泛地合理应用提供了支援证据。
维适平®
2025年,我们持续推进维适平®在中国大陆正式获批上市前的准备工作。去年,该药物在“港澳药械通”政策下于广东省12家医疗机构为患者提供了早期临床使用机会,这为2026年2月获得中国国家药品监督管理局的新药上市批准打下良好的医生和患者基础。我们同时在大湾区启动了真实世界研究,旨在积累更多循证依据,以指导临床实践。
继2024年12月,艾曲莫德被纳入美国胃肠病协会(AGA)临床实践指南,去年6月又被纳入《2025 ACG 临床指南:成人溃疡性结肠炎》,新版指南强烈推荐将艾曲莫德用于中重度活动性溃疡性结肠炎患者的诱导缓解治疗(中等质量证据),并推荐在经鞘氨醇-1 -磷酸 (S1P) 受体调节剂诱导缓解后继续使用艾曲莫德以维持缓解(强烈推荐,中等质量证据)。此次新版指南是由美国胃肠病学会(American College of Gastroenterology)制定,基于近五年来最新的循证医学证据,系统总结了溃疡性结肠炎在治疗和并发症预防方面的新方法与新进展,旨在为临床医生提供更规范、科学的管理参考。这一重要进展体现了国际权威医学指南对艾曲莫德临床价值的高度认可。
此外,4篇关于艾曲莫德的文章在国内外医学期刊上发表,其中艾曲莫德在亚洲中重度活动性溃疡性结肠炎患者中的多中心Ⅲ期临床ENLIGHT UC研究结果2025年9月发表于国际权威期刊《柳叶刀胃肠病学和肝病学》,其疗效与安全性获得全球顶级学术期刊认可。
为加强长期供应稳定性及高毛利水平,我们去年在嘉善生产基地启动了本地化生产项目,总投资额达人民币7000万元,全面投产后年产能预计可达500万瓶。
2025年12月,云顶于海森生物达成战略合作协议,其中包含为海森生物旗下急重症、心血管及代谢三大治疗领域的六款已获批并商业化上市的产品提供商业化服务。这六款产品为:急重症领域的罗氏芬®(Ceftriaxone)、思他宁®(Somatostatin)、亚宁定®(Urapidil);心血管领域的易达比®(Azilsartan)、必洛斯®(Candesartan)以及代谢领域的倍欣®(Voglibose)。云顶将按相关产品季度净销售总额的20%-55%收取服务费。
商业化展望
展望2026年,我们仍将专注于深化核心治疗领域的商业化执行,同时拓展市场准入,为产品管线的下一阶段增长打下坚实基础。
作为目前国家医保目录中唯一获批用于治疗IgA肾病的药物,耐赋康®预计将在2026年继续作为公司销售收入的核心增长引擎。借助进入国家医保目录后的快速放量势头,我们计划进一步拓展核心市场的覆盖,扩张内部销售团队规模。同时通过与CSO机构合作,加深下沉市场渗透,将覆盖范围进一步扩大至超过90%的可及市场。与此同时,我们将通过有效的医患教育和开展更多真实世界研究,进一步强化医生和患者对国内外指南的推荐以及我们“对因治疗、早期治疗、长期治疗”疾病管理策略的认知。
对于依嘉®,我们将扩大目标医院数量并深化在核心医院的渗透,持续扩大药敏常规开展,以及重症监护相关科室的拓面,如呼吸及外科重症监护室等。同时我们将持续积累不同感染部位真实世界证据,助力依嘉®成为多重耐药感染经验治疗的基石。此外,我们计划于2026年下半年参加国家医保药品目录谈判,并同步推进本地化生产布局,旨在使更多的中国患者获益的同时推动该产品迈入新的增长周期。
维适平®于2026年2月在中国大陆获得上市批准后,仅用21个工作日即实现中国大陆首张处方的成功落地,彰显我们将国际前沿创新疗法快速引入中国临床实践的执行力。近年来,中国溃疡性结肠炎发病率持续上升,并呈现年轻化趋势,预计患者人数将由2025年的约98万增长至2031年的约150万。而维适平®在临床研究中展现出快速、持久的临床缓解及深度黏膜愈合的卓越疗效和良好的安全性,并已获国际主流治疗指南的强烈推荐作为一线用药,同时还具有每日一次口服的便利性。我们相信,该产品有望成为继耐赋康®之后公司推出的又一个重磅产品。公司今年将为其上市投入核心的市场与医学资源,包括多渠道开展广泛的医生患者教育活动,持续开展真实世界研究,搭建一支专业高效的销售队伍,并积极筹备2026年下半年的国家医保目录谈判。同时,我们将积极推进本地化生产项目,预计将于明年投产。
除了我们自有的商业化产品管线,为海森生物旗下六款成熟产品提供商业化服务也将带来稳定的收入,尤其是罗氏芬®作为被临床广泛认可的第三代头孢菌素,已被纳入中国国家基本药物目录,其作为一款社区获得性感染治疗药物可与依嘉®的治疗院内重症感染形成互补与高效协同。
业务拓展
2025年12月,公司发布2030年发展战略,全面规划未来五年发展蓝图,将持续丰富产品管线,最大化创新药商业化平台价值。其中,战略指出,未来五年公司计划引进20个以上的高价值资产,为2030年贡献收入60亿,并探索潜在对外授权收入。在该战略的指引下,公司积极推动授权引进,拓展治疗领域覆盖广度,增强应对未来发展的长期韧性。
去年10月,公司与Visara, Inc.签订协定,获得独家许可,在大中华区、新加坡、韩国及若干东南亚国家进行临床开发、生产和商业化VIS–101,将业务拓展至眼科这一临床需求尚未充分满足且具有创新机会的蓝海治疗领域。VIS–101是一款新型双功能生物制剂,针对VEGF-A与ANG–2,其疗效较第一代治疗更为显着,可有望为湿性年龄相关性黄斑部病变(wet AMD)、糖尿病性黄斑部水肿(DME)及视网膜静脉阻塞(RVO)患者提供更持久的治疗效益。
去年12月,公司与海森生物达成多项战略协议,包括一项涵盖多款成熟产品的商业化服务协定,以及一项关于乐瑞泊®的大中华区独家授权合约。这项合作将提升公司现有商业化平台的高效利用,在心血管这一高潜力治疗领域建立起基础性产品布局,并为公司研发管线补充一款已临近注册里程碑的后期阶段候选药物。
2026年2月,云顶新耀与麦科奥特科技签订独家授权合约,获得在中国及亚太地区(日本除外)商业化MT1013的权益。MT1013为全球首创的双靶点受体激动剂多肽,可同时靶向钙敏感受体(CaSR)及成骨生长肽(OGP)受体,开发主要用于治疗继发性甲状旁腺功能亢进症。此次战略合作将与云顶新耀现有肾科管线形成协同效应,强化产品布局,巩固公司在亚洲肾脏及自身免疫疾病领域的领导地位,并将产品覆盖从IgA肾病拓展至更广泛的慢性肾脏病领域。
2026年3月,本公司宣布与箕星药业香港有限公司达成资产收购协议,获得艾曲帕米(Etripamil)鼻喷雾剂(拟定中文商品名:星必妥®)在大中华区的开发、商业化及产品地产化权益。此次合作是本公司深化心血管领域战略布局的重要举措,进一步丰富了公司的产品管线、增强协同效应,持续巩固公司在心血管疾病领域的发展。除了在美国获批用于成人阵发性室上性心动过速(PSVT)急性症状性发作的疗法,艾曲帕米鼻喷雾剂正开发用于伴有快速心室率反应的房颤(AFib-RVR)适应症。
展望2026年,云顶新耀将继续执行与其2030发展战略相一致的积极业务发展战略,坚定不移地推进创新药商业化平台建设,建设更丰富、多元化的商业化组合,为未来发展提供坚实保障。云顶新耀将继续聚焦其在核心治疗领域,包括CKM(心血管、肾脏及代谢)、自身免疫、急重症等疾病治疗领域,优先考虑处于临床后期阶段及临近商业化的产品,以提升现有商业化平台的高效利用和生产力;同时有选择性地拓展进入其他具有重磅潜力的高价值治疗领域。
在对外授权合作方面,云顶新耀将继续为具有全球权益的内部研发管线寻求全球合作伙伴机会,这包括已获得Ib/IIa期一年随访资料支援的EVER001(希布替尼),以及公司即将开启临床研究的mRNA自体生成CAR-T专案。公司相信,战略性全球合作能够加速临床开发、获批上市并提升长期价值创造。
凭借稳健的现金储备与持续的经营性现金流,云顶新耀已具备坚实基础,可稳步推进业务发展战略,不断拓展全球布局,从而打造一个多元化、具备全球竞争力并能实现可持续增长的创新药产品组合。
自主研发
2025年是云顶新耀双轮驱动战略及其自主研发的mRNA平台成果斐然的一年,公司在个性化及通用型mRNA肿瘤治疗性疫苗以及自体生成CAR-T项目上均取得重大进展,体现了公司在发现、转化、CMC及早期临床开发各环节的高效执行。
在我们内部开发的mRNA平台管线中,个性化肿瘤疫苗EVM16去年成功为9名患者完成给药,完成了IIT Part 1a期的低、中、高剂量爬坡。我们计划在2026年上半年于国际学术会议上公布该研究的资料结果,并于年内启动IIT的Part 1b期扩展研究。
针对我们的通用型肿瘤相关抗原(TAA)疫苗EVM14,我们分别在2025年3月和8月获得了美国FDA和中国CDE的新药临床试验批准,这标志着云顶首次在美中两国同时获得IND批准。公司在其嘉善生产基地成功完成并放行了EVM14的首个临床批次GMP生产,为全球临床开发提供了支援。同年11月,首位患者在美国完成给药,启动了EVM14在人体受试者中的临床评估。预计今年将完成包括美国和中国队列的低、中、高剂量爬坡。
云顶的自体生成mRNA CAR-T平台EVM18在2025年亦取得显着进展,完成临床前概念验证,确定临床候选分子并积极推进临床开发。今年,我们计划围绕多项自身免疫适应症启动多个IIT,同时积极推进全球新药临床试验申请递交工作,以开启系统性的临床评估。
财务亮点
国际财务报告准则数字
截至2025年12月31日止年度的收益为人民币1,706.7百万元,较截至2024年12月31日止年度的人民币706.7百万元大幅增加人民币1,000.0百万元或141.5%。收益增加主要由于耐赋康®在已商业化市场的销售额继续上升所致。
在中国市场,将耐赋康®纳入国家医保药品目录(「NRDL」)为关键的增长动力,导致截至2025年12月31日止年度的耐赋康®收益大幅增加。
在中国以外的市场,耐赋康®于台湾及韩国成功上市并实现重要里程碑,在其他亚洲市场的销售额亦继续上升。同时,VELSIPITY®于新加坡市场成功上市。该等成就突显本集团在扩展亚洲版图及提升患者用药可及性方面的进展。
毛利率由截至2024年12月31日止年度的74.6%减少至截至2025年12月31日止年度的69.3%。剔除无形资产摊销后,毛利率由截至2024年12月31日止年度的82.9%减少至截至2025年12月31日止年度的74.1%。有关减少主要由于耐赋康®于中国大陆纳入NRDL。
尽管如此,本集团继续透过流程改善及供应链精简等内部效率措施优化产品成本。此外,本公司与供应商通力合作(如联合降本计划)以实现规模经济。
截至2025年12月31日止年度的研发开支为人民币511.0百万元,较截至2024年12月31日止年度的人民币528.0百万元略有减少。本公司于年内成功实现多项研发里程碑,并一直积极优化其研发战略,以加速其体内CAR-T及mRNA平台的开发,迈向下一阶段研究及临床准备,并进一步释放EVER001(希布替尼)的价值。此外,凭藉其卓越的临床开发能力,本公司透过战略合作及授权引进项目进一步丰富其后期产品管线。
一般及行政开支由上年度的人民币250.1百万元增加人民币26.4百万元至截至2025年12月31日止年度的人民币276.5百万元。该增加主要由于员工人数增加,因本集团对人才获取进行战略性投资,以支持推进其管线开发及市场扩张计划。
分销及销售开支由截至2024年12月31日止年度的人民币508.1百万元增加人民币272.5百万元至截至2025年12月31日止年度的人民币780.6百万元。本公司积极扩大医疗机构的覆盖范围,并加强学术推广及医学教育活动。本集团致力于搭建全渠道商业化体系,并提升其于药品全生命周期的商业化能力。
经营开支总额(包括一般及行政开支、研发开支以及分销及销售开支)占收益的比率下降90.1个百分点,反映本集团的运营效率有所提升及资源配置更为聚焦。
年内亏损净额由截至2024年12月31日止年度的人民币1,041.4百万元减少人民币743.6百万元至截至2025年12月31日止年度的人民币297.8百万元。该减少主要由于(i)强劲的产品收益增长,(i)运营效率提升,(i)就新加坡产生的累计税项亏损确认递延税项资产,原因为认为未来很可能有足够的应课税利润以动用该等税项亏损,及(iv)与Zetomipzomib、SPR206及FGF401有关的无形资产产生的减值亏损人民币312.3百万元,而截至2024年12月31日止年度与mRNA COVID-19疫苗有关的减值亏损为人民币356.3百万元。
截至2025年12月31日,现金及现金等价物以及银行存款为人民币2,731.5百万元。
非国际财务报告准则计量
年内经调整利润/(亏损)由截至2024年12月31日止年度的亏损人民币537.6百万元转为截至2025年12月31日止年度的利润人民币187.2百万元,增加人民币724.7百万元,主要是剔除无形资产减值的一次性及非经常性亏损及联营公司投资产生的投资收益,以及以股份为基础的薪酬的非现金开支及无形资产摊销。
关于云顶新耀
云顶新耀是一家专注于创新药研发、临床开发、制造和商业化的生物制药公司,致力于满足全球市场尚未满足的医疗需求。云顶新耀的管理团队在中国及全球领先制药企业拥有深厚的专长和丰富的经验。公司在浙江嘉善拥有具备商业化规模的全球生产基地,并严格按照国家药品监督管理局(NMPA)和欧洲药品管理局(EMA)的GMP要求及世界卫生组织(WHO)PQ标准建设。公司聚焦自身免疫、眼科、急重症及CKM(心血管、肾脏及代谢)等疾病治疗领域,已打造集全渠道商业化体系与药品全生命周期商业化能力于一体的商业化平台,并以拥有全球权益的自研mRNA平台为基础,持续推进mRNA in vivo CAR-T与mRNA肿瘤疫苗等现有管线,同时通过引进及生态孵化潜力平台,拓展研发能力,同时强化全球化布局,加快国际化发展进程。