• JAB-23E73的I期临床数据展现出优于pan-KRAS分子胶RMC-6236的潜力;
• 加科思进入收获期,预计今年扭亏为盈;
• 加科思pan-KRAS小分子抑制剂专利布局行业领先;
• 加科思正在通过xADC平台拓宽KRAS治疗安全窗口;
• 在合作伙伴选择上,王印祥博士认为,除了市场推广能力,管线协同性也是关键考量因素。
加科思在泛KRAS(pan-KRAS)小分子抑制剂这一赛道率先取得了突破。JAB-23E73作为全球首个披露临床数据的pan-KRAS小分子抑制剂,其I期临床数据显示,该产品在安全性及胰腺导管腺癌(PDAC)后线治疗疗效上具有优于RMC-6236的潜力。
Revolution Medicines研发的RMC-6236是pan-KRAS分子胶类药物的代表性产品,在该赛道全球的在研产品中临床进展最快,已推进至III期,并获FDA突破性疗法认定。凭借该产品的潜力,此前曾传出默沙东与Revolution洽谈收购,交易规模或超300亿美元的消息。
“pan-KRAS赛道的两大技术路线,无论小分子还是分子胶,耐药问题和毒副作用方面仍有较大优化空间,于是加科思还前瞻性地布局了xADC技术平台。”加科思董事长兼联席CEO王印祥博士告诉研发客。

加科思董事长兼联席CEO 王印祥博士
率先披露临床数据
KRAS突变涉及约23%的人类癌症,在胰腺癌、结直肠癌、非小细胞肺癌等高发癌种中均有高比例突变,每年新增相关病例约为270万。在克服多种突变和耐药问题的巨大临床需求下,多家国内外企业涌入pan-KRAS赛道,形成小分子抑制剂与分子胶两大技术路线的分流与对抗。(见下图)
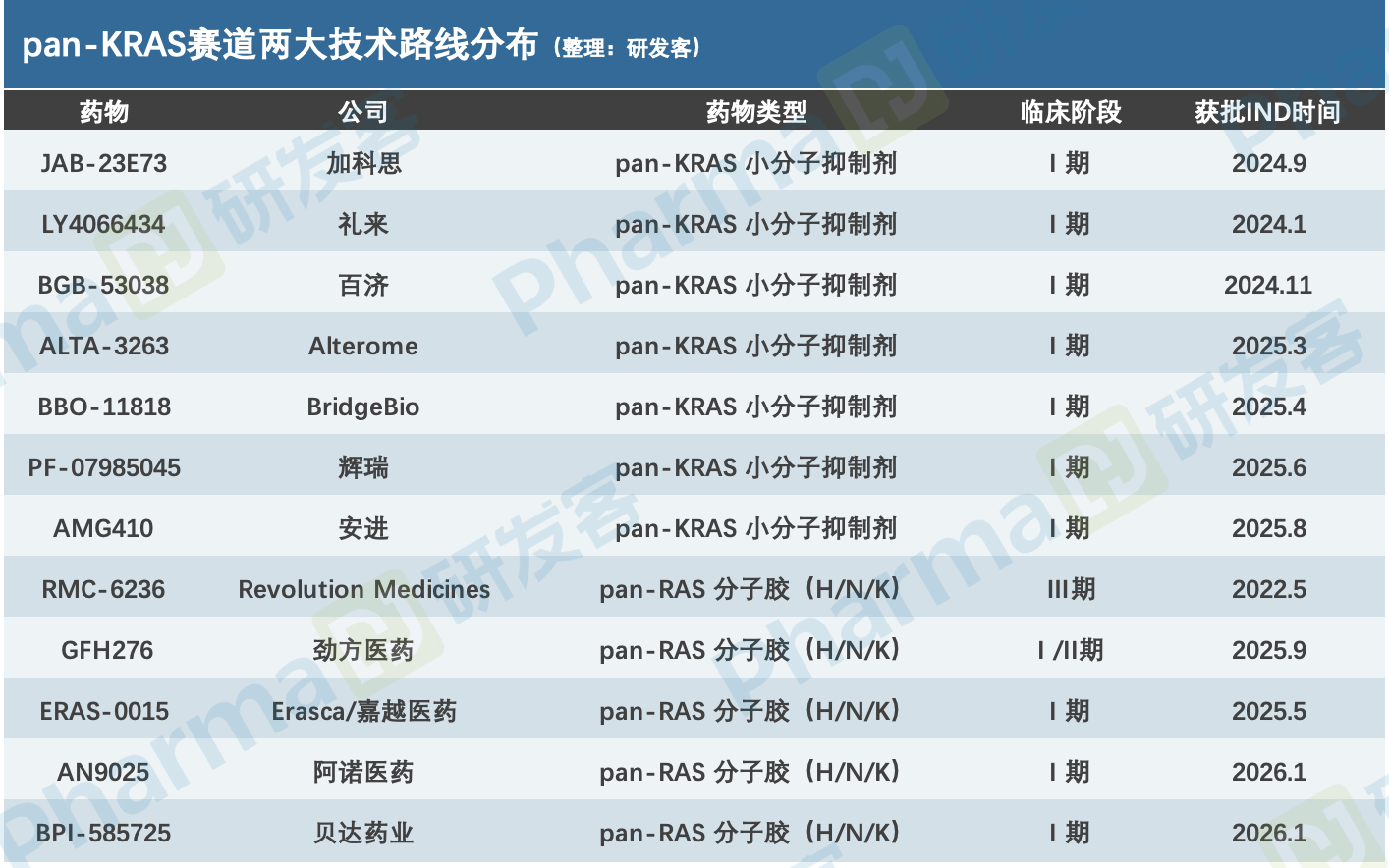
目前,分子胶赛道除Revolution的RMC-6236进入III期外,其余均处在临床I期。小分子赛道相关在研产品均处在临床I期,主要玩家包括礼来、辉瑞、百济神州等;加科思的JAB-23E73进度相对领先,针对PDAC后线治疗的I期试验正在中美同步开展。
近日,加科思率先披露了JAB-23E73的PDAC中国临床数据。
截至2026年1月15日,中国I期试验已入组42例患者,三级治疗相关不良事件(TRAE)发生率为11.9%,远低于RMC-6236的34%。在安全性关键指标上,JAB-23E73 所有级别的皮疹发生率为14.3%,且无三级及以上的皮疹反应,而RMC-6236的皮肤毒性发生率高达91%,其中8%为三级及以上严重副反应。
“分子胶同时抑制HRAS、NRAS和KRAS三个靶点,而与肿瘤相关的主要是KRAS,另外两个靶点的抑制可能带来更高的毒副作用风险。”王印祥解释道,机制上的区别使得小分子抑制剂在安全性上具备先天优势。
疗效方面,JAB-23E73 同样表现亮眼。在预测有效剂量范围内的13例(包括2例二线和11例三线及三线以上)PDAC患者中,客观缓解率(ORR)为38.5%(其中包括已确认和未确认PR),疾病控制率(DCR)为84.6%。而RMC-6236针对三线及以上后线患者的ORR约为22%。
此外,JAB-23E73联合白蛋白结合型紫杉醇和吉西他滨用于KRAS突变胰腺癌一线治疗的Ib/III期临床试验已于2026年2月获得国家药监局药审中心批准。
提前构建专利护城河
为了应对未来的竞争,加科思在pan-KRAS小分子抑制剂领域已提前布局87件有效优先权专利,不仅数量远超BMS、辉瑞和百济神州等竞争对手,且最早优先权日为2021年8月18日。(见下图)
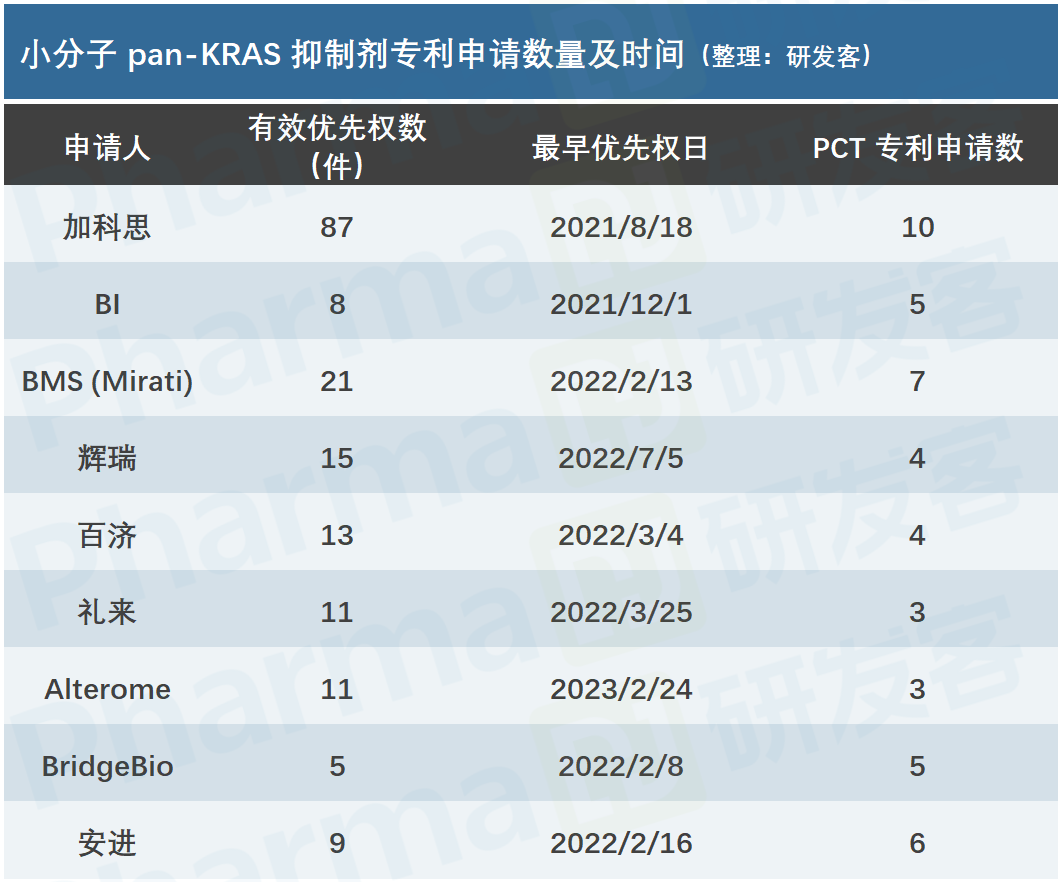
数据来源 | 加科思
“我们在专利布局和技术原创性方面有系统性的积累和前瞻性规划,并且已经形成较为扎实的专利布局基础。”王印祥表示,小分子pan-KRAS的结合口袋非常浅,研发难度极高,后续企业很难找到新的突破空间,加科思在这一领域的先发优势已转化为难以逾越的竞争壁垒。他透露,已有其他竞争对手因专利限制被迫调整研发方向。
相比之下,分子胶因专利空间相对更大、合成工艺更加复杂,导致市场竞争分散,且制造成本高昂,其在中国的商业化可行性未来可能会受到限制。
xADC有望开辟KRAS治疗新路径
面对第一代口服pan-KRAS药物在安全窗和耐药性上的局限,加科思布局了tADC(靶向药载荷ADC)和iADC(免疫招募剂ADC)两大技术方向,希望进一步拓宽KRAS治疗的安全窗口。
tADC平台的代表项目JAB-BX600以EGFR抗体为靶向载体,将高活性KRAS G12D抑制剂作为功能性载荷。
据介绍,其载荷细胞活性在当前KRAS G12D抑制剂项目中处于最高水平,tADC细胞活性可达10皮摩尔(pM)级别,显著优于小分子口服 KRAS 抑制剂普遍的纳摩尔(nM)级别。同时,tADC释放的G12D抑制剂在肿瘤中的Cmax(药峰浓度)为血浆中的2000倍,安全窗更宽,而常规口服小分子药物在肿瘤与血液中的浓度基本相当。
此外,将EGFR抗体作为递送载体可同时发挥抗体的协同作用,阻断KRAS抑制剂单药治疗诱导的EGFR负反馈激活,克服代偿性耐药,在结直肠癌适应症中优势更为突出。与口服小分子抑制剂相比,其精准靶向的特性进一步增强了药物安全性与治疗窗口,疗效也更为持久。
iADC平台的核心项目JAB-BX467则是以HER2抗体为靶向载体,搭载 STINGa(STING激动剂)。STINGa可促进干扰素和趋化因子分泌,在肿瘤微环境中招募淋巴细胞,将“冷肿瘤”转化为“热肿瘤”,从而有望解决约70%的实体瘤患者对PD-1单药无响应的临床困境。
临床前数据显示,JAB-BX467能显著促进T细胞浸润肿瘤组织,在HER2高表达和低表达肿瘤模型中,均展现出比DS-8201更持久的肿瘤杀伤效果,且能介导长期免疫记忆——经治疗的小鼠在再次接种肿瘤后仍能有效抑制肿瘤生长。
目前全球仅有第一三共的iADC同类项目DS-3610A进入了临床(I期)。
“功能性载荷 ADC 从机制上改变了传统ADC的肿瘤杀伤逻辑。而且我们的xADC平台的模块化设计支持抗体与载荷的灵活组合,未来可拓展更多靶点和适应症,形成可持续的技术迭代能力。”王印祥表示。
加科思预计于2026年下半年提交JAB-BX467和JAB-BX600的IND申请。除已披露的两个核心项目外,加科思还在推进多个未公开靶点的ADC项目。
平衡BD短期收益与长期价值
已成立十年的加科思,除了前述pan-KRAS抑制剂、新一代ADC,还有靶向P53 Y220C、BET、Aurora A 等多个口服小分子项目正在中美同步推进针对肿瘤的临床试验,构建了覆盖不同肿瘤类型的差异化管线。今年加科思将进入收获期。财报显示,其2025年收支结余为正,预计今年实现扭亏为盈。
2026年收入的重要支撑,来自去年与阿斯利康就JAB-23E73完成许可与合作协议交割的1亿美元首付款。2025年12月,加科思与阿斯利康就JAB-23E73达成总额20.15亿美元的授权协议,创下中国临床阶段小分子抗肿瘤药对外授权金额最高纪录。
此外,加科思还将收到艾力斯就戈来雷塞的销售分成。戈来雷塞由加科思的合作伙伴艾力斯负责在中国的商业化推广,已于去年在中国获批上市,用于治疗既往接受过至少一线系统治疗的KRAS G12C突变非小细胞肺癌患者,并于同年纳入国家医保目录,今年有望进一步放量。
“全球KRAS赛道竞争激烈,阿斯利康在肿瘤领域的推广能力能帮助我们抢占先机,我们评估后认为更大的市场规模带来的长期收益远胜于独自推进到临床后期可能获得的更高首付款。“王印祥说,“对于Biotech来说,资金链的安全非常重要,这笔交易的回报可以为我们xADC产品的研发提供充足弹药。”
除了市场推广能力,王印祥认为管线协同性也是关键考量因素。阿斯利康在靶向药ADC领域均处于全球领先地位,其丰富的管线资源能与加科思pan-KRAS抑制剂形成联合用药方案,尤其是在肺癌、结直肠癌等适应症的一线治疗中发挥协同作用。
这种“战略互补,长期共赢”的合作逻辑,也体现在与艾力斯的商业化合作中——艾力斯在肺癌领域的学术推广优势与加科思的技术支撑形成互补,可推动戈来雷塞快速实现市场渗透。
王印祥告诉研发客,加科思接下来BD策略将更加从容,后续项目不会急于推进BD,会等待更多临床数据出来后再寻求价值最大化的合作。他强调“关注长期的基础研究突破比追求短期效应更能带来持续的成功”,因为基础研究与技术转化是生物医药企业的核心竞争力。
编辑 | 姚嘉
yao.jia@PharmaDJ.com
访问研发客网站,深度报道和每日新闻抢鲜看