银屑病是由遗传与环境共同作用诱发的免疫介导的慢性、复发性、炎症性、系统性疾病1。我国银屑病患病率约0.5%,患者约700万例2。银屑病存在多种合并症,以肥胖为代表的代谢相关合并症发生率最高,占12.21%-41.67%3-5。随身体质量指数(BMI)增加,患者发展为重度银屑病风险及进展为银屑病关节炎的风险也大幅提升6-7,形成"肥胖-炎症-银屑病"的恶性循环,成为临床诊疗的重要难题。
2026年美国皮肤科学会年会(AAD)上,新型IL-23p19抑制剂匹康奇拜单抗(Picankibart)凭借Ⅲ期CLEAR-1临床研究亚组分析的亮眼数据,打破BMI和体重对银屑病治疗效果的桎梏,在银屑病领域率先带来了“超重/肥胖不影响疗效”的中国方案。
肥胖对银屑病治疗的核心挑战
从病理机制来看,肥胖驱动的慢性低度炎症是关键:这种状态通过多种机制破坏免疫稳态,包括异常的脂肪因子分泌、炎症细胞因子水平升高以及各种免疫细胞功能的改变,如促炎性T细胞群增加(包括Th1 、CD8+ 、Th17 )及炎症介质生成增加(包括IFN - γ 、IL-17 ),进一步加重皮肤的炎症反应8;同时肥胖会改变抗体药物在体内的分布容积与清除率,导致生物制剂暴露不足9 ,降低治疗效果。
这一病理机制转化为临床治疗的多重严峻挑战——既往主流生物制剂疗效普遍受BMI影响:肥胖是TNF-α抑制剂(如阿达木单抗)疗效不佳的预测因素10;在IL-17抑制剂中,司库奇尤单抗需为体重≥90kg患者增加给药频率才能保证疗效且BMI对其药物留存率产生负面影响11-12,针对依奇珠单抗的相关研究同样显示其在肥胖患者中应答不足11; IL-23抑制剂古塞奇尤单抗在肥胖患者中也存在皮损清除延迟问题,第12周时BMI<25与≥30 kg/m²亚组PASI=0应答率相差达30%,肥胖组(BMI≥30 kg/m²)仅14.4%达到皮损全清13。此外,超重/肥胖患者外用药物渗透受限14、传统系统治疗毒性风险升高15-16,多重因素叠加进一步加剧了治疗困境,临床亟需突破体重桎梏的新型疗法。
匹康奇拜单抗在不同BMI和体重的成人斑块状银屑病患者中的疗效:Ⅲ期CLEAR-1临床研究的亚组分析
研究背景与目的
该研究是新型IL-23p19抑制剂匹康奇拜单抗的一项Ⅲ期关键性研究(CLEAR-1)的亚组分析,评估了匹康奇拜单抗在中重度斑块状银屑病中国成人患者中的疗效和安全性,本分析重点关注不同BMI和体重(BW)患者的疗效结果17。
研究方法
共有500例患者以2:2:1的比例被随机分配至100mg匹康奇拜单抗组、200mg匹康奇拜单抗组或安慰剂组。100mg和200mg组在第0、4、8周接受200mg匹康奇拜单抗治疗(匹康奇拜单抗组),随后在第20、32、44周分别接受200mg或100mg治疗。安慰剂组在第0、4、8周接受安慰剂后,于第16、20、24、32、44周转为接受200mg匹康奇拜单抗治疗。疗效评估依据为不同BMI(正常,<24 kg/m2;超重,≥24 kg/m2且<28 kg/m2;肥胖,≥28 kg/m2)和体重(<中位数,≥中位数)亚组的PASI百分比应答率17。
研究结果
-
体重无界限:高体重患者同样实现快速、深度、持久皮损清除
-
基线时,中位体重为73.55kg。对于两个体重亚组(<73.55kg组,≥73.55kg组),在第16周时,匹康奇拜单抗组≥73.55kg亚组近80%达到PASI 90,与<73.55kg亚组相当(图1)。在第52周时,100mg组和200mg组达到PASI 75、90、100的百分比与第16周时相当,疗效保持稳定(图2)17。
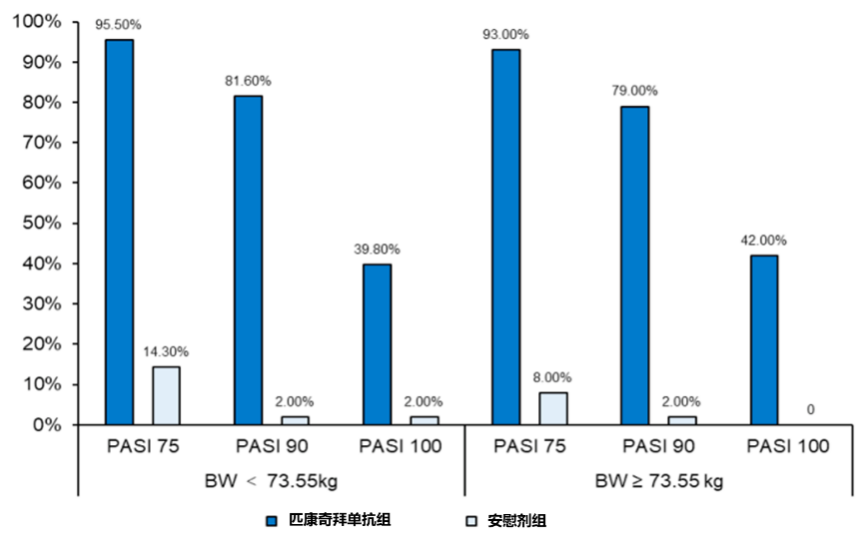
图1 第16周不同体重PASI75、90、100应答率
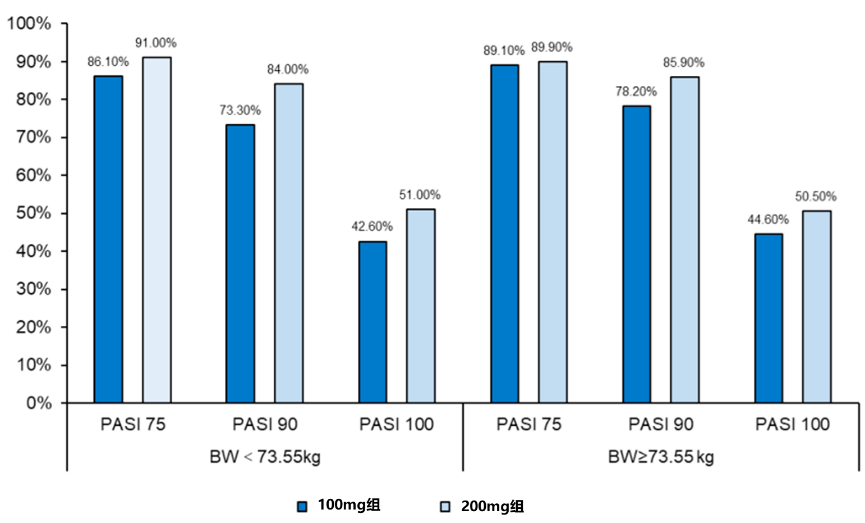
图2 第52周不同体重PASI75、90、100应答率
-
BMI全覆盖:超重/肥胖患者与正常BMI患者获益相当
-
研究基线中,正常人群、超重和肥胖的百分比分别为31.6%、41.2%和27.2%。在第16周时,匹康奇拜单抗在正常亚组、超重亚组和肥胖亚组中PASI 90应答率分别为82%,80%,78.7%(图3),三个亚组应答情况相当。在第52周时,100mg组 、200mg组不同BMI亚组达到PASI 75、90、100的百分比与第16周时基本相似(图4)17。这一结果提示了,匹康奇拜单抗在疗效的早期应答和长期稳定中,均保持了不受BMI影响的稳定疗效,有效解决了既往部分生物制剂在合并超重/肥胖患者中应答不佳的核心难题,为该类银屑病患者的治疗提供了优选方案。
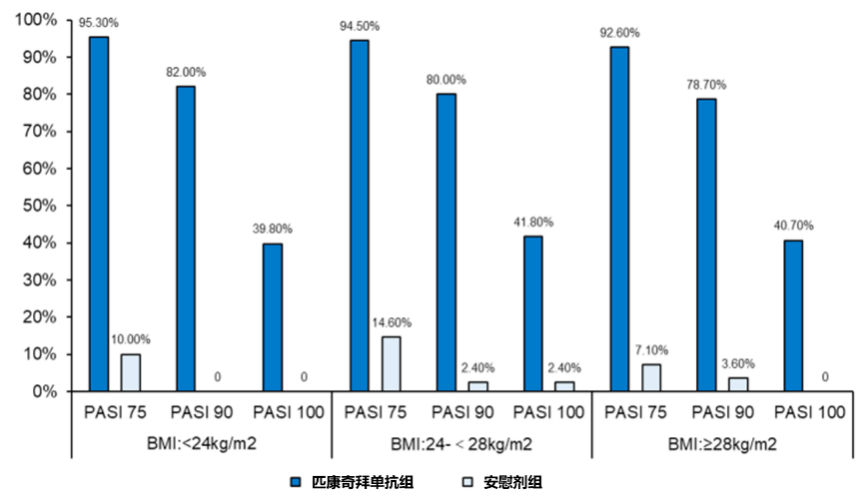
图3 第16周不同BMI PASI75、90、100应答率
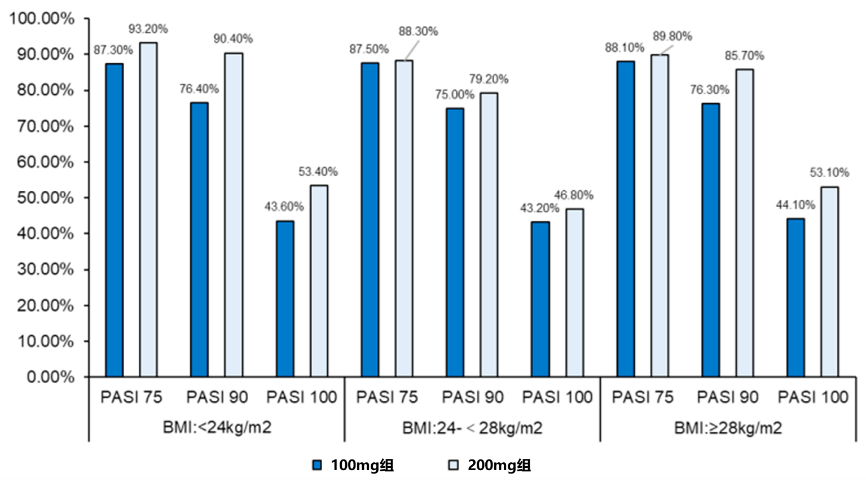
图4 第52周不同BMI PASI75、90、100应答率
研究结论
上述结果表明,匹康奇拜单抗在各种BMI和体重亚组患者中均可显著清除皮损。匹康奇拜单抗起效迅速,大多数患者在第16周达到PASI 90,约40%患者达到PASI 100。此外,在整个试验过程中,所有亚组的治疗效果均得到持续维持。第16周和第52周之间,PASI 75、PASI 90和PASI 100的应答率保持相当。因此,匹康奇拜单抗在不同体重和BMI亚组中表现出相当的皮损清除效果,进一步证明其作为一种新型IL-23抑制剂的理想疗效17。
信达生物深切关注中国慢病患者需求,在银屑病与肥胖领域双线布局。在银屑病领域打造首个国内原研IL-23p19抑制剂匹康奇拜单抗,长效便捷且对高BMI人群同样疗效稳定,切合银屑病患者慢病管理需求;在减重领域推出全球首个获批的GCG/GLP-1双靶点减重降糖药物玛仕度肽,为肥胖问题提供了创新方案。
关于信美悦®(匹康奇拜单抗注射液)
匹康奇拜单抗(研发代号:IBI112)为重组抗白介素23p19亚基(IL-23p19)抗体注射液,是由信达生物自主研发,具有自主知识产权的一种单克隆抗体,特异性结合IL-23p19亚基。通过阻止IL-23与细胞表面受体结合,阻断IL-23受体介导信号通路发挥抗炎作用。匹康奇拜单抗有望为银屑病、溃疡性肠炎和其他自身免疫性疾病患者提供更有效、更长给药周期的治疗方案。
信美悦®(匹康奇拜单抗注射液)获得NMPA批准适应症为:适合系统性治疗的中重度斑块状银屑病成人患者。
匹康奇拜单抗当前开展了多项临床研究,包括:
-
在中重度斑块状银屑病患者中开展的注册III期临床研究(CLEAR-1);
-
在中重度斑块状银屑病患者中开展的随机撤药再治疗的III期临床研究(CLEAR-2);
-
在中重度斑块状银屑病患者中开展的生物制剂治疗转匹康奇拜单抗治疗的III期临床研究(CLEAR-3);
-
在中重度斑块状银屑病患者中开展的生物制剂治疗转匹康奇拜单抗治疗的II期临床研究;
-
在中重度活动性溃疡性结肠炎患者中开展的II期临床研究;
除CLEAR-3研究正在进行中,其余研究均已达成终点。
此外,匹康奇拜单抗治疗青少年银屑病和成人银屑病关节炎等多项新临床研究正在开展中。
关于信达生物
“始于信,达于行”,开发出老百姓用得起的高质量生物药,是信达生物的使命和目标。信达生物成立于2011年,致力于研发、生产和销售肿瘤、自身免疫、代谢、眼科等重大疾病领域的创新药物,让我们的工作惠及更多的生命。公司已有18个产品获得批准上市,它们分别是信迪利单抗注射液(达伯舒®),贝伐珠单抗注射液(达攸同®),阿达木单抗注射液(苏立信®),利妥昔单抗注射液(达伯华®),佩米替尼片(达伯坦®),奥雷巴替尼片(耐立克®), 雷莫西尤单抗注射液(希冉择®),塞普替尼胶囊(睿妥®),伊基奥仑赛注射液(福可苏®),托莱西单抗注射液(信必乐®),氟泽雷塞片(达伯特®),匹妥布替尼片(捷帕力®),己二酸他雷替尼胶囊(达伯乐®),利厄替尼片(奥壹新®),替妥尤单抗N01注射液(信必敏®),玛仕度肽注射液(信尔美®),伊匹木单抗N01注射液(达伯欣®)和匹康奇拜单抗(信美悦®)。目前,5个新药分子进入III期或关键性临床研究,另外还有14个新药品种已进入临床研究。
公司已与礼来、罗氏、武田、赛诺菲、Incyte和MD Anderson 癌症中心等国际合作方达成30多项战略合作。信达生物在不断自研创新药物、谋求自身发展的同时,秉承经济建设以人民为中心的发展思想。多年来,始终心怀科学善念,坚守“以患者为中心”,心系患者并关注患者家庭,积极履行社会责任。公司陆续发起、参与了多项药品公益援助项目,让越来越多的患者能够得益于生命科学的进步,买得到、用得起高质量的生物药。截至目前,信达生物患者援助项目已惠及20余万普通患者,药物捐赠总价值36亿元人民币。信达生物希望和大家一起努力,提高中国生物制药产业的发展水平,以满足百姓用药可及性和人民对生命健康美好愿望的追求。
声明:
1.信达不推荐任何未获批的药品/适应症使用。
2.雷莫西尤单抗注射液(希冉择®),塞普替尼胶囊(睿妥®)和匹妥布替尼片(捷帕力®)由礼来公司研发。
参考文献:
1.中国银屑病诊疗指南(2023版)
2.李慧贤,等.基于全球疾病负担(GBD)大数据的中国银屑病流行病学负担分析[J].中国皮肤性病学杂志,2021,35(4):386-392
3. Haque, A, et al. Int J Res Dermatol. 2025; 11 (2): 88-93.
4. Chen W, et al. Clin Cosmet Investig Dermatol. 2025;18:491-501.
5. Almenara-Blasco M, et al. J Clin Med. 2024;13(2):492.
6.Love TJ, et al. Ann Rheum Dis. 2012;71(8):1273-1277.
7.Wang H, et al. Sci Rep. 2025 Apr 1;15(1):11158.
8. Qin Fei,et al. Biomedicines. 2025 Jun 10;13(6):1429.
9. Xin Wang and Linfeng Li.Front Pharmacol.2026 Jan 6:16:1685072.
10. Singh S, et al. PLoS One. 2018 May 17;13(5):e0195123.
11. Pirro F, et al. Clin Drug Investig. 2021;41(10):917-925.
12. Li Y, et al. J Am Acad Dermatol. Published online February 23, 2026.
13. Guselkumab improves psoriatic skin and HRQoL outcomes across BMI subgroups, including patients with involvement of hard-to-treat areas: results from the real-world PERSIST study. AAD ID: 51791
14. Vata D, et al. Life (Basel). 2023;13(10):1947.
15.Herron MD, et al. Arch Dermatol. 2005;141(12):1527-1534.
16. Vata D, et al. Life (Basel). 2023;13(10):1947.
17. Yuling Shi,et al. Efficacy of Picankibart among Difference BMI and Body Weight in Adult Plaque Psoriasis: Subgroup Analyses of the Phase 3 CLEAR-1 Trial.2026 AAD.