
FDA目前已经批准Dupixent 9个适应症,特应性皮炎是第一个获批的。Keytruda首先运用在黑色素瘤的治疗中,之后获得批准用于超过40种适应症——这些“重磅炸弹”临床开发时的第一步是怎么走的,选择适应症的时候又需要考虑什么呢?
我先把结论放在前面:同样的分子,评估不同适应症的时候,我们需要从科学、临床开发和商业价值的角度来综合考量;而做决策的时候,我们则需要对自己有正确、全面的认知,知道在速度、资源、风险和价值这些因素中,什么对我们来说最关键、最重要。
这里我举一个比较简单易懂的例子:刚刚获批的强生口服多肽Icotyde(icotrokinra)。
icotrokinra是强生与Protagonist Therapeutics共同开发的IL-23受体的口服抑制剂。在去年完成的III期银屑病试验里,它不仅相比安慰剂达到了试验的主要终点,而且在和BMS的Sotyktu头对头的比较里也更有效,因此被称为有可能改变游戏规则的重磅药物[1]。但是在2017年授权交易的新闻稿里[2],炎症性肠病才是这个分子当时计划中的适应症。我们可以试着分析一下,为什么银屑病最终被选作首发适应症呢?
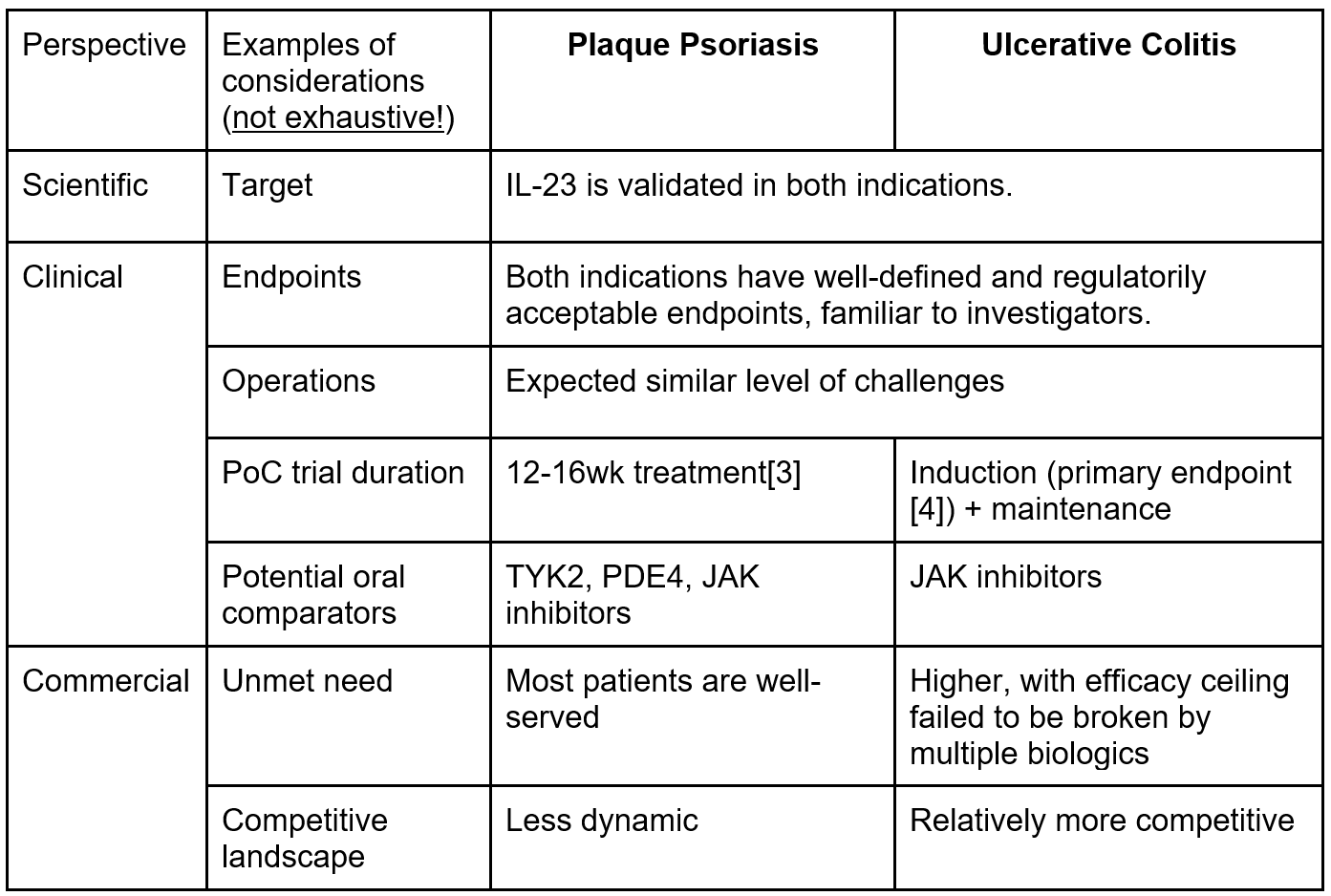
来源|作者根据资料制作
首先,这个例子简单易懂是因为IL-23及相关的作用机制在这两个适应症里都是已经验证过的,因此从科学的角度来看,如果这个分子在皮肤里的药代动力学数据也好,先开发银屑病或是炎症性肠病应该没有太大区别。
其次,从开发途径的角度来说,临床试验的考虑有一些不同之处:第一,银屑病试验时间较短,而溃疡性结肠炎的试验不仅需要诱导,维持期的数据也很重要;第二,银屑病当时有几款口服小分子效果勉强,icotrokinra挑Sotyktu这个软柿子来捏比较有把握。除此之外,两个适应症的主要终点和监管要求方面都很清晰明确,运营挑战也应该差别不大。
最后的考虑是根据商业价值。银屑病(加上银屑病关节炎)和炎症性肠病(先看溃疡性结肠炎)的中、重症发病率都很高,市场巨大,不相伯仲。银屑病未满足的临床需求相比略低 (不少竞品都是看PASI 90甚至PASI 100这样的有效性终点), 但是竞争也不像在炎症性肠病中那么激烈。
综上,如果单从这个分子的角度考虑,银屑病在临床试验所需资金、时间上略胜一筹。如果III期做头对头比较,风险略大一些,但如果成功,应该会带来更高的市场份额和更大的价值。
可是,如果我们从强生的整个免疫管线策略来看,比较的结果就很明显了。
类似罗氏的一个CD20靶点养活大半个公司(rituximab、obinutuzumab、 ocrelizumab、mosunetuzumab 和glofitamab),强生在IL-23/IL-12路径也是深耕多年,先有Stelara(ustekinumab),后有Tremfya(guselkumab)[5]。icotrokinra的主要任务就是和Tremfya一起,弥补Stelara因为专利悬崖而被侵蚀的销量,同时利用口服的优势继续扩大可能获益的患者人数。
根据管线策略,icotrokinra优先开发银屑病的原因主要有三:一是Tremfya当时已经在银屑病上获批,下一步就是进行炎症性肠病的III期试验,所以要避免自家针对同一靶点的两款药物同一段时间段内在同个适应症上互相残食市场份额;二是强生在炎症性肠病还布局了golimumab和guselkumab的联合疗法,成功率较高;最后一点,强生终止了另一款口服IL-17A抑制剂的开发,所以更加需要icotrokinra巩固它在银屑病的市场地位。

来源|作者根据资料制作
速度、资源、风险和价值这四个因素之间互相影响,并不完全独立。一般来说,跨国大药企最看重的是每款药物和整个管线的匹配度及商业价值,其次是风险。
还是icotrokinra的例子:II期试验中,100mg日服两次的有效性最好;但III期试验直接把200mg日服一次作为最终的剂量,是一个冒着可控风险来追求利益最大化的典型例子。
对于初创企业来说,虽然价值和风险都很重要(尤其是在融资的时候),但多数情况下必须根据有限的时间和资金做出取舍。
Nature Biotechnology三月的一篇文章列举了多家公司开发不同T细胞结合器来深度清除B细胞,从而治疗不同免疫疾病的例子:其中大多数公司都选择了系统性红斑狼疮作为第一个适应症,但也有一些公司另辟蹊径[5]。这些决定与分子在临床前的数据肯定有关,但更主要是取决于公司的资源、对风险的接受程度、退出策略及长远规划:有的资金雄厚,冒着风险也要在所有的大饼上都先啃上一口;有的打算率先把一两个被别人忽视的饼干完全吞下,先填填肚子;更多的是在食堂排队买盒饭,按部就班、循规蹈矩。
所以说,各家对适应症的选择、优先级及其开发的先后顺序没有对错优劣之分,只是针对不同的情况斟酌考量、权衡利弊的结果。我们收集详尽的信息来全面评估管线、布局适应症就已经很不容易了,最难的一步,其实是提高自己的认知,正确客观地了解、评价自己的优势、所需、最终的底线和发展方向。
Sources:
[1] https://www.fiercepharma.com/pharma/jj-protagonists-game-changer-once-daily-psoriasis-pill-icotyde-nabs-fda-approval?utm_medium=email&utm_source=nl&utm_campaign=LS-NL-FiercePharma&oly_enc_id=6121H9540689D6A
[2] JNJ press release. https://www.jnj.com/media-center/press-releases/janssen-enters-into-worldwide-exclusive-license-and-collaboration-agreement-with-protagonist-therapeutics-inc-for-the-oral-interlukin-23-receptor-antagonist-drug-candidate-for-the-treatment-of-inflammatory-bowel-disease
[3] FRONTIER1 (Ph2b in PsA): https://clinicaltrials.gov/study/NCT05223868?term=JNJ-77242113&viewType=Card&cond=Plaque%20Psoriasis&rank=6&tab=study#study-plan
[4] ANTHEM-US (Ph2b in UC) https://clinicaltrials.gov/study/NCT06049017?cond=Ulcerative%20Colitis&term=JNJ-77242113&viewType=Card&rank=1#study-plan
[5] Business review 2023 Dec. https://s203.q4cdn.com/972069832/files/doc_downloads/2024/01/innovative-medicine-presentation-update.pdf
[6] Senior M and Grieshaber-Bouyer. B cell depletion in autoimmune disease: in vivo CAR-T or T cell engagers? Nature Biotechnology (2026) https://doi.org/10.1038/s41587-026-03069-5
“马后炮”栏目文章回顾
免疫界新星Abivax:新靶点开发的控风险样本 | 药物研发三角定律(上)
MNC唯快不破,Biotech“四不像” | 药物研发三角定律(下)
知“错”就改的FDA,错了吗?
出师未捷,赛诺菲BTK抑制剂还能翻身吗?
从赛诺菲换帅看临床试验的成功率
Biotech卖的是什么?
编辑 | 陈小娟
xiaojuan.chen@PharmaDJ.com
编辑 | 姚嘉
yao.jia@PharmaDJ.com
访问研发客网站,深度报道和每日新闻抢鲜看