近日,恒瑞医药HER2 ADC创新药瑞康曲妥珠单抗(SHR-A1811)I期HORIZON-X研究(SHR-A1811-I-101)的长期随访结果正式发表于《自然》子刊、国际知名医学期刊《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy,简称STTT,IF:52.7)[1]。
该研究由中山大学孙逸仙纪念医院宋尔卫院士、姚和瑞教授牵头,主要研究结果已于2024年见刊国际肿瘤学领域顶尖期刊《Journal of Clinical Oncology》。本次更新呈现关键次要终点:无进展生存期(PFS)和缓解持续时间(DoR)的最终结果,以及瑞康曲妥珠单抗总体应答和安全性数据的更新分析。结果进一步证实了瑞康曲妥珠单抗在经多线治疗的晚期实体瘤患者中的临床获益和可控的安全性[1]。

图1:HORIZON-X研究见刊《STTT》
研究设计
HORIZON-X研究是一项国际多中心、首次在人体中进行的I期试验,在33个中心开展。纳入了HER2表达或突变的不可切除、晚期或转移性实体瘤,并且对标准治疗无效或不耐受的患者。瑞康曲妥珠单抗通过静脉注射给药,每3周1次,每公斤体重剂量从1.0-8.0mg/kg进行剂量爬坡,选择4.8-8.0mg/kg进行PK拓展,选择4.8和6.4mg/kg进行疗效拓展。主要研究终点为剂量限制性毒性、安全性和Ⅱ期推荐剂量。
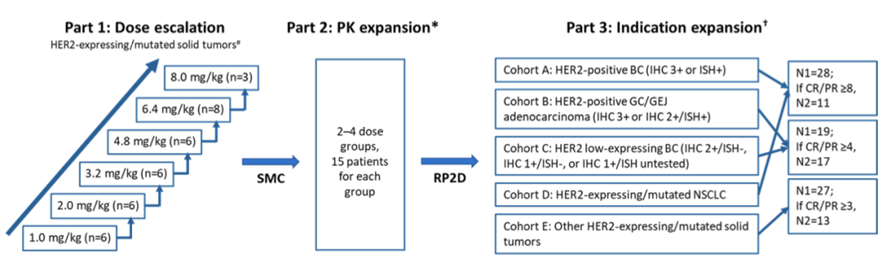
图2:HORIZON-X研究设计
研究结果
1.基线特征
2020年9月7日至2024年6月4日,396例患者接受了瑞康曲妥珠单抗治疗,患者既往中位治疗方案数为3(IQR:2-5)。在246例乳腺癌患者中,HER2阳性乳腺癌患者(N=136)的既往中位治疗方案数为3(IQR:2-5),HER2低表达乳腺癌患者(N=110)为3(IQR:2-5)。HER2阳性乳腺癌队列中,99.3%、43.4%和14.7%的患者分别接受过曲妥珠单抗、帕妥珠单抗和恩美曲妥珠单抗(T-DM1)治疗;HER2低表达乳腺癌队列中,上述比例分别为13.6%、5.5%和2.7%。
截至2025年3月12日,HER2阳性乳腺癌患者的中位随访时间为17.1个月,HER2低表达乳腺癌患者为10.6个月。
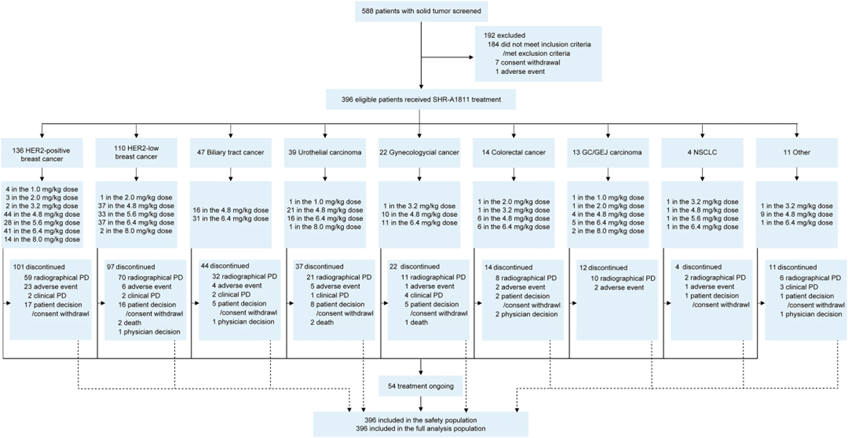
图3:HORIZON-X研究受试者分布
2.疗效
136例HER2阳性乳腺癌患者的中位无进展生存期(mPFS)为25.0个月(95% CI:17.2-33.6),中位缓解持续时间(mDoR)为25.1个月(95% CI:16.8-37.5),客观缓解率(ORR)为78.7%(95% CI:70.8-85.2)。
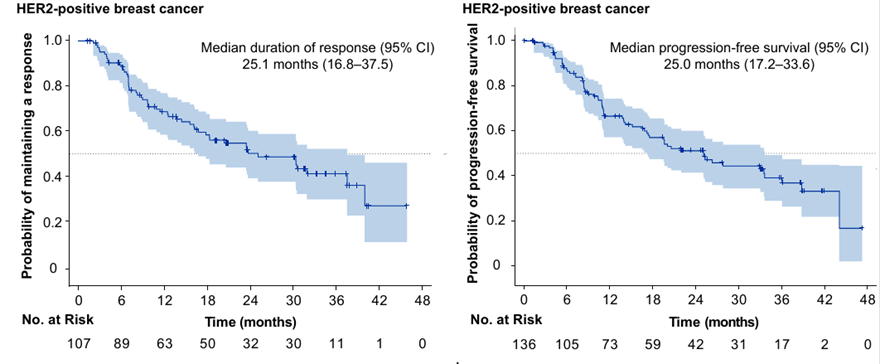
图4:HER2阳性乳腺癌患者的mDoR和mPFS
110例HER2低表达乳腺癌患者的mPFS为11.0个月(95% CI:8.2-13.8),mDoR为12.4个月(95% CI:8.1-22.1),ORR为61.8%(95% CI:52.1-70.9)。
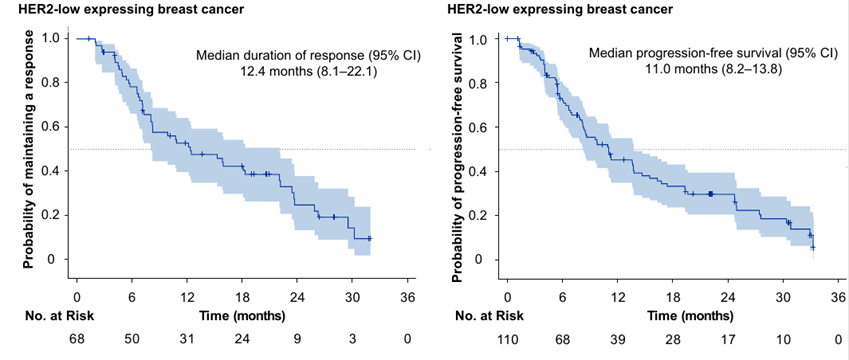
图5:HER2低表达乳腺癌患者的mDoR和mPFS
在246例乳腺癌患者中,205例接受了中心实验室HER2检测,其中有54例HER2超低表达或零表达患者,mPFS为9.8个月(95% CI:7.2-13.8),ORR为59.3%。
在伴有肝转移/脑转移(疾病进展高风险人群)的乳腺癌患者中,肿瘤应答同样具有持久性。HER2阳性乳腺癌肝转移患者(N=52)的mPFS为27.8个月(95% CI:11.0-38.7),mDoR为30.4个月(95% CI:11.5-NE);HER2低表达患者(N=65)的mPFS为10.9个月(95% CI:7.8-13.6);mDoR为10.8个月(95% CI:8.1-22.1)。HER2阳性乳腺癌脑转移患者(N=18)中位PFS为14.1个月(5.3–19.5),HER2低表达患者(N=3)为8.5个月(7.0–NE)。
3.安全性
整体安全性可控。
总结
本次最终分析进一步证实了瑞康曲妥珠单抗在经多线治疗的晚期实体瘤患者中的临床获益和可控的安全性,有望成为经多线治疗的HER2表达或突变实体瘤患者新的治疗选择。基于随之开展的III期HORIZON-Breast01研究[2],瑞康曲妥珠单抗于2026年3月已正式获批乳腺癌领域首个适应证,适用于治疗既往接受过一种或一种以上抗HER2药物治疗的局部晚期或转移性HER2阳性成人乳腺癌患者。
值得一提的是,瑞康曲妥珠单抗已布局多个疾病领域。2025年5月获批用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。截至目前,瑞康曲妥珠单抗已有十项适应症被纳入突破性治疗品种名单,覆盖非小细胞肺癌、乳腺癌、胃癌或胃食管结合部腺癌、结直肠癌、胆道癌、妇科恶性肿瘤等多个瘤种,未来有望为更多肿瘤患者带来新的治疗选择。
参考文献:
[1] Yao, H., et al. Sig Transduct Target Ther 11, 104 (2026).
[2] Song EW, et al. 2025 ESMO LBA19.