脑转移是非小细胞肺癌(NSCLC)患者最常见的远处转移并发症之一,预后极差且患者常伴随神经系统功能障碍,严重影响生活质量,临床上有巨大未被满足的治疗需求。在刚结束的2026年欧洲肺癌大会(ELCC)上,中山大学肿瘤防治中心张力教授和美国MD安德森癌症中心乐秀宁教授等众多国际肺癌专家参与的HARMONi研究公布了颅内疗效的探索性分析结果,引发学界广泛关注。HARMONi研究是一项全球多中心、随机、双盲的Ⅲ期临床研究,对比了依沃西(PD-1/VEGF双抗)+化疗和安慰剂+化疗在EGFR-TKI治疗进展的NSCLC疗效与安全性。本次ELCC公布的结果显示,无论基线是否存在脑转移,联合依沃西均可带来更长的颅内PFS获益,且颅内脑转移累积发生率更低。引人瞩目的是,依沃西通过其独特的“靶免一体”机制展现出强大的 “脑保护” 价值,针对基线无脑转移的患者,依沃西组 12 个月的脑转移累积发生率控制在 3.2% 的极低水平(比对照组发生率减少了2/3),显著延缓并减少了颅内新发转移灶的产生[1]。本文将系统解读HARMONi系列研究颅内疗效,并深入探讨依沃西在治疗和预防肺癌脑转移的优势以及“脑保护”的机制和临床价值。
HARMONi研究探索性分析发现
依沃西实现脑转移“治疗+预防”双重获益
脑转移在NSCLC中发生率高且预后极差。流行病学数据显示,10%-20%的NSCLC患者在初诊时即合并脑转移,而在疾病进程中,高达40%的患者会进展为脑转移[2, 3],尤其是EGFR突变阳性NSCLC患者发生脑转移的风险显著增高,随EGFR-TKI治疗发生率可达约70%[4]。脑转移是NSCLC独立的负面预后因素,一旦发生脑转移,仅接受姑息治疗的中位总生存(OS)时间仅约2个月;即使接受放疗,其中位OS也仅延长至7.6个月左右[2, 3]
HARMONi研究共纳入438例三代EGFR-TKI进展后的EGFR突变NSCLC患者,其中基线伴脑转移者108例(每组各54例)。ELCC公布的结果显示[1],依沃西治疗组在基线伴有脑转移人群的颅内mPFS达到10.1个月,而对照组为6.5 个月,HR=0.53 (0.33-0.84), P=0.0068。在基线无脑转移人群中,依沃西治疗组的中位颅内PFS达15.7个月,也显著优于对照组的11.6个月,HR=0.72(0.55-0.94)。
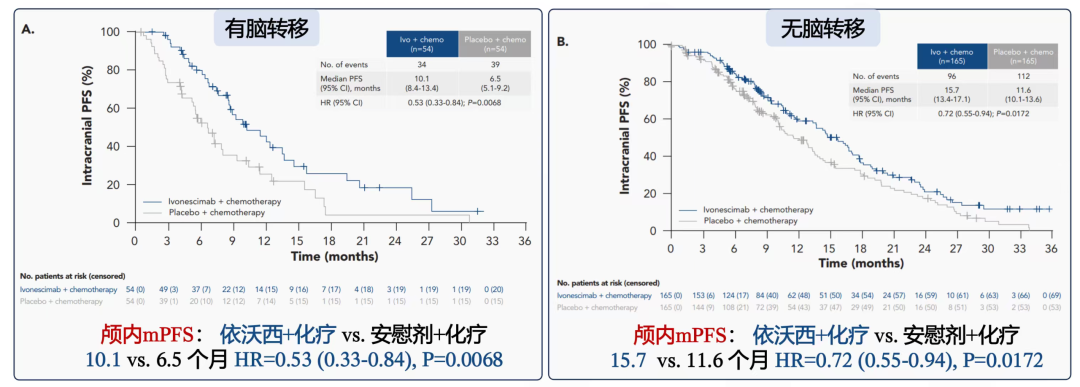
图1 HARMONi研究基线伴或不伴脑转移颅内PFS结果
更令人惊喜的是,依沃西治疗组在6个月和12个月的脑转移累积发生率均显著低于对照组。在基线伴脑转移人群中,依沃西联合化疗组6个月和12个月的颅内进展累积发生率分别为6.1%和10.4%,而对照组则高达30.4%和35.7%(P=0.0007)。在基线无脑转移人群中,依沃西组的6个月和12个月的脑转移累积发生率分别仅为2.5%和3.2%,对照组则为8.1%和9.5%(P=0.0136)[1]。这说明对于基线无脑转移的患者接受依沃西联合化疗治疗的脑转移累积发生率比对照组减少了2/3,在依沃西治疗1年时,仅有3.2%患者发生脑转移。这种差异充分说明了依沃西在治疗和预防脑转移上的优势,依沃西可能具有“脑保护”的作用机制以降低脑转移的风险。
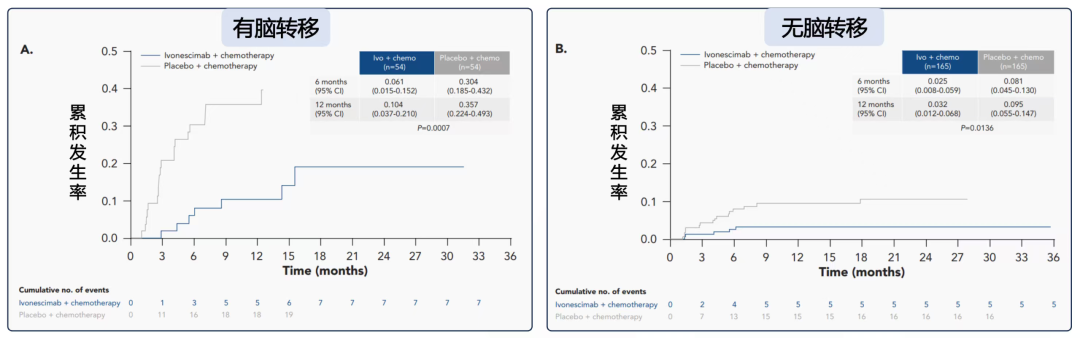
图2HARMONi研究基线伴或不伴脑转移患者的颅内进展累积发生率
HARMONi-A与HARMONi-2研究均表明
依沃西有更强的颅内疗效
HARMONi-A研究是张力教授牵头的一项在中国人群开展的随机、双盲、安慰剂对照的Ⅲ期临床试验,同样纳入EGFR-TKIs治疗后进展的晚期非鳞NSCLC患者。研究共入组322例患者,其中基线伴脑转移者72例(依沃西组35例,安慰剂组37例)[5]。在ITT人群中,依沃西组的mPFS为7.1个月(vs对照组4.8个月),HR:0.46;mOS为16.8个月(vs对照组14.1个月),HR:0.74;其中脑转移亚组PFS和OS的HR值分别为0.40和0.61[6]。依沃西联合化疗治疗EGFR-TKI进展的NSCLC均取得PFS和OS显著获益。
HARMONi-A研究脑转移亚组分析同样显示[7],在基线伴脑转移人群中,依沃西联合化疗组的颅内PFS达8.4个月,对照组仅5.4个月(HR=0.33,P=0.005),6个月颅内PFS率分别为83.7%和42.9%。这意味着,依沃西联合化疗可将脑转移患者的颅内进展风险降低了67%,6个月的颅内无进展生存率翻了一倍!
HARMONi-A研究与HARMONi研究两相印证,奠定了依沃西给EGFR-TKI进展后脑转移患者带来的显著获益。
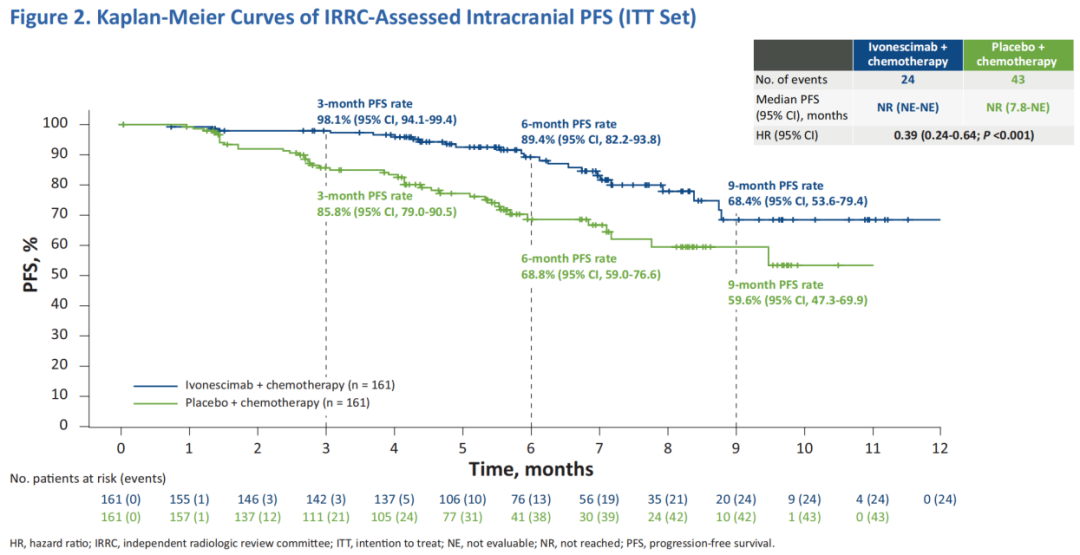
图3HARMONi-A研究ITT人群颅内PFS结果
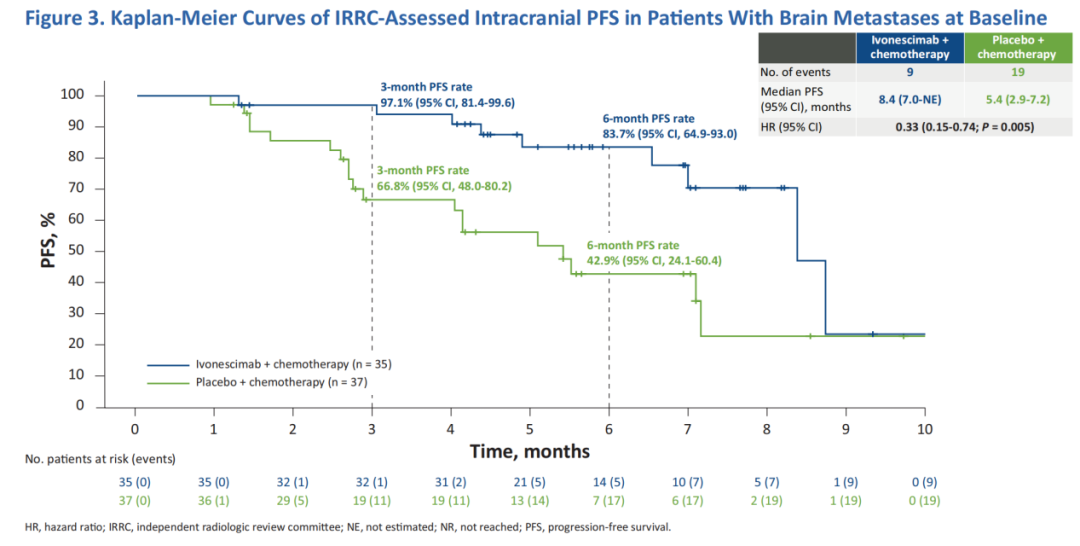
图4HARMONi-A研究基线伴脑转移人群颅内PFS结果
除了HARMONi和HARMONi-A研究中看到的依沃西对于EGFR阳性人群脑转移的突出疗效,HARMONi-2研究在驱动基因阴性NSCLC中的结果也表明:依沃西单药脑转移亚组的PFS为8.0个月,而帕博利珠单抗为5.0个月,HR=0.55。这说明依沃西相较于传统PD-1单抗(帕博利珠单抗)在治疗脑转移方面也有更强获益趋势,可以降低疾病进展或死亡风险45%[8],进一步夯实了依沃西在治疗NSCLC脑转移患者中的优势地位。
基于优秀的数据,依沃西已获得《肺癌脑转移中国治疗指南(2026版)》推荐,用于EGFR-TKI耐药后的非鳞状NSCLC脑转移患者[9]。此外,《中国驱动基因阳性非小细胞肺癌脑转移临床诊疗指南(2025版)》也指出,对靶向治疗耐药的EGFR突变NSCLC脑转移患者,可考虑依沃西联合化疗(推荐)[10]。为临床医师提供了明确的循证依据。
为什么依沃西能在NSCLC脑转移人群取得如此突出的获益,且能显著降低脑转移的发生风险。这需要从机制上深入探讨。
脑转移的发生机制:VEGF与血脑屏障
脑转移的形成是一个多步骤、高度复杂的生物学过程,涉及肿瘤细胞从原发灶脱落、侵入血液循环、穿越血脑屏障、在脑微环境中定植并增殖。正常的脑组织拥有血脑屏障(BBB),这是一种由脑微血管内皮细胞通过紧密连接蛋白(如Claudin-5、Occludin)和粘附连接蛋白(如VE-cadherin)构成的重要防御结构,严格限制血液中大分子物质和免疫细胞进入脑实质,从而维持脑内微环境稳定。然而,在肿瘤脑转移过程中,转移性肿瘤细胞或脑部微环境分泌的血管内皮生长因子(VEGF)可激活内皮细胞表面的VEGFR-2,通过Src激酶介导的紧密连接蛋白磷酸化和内吞作用,并经由Rho/ROCK通路诱导细胞骨架收缩,导致血脑屏障通透性增加,为肿瘤细胞跨内皮迁移进入脑实质提供了“机会”。这也奠定了依沃西在治疗基线脑转移患者和降低或延缓脑转移的潜在机制优势。此前贝伐珠单抗已获批了脑胶质瘤的二线治疗。
依沃西“靶免一体”机制有效控制脑转移
并显著降低脑转移风险
依沃西治疗脑转移的作用机制
依沃西是全球首创的PD-1/VEGF双抗,独特的对称四价结构将PD-1和VEGF融为一体,在体内能发挥抗PD-1和抗VEGF的高效协同作用。一方面依沃西的PD-1部分能通过阻断PD-1/PD-L1通路,解除肿瘤微环境对T细胞的抑制,在外周激活T细胞,被激活的T细胞能够主动穿越受损的血脑屏障进入脑实质,或通过脉络丛和脑膜淋巴管进入脑脊液从而发挥抗肿瘤作用[11]。但脑转移灶的免疫微环境常处于抑制状态,导致脑转移瘤中CD8+T细胞处于耗竭状态,大大限制了疗效。而这正是依沃西另一端抗VEGF的用武之地,抗VEGF能使肿瘤血管正常化、改善免疫微环境,从而为抗PD-1端解除抑制的T细胞提供最佳“战场”环境,提高了对脑转移灶的作用。同时抗VEGF还能缓解脑部水肿,改善神经功能。综上,依沃西的靶免一体,高效协同机制让其在治疗肿瘤脑转移中发挥出更强疗效。
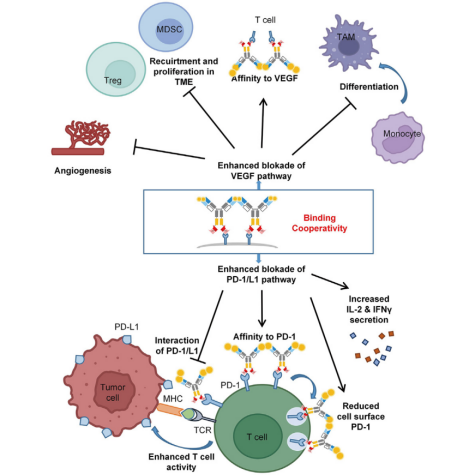
图5 依沃西作用机制
依沃西的脑保护作用机制
-
修复“保护罩”,维持血脑屏障完整性:肿瘤细胞分泌的VEGF-A与脑微血管内皮细胞表面的VEGFR-2受体结合后会激活Src激酶介导的磷酸化和内吞作用,直接破坏紧密连接蛋白(血脑屏障的结构基础)。同时通过Rho/ROCK通路收缩细胞骨架,物理性地拉开细胞连接。这使得血脑屏障从“锁紧”状态变为“漏开”状态,为肿瘤细胞脑转移打开了方便之门。依沃西的抗VEGF作用能够修复血脑屏障[12]。
-
阻断向脑部转移的“导航信号”:VEGF本身就是一个强效的趋化因子,VEGF信号通路可以上调肿瘤细胞表面某些趋化因子受体(如CXCR4)的表达。这些受体与脑组织中高表达的配体(如CXCL12)相互作用,形成一种“导航”信号,引导肿瘤细胞向脑部定向迁移。依沃西的抗VEGF作用可以干扰这一趋化信号,降低肿瘤细胞向脑部迁移的效率[13]。
-
降低肿瘤细胞黏附。VEGF信号通路可以上调肿瘤细胞表面整合素(如αvβ3、α5β1)的表达和活性。高表达的整合素使肿瘤细胞更容易粘附到脑微血管内皮细胞和血脑屏障上,促进跨内皮迁移进入脑实质[14]。
依沃西靶免一体的机制能够降低和延缓脑转移发生的同时,高效杀伤肿瘤细胞和使肿瘤血管“正常化”,最大程度从源头控制VEGF的过高表达,降低了脑转移的发生风险。这也是依沃西与传统PD-1单抗或ADC类药物显著差异化的地方。
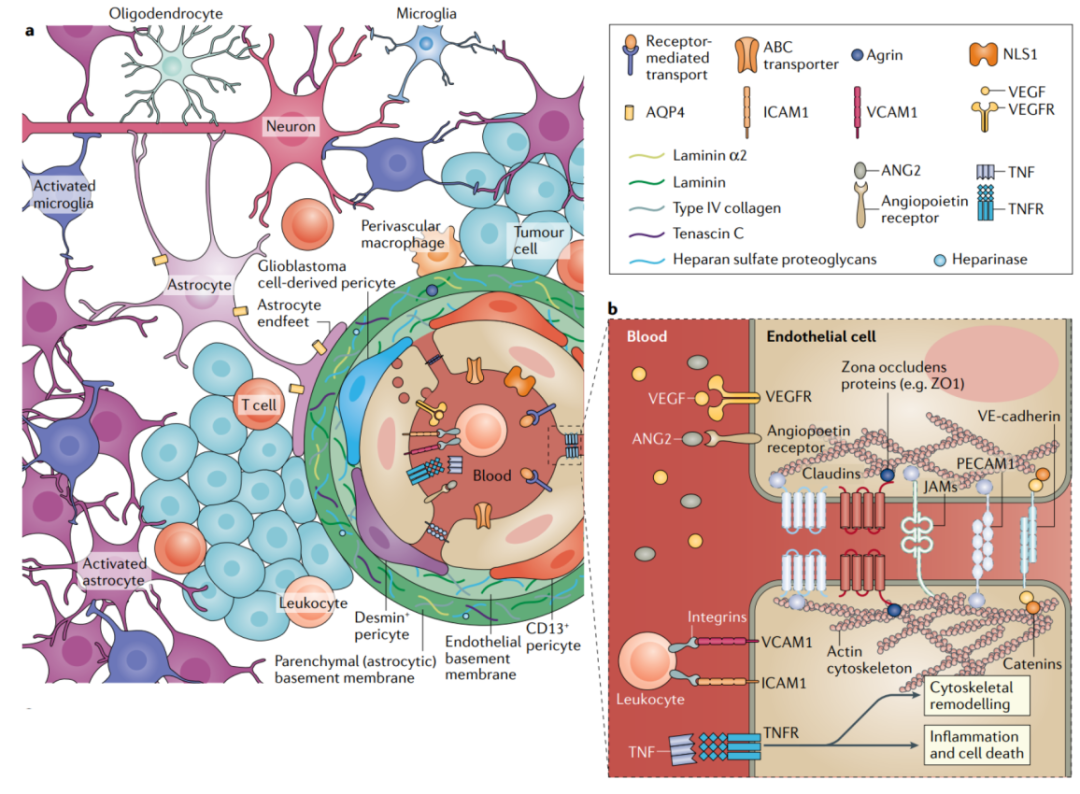
图6VEGF参与细胞间粘附的蛋白发生改变,伴随血脑屏障(BBB)向血-肿瘤屏障(BTB)的转化[15]
总结与展望
脑转移始终是非小细胞肺癌(NSCLC)临床诊疗中难以逾越的“瓶颈”。它不仅是患者生存获益的独立负面预后因素,更伴随严重的神经系统后遗症——认知障碍、运动功能受损、癫痫及颅内高压,导致患者生活质量(QoL)发生断崖式恶化 。从卫生经济学维度考量,密集的影像学随访、放疗干预及复杂的住院管理,造成了巨大的医疗资源消耗与社会经济负担 。因此,探索一种既能高效清除颅内既有病灶,又能阻断新发转移的系统性“脑保护”策略,已成为肺癌精准治疗的核心攻关方向。
依沃西作为全球首创的PD-1/VEGF 双特异性抗体,凭借“靶免一体”的高效协同机制,在 NSCLC 脑转移领域实现了从“被动治疗”向“系统性脑保护”的治疗范式跨越。临床研究证实,对于基线伴脑转移的患者,依沃西可显著延长颅内PFS,降低颅内进展风险;对于基线无脑转移的患者,依沃西通过修复血脑屏障并阻断肿瘤趋化信号,展现出卓越的“脑保护”价值,可显著降低颅内进展累积发生率,显著延缓脑转移发生,颅内进展发生率维持在3%的低水平[1]。因此,临床上对于EGFR-TKI经治人群的全程治疗策略中,依沃西方案应及早介入,能最大程度控制并降低脑转移风险、显著延长总生存期。对于驱动基因阴性晚期NSCLC的一线治疗,在患者体能状态和免疫功能尚佳的早期阶段采用依沃西方案也能发挥更大抗肿瘤作用,并凭借其“脑保护”特性有效降低远期脑转移风险。依沃西方案的临床应用,标志着 NSCLC治疗正式进入了“主动脑保护”的新时代,为患者实现长期颅内稳定与生活质量获益的更高质量长生存点亮了曙光。
关于康方生物
康方生物(9926.HK)是一家集研究、开发、生产及商业化全球首创或同类最佳创新生物新药于一体的领先企业。自2012年成立以来,公司始终以患者为中心,以临床价值为导向,打造了独有的端对端康方全方位新药研究开发平台,建立了以Tetrabody双抗/多抗技术、Dual-Shield ADC、Dual-Lock TCE、Tissue-Smart siRNA、细胞治疗及Flex-Nano mRNA等技术为核心的研发创新体系,国际化标准的GMP生产体系和运作模式先进的商业化体系,成为了在全球范围内具有竞争力的生物医药创新公司。
公司已开发了50个以上用于治疗肿瘤、自身免疫、炎症、代谢疾病等重大疾病的创新候选药物,27个新药已进入临床(包括15个双抗/多抗/双抗ADC),7个新药已在商业化销售,2个新药4个适应症的上市申请处于审评审批阶段。
康方生物是全球迄今唯一拥有2个肿瘤免疫双抗新药的制药公司:
2022年6月,公司全球首创的PD-1/CTLA-4双抗卡度尼利获批上市,是全球首个获批的肿瘤免疫治疗双抗新药,也是中国第一个双特异性抗体新药。目前卡度尼利一线治疗胃癌、一线治疗宫颈癌和治疗复发/转移性宫颈癌的适应症已获批,12个注册性/III期临床正在开展。
2024年5月,公司全球首创的PD-1/VEGF双抗新药依沃西获批上市,用于EGFR-TKI治疗进展的局部晚期或转移性nsq-NSCLC,成为全球首个获批的“肿瘤免疫+抗血管生成”机制双抗新药。同期,依沃西在与全球“药王”帕博利珠单抗的随机、双盲、对照一线治疗PD-L1阳性NSCLC的“头对头”III期临床研究中获得显著阳性结果,依沃西可降低患者疾病进展/死亡风险达49%,依沃西成为全球首个在头对头III期临床研究中证明疗效显著优于“药王”帕博利珠单抗的药物。基于该研究结果,依沃西该项适应症于2025年4月获批上市,成为一线肺癌治疗新的标准治疗方案,为患者提供全新更优的“去化疗”选择。目前依沃西有15项注册性/III期临床已开展/启动,包括5项国际多中心注册性III期临床研究。
2024年12月,卡度尼利和依沃西均通过医保谈判被纳入国家新版医保目录。2025年12月,除派安普利新获批的一线肝细胞癌适应症,康方生物5个自主商业化自研新药的其余全部获批适应症均已纳入国家医保目录。
此外,基于公司在肿瘤免疫双抗领域取得的全球领先优势,公司正全力推进IO2.0+ADC2.0全球战略,构建“跨代”式国际竞争优势。目前,公司自主研发的首个双抗ADC药物Trop2/Nectin4 ADC(AK146D1)、新一代Her3 ADC(AK138D1)联合卡度尼利和依沃西治疗实体瘤II期临床研究正在开展。此前,该组合疗法 I 期临床已获美国 FDA 和中国 NMPA 批准开展。后续一系列自研新一代ADC/双抗ADC也将相继进入临床开发阶段。这将助力公司产品组合在全球范围内建立“跨代”式的竞争战略优势。
国际市场开发是康方生物核心发展战略,继2015年开中国先河将自主研发的CTLA-4单抗权益许可给默沙东公司之后,2022年12月,公司再次创造中国纪录,以50亿美金+2位数百分比销售提成的方案,将依沃西部分海外权益许可给美国Summit公司,该合作创下了彼时中国新药对外许可的最高交易金额纪录。此外,派安普利单抗治疗鼻咽癌的两项适应症于2025年4月获得美国食品药品监督管理局(FDA)批准上市。
公司自身免疫相关疾病及中枢神经系统疾病治疗领域也已全面进入商业化发展阶段:伊努西单抗(PCSK9)治疗高胆固醇血症两项适应症获批销售;依若奇单抗(IL-12/IL-23)治疗中重度斑块状银屑病成人患者适应症获批上市销售;此外,古莫奇单抗(IL-17)和曼多奇单抗(IL-4R)多项III期临床研究成功,正处于上市审评阶段。公司各领域产品协同效应和战略组合力进一步提升。
康方生物期望通过高效及突破性的研发创新,开发国际首创及同类药物最佳疗法的新药,为全球患者提供更优疾病解决方案,成为全球领先的生物制药企业。
参考文献:
[1]Le X, et al. Intracranial efficacy of ivonescimab plus chemotherapy in epidermal growth factor receptor (EGFR) tyrosine kinase inhibitor-resistant, EGFR-mutated non-small cell lung cancer in the HARMONi study. 2026 ELCC. 15P.
[2]Ye LY, et al. The structure of blood-tumor barrier and distribution of chemotherapeutic drugs in non-small cell lung cancer brain metastases. Cancer Cell Int. 2021 Oct 24;21(1):556.
[3]Souza VGP, et al. Advances in the Molecular Landscape of Lung Cancer Brain Metastasis. Cancers (Basel). 2023 Jan 24;15(3):722.
[4]Zhao W, et al. Epidermal growth factor receptor mutations and brain metastases in non-small cell lung cancer. Front Oncol. 2022 Nov 15;12:912505.
[5]HARMONi-A Study Investigators; Fang W, et al. Ivonescimab Plus Chemotherapy in Non-Small Cell Lung Cancer With EGFR Variant: A Randomized Clinical Trial. JAMA. 2024 Aug 20;332(7):561-570.
[6]Zhang L,et al. Final Overall Survival Analysis : HARMONi-A StudyIvonescimab + chemotherapy versus ChemotherapyIn patients with EGFR-mutant NSCLC progressed on EGFR TKI.2025 SITC. 1348
[7]ZhangL, et al. Intracranial Progression-Free Survival With Ivonescimab Compared to Placebo in the HARMONi-A Trial of Pattents With Previously Treated EGFR Mutatton–Posittve Non–Small Cell Lung Cancer. 2024 ESMO IO. 134P.
[8]Xiong A, et al. Ivonescimab versus pembrolizumab for PD-L1-positive non-small cell lung cancer (HARMONi-2): a randomised, double-blind, phase 3 study in China. Lancet. 2025;405(10481):839-849.
[9]中国医疗保健国际交流促进会,中国医师协会肿瘤医师分会. 肺癌脑转移中国治疗指南(2026版).中华肿瘤杂志,2026, 48(1):44-78.
[10]中国医药教育协会肺癌医学教育专业委员会, 北京医学奖励基金会肺癌医学青年专家委员会脑转移协作组. 中国驱动基因阳性非小细胞肺癌脑转移临床诊疗指南(2025 版). 中国肺癌杂志, 2025, 1(28): 1-21.
[11]Engelhardt B, et al. Capture, crawl, cross: the T cell code to breach the blood-brain barriers. Trends Immunol. 2012 Dec;33(12):579-89.
[12]Avraham, H, et al. VEGF-A-mediated disruption of the blood-brain barrier in brain metastasis. Cancer Research, 2010, 70(21), 8335-8344.
[13]Steeg, P. Targeting the blood-brain barrier in brain metastasis. Nature Reviews Clinical Oncology, 2016, 13(8), 478-492.
[14]Desgrosellier, et al. Integrins in cancer: biological implications and therapeutic opportunities. Nature Reviews Cancer, 2010, 10(1), 9-22.
[15]Steeg PS. The blood-tumour barrier in cancer biology and therapy. Nat Rev Clin Oncol. 2021 Nov;18(11):696-714.