中国苏州,2026年4月20日——基石药业(股票代码:2616.HK),一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,今日宣布公司在4月17日至22日召开的美国癌症研究协会(AACR)年会上展出包括CS5007(EGFR/HER3 ADC)、CS5006(ITGB4 ADC)、CS5008(DLL3/SSTR2 ADC)在内三项自主研发管线的临床前最新研究成果。
基石药业自主研发ADC技术平台
本次AACR展出的CS5007(EGFR/HER3 ADC)、CS5006(ITGB4 ADC)、CS5008(DLL3/SSTR2 ADC)皆出自基石药业自主开发的专有抗体偶联药物(ADC)技术平台,该平台具有以下特征:
-
高稳定性与精准释放:采用基石药业专有的CSL20连接子,具备极强的亲水性,提升了循环稳定性;并能通过串联切割机制(经β-葡萄糖醛酸酶和组织蛋白酶协同作用)实现高效的肿瘤选择性有效载荷释放。
-
强效载荷:使用依喜替康(Exatecan)作为有效载荷,一种经临床验证的高效拓扑异构酶I抑制剂,具有强效的旁观者效应,有效降低多药耐药的敏感性。
CS5007 EGFR/HER3 双特异性ADC
【摘要标题】:Preclinical efficacy and safety of CS5007, an EGFR×HER3 dual-targeting antibody-drug conjugate with a topoisomerase 1 inhibitor payload
【展示形式】:壁报
【展示地点】:第17区,展板#11
【展示时间】:2026年4月20日(星期一)9:00—12:00 太平洋时间
【壁报编号】:1823
EGFR和HER3作为ErbB家族的重要成员,是多种人类上皮恶性肿瘤中频繁共表达的关键致癌驱动因子。尽管单靶点EGFR疗法已作为标准治疗被广泛应用,但由HER3代偿性信号传导和异源二聚化引发的适应性耐药,严重限制了这类疗法的长期临床获益。因此,同时靶向EGFR和HER3成为一种极具潜力的突破策略:该方法可通过物理阻断受体二聚化,全面抑制ErbB信号网络(包括PI3K/Akt和MEK/ERK通路),进而有效克服复杂的肿瘤异质性。CS5007旨在通过协同靶向EGFR以及作为家族广泛二聚化核心的HER3,全面阻断除HER2同源二聚体以外的几乎所有HER家族致癌受体复合物,从而有效切断驱动肿瘤生存与增殖的级联信号网络。
CS5007是一种双特异性ADC,由抗EGFR/HER3人源IgG1抗体、基石药业专有的亲水性CSL20连接子,以及临床验证的拓扑异构酶I抑制剂Exatecan组成。该药物采用半随机偶联将连接子载荷与抗体结合,其平均药物抗体比(DAR)约为4。
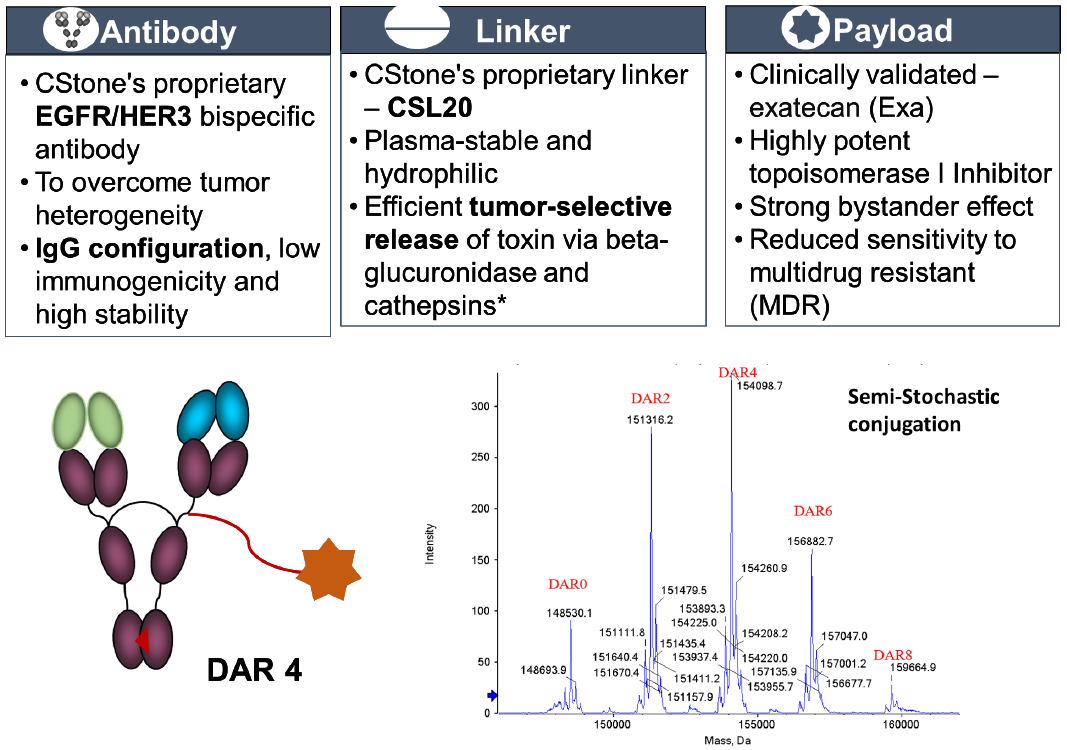
注:* β-葡萄糖醛酸酶仅在细胞内发挥作用,并在肿瘤细胞中高表达。
卓越的分子稳定性
CS5007在体外血浆稳定性测试中表现优异,其稳定性优于DS-8201(德曲妥珠单抗)。在血浆中孵育7天后,其游离载荷的释放率低于0.5%,降低了脱靶毒性风险。
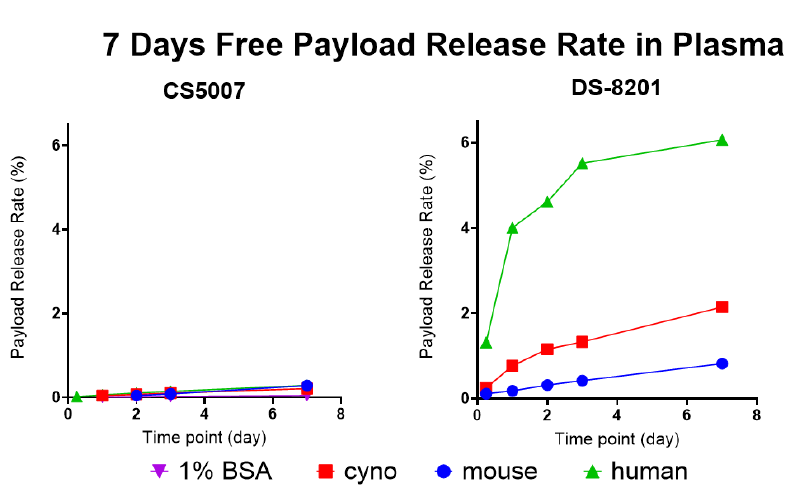
双重信号通路阻断机制
通过蛋白免疫印迹法(Western Blots),在由双靶点配体(TGF-α/EGF与NRG1β1)模拟的持续刺激微环境中,评估了CS5007的裸抗J17对不同人肿瘤细胞系的信号阻断能力。J17能够通过双重靶向EGFR和HER3,实现对下游信号通路(包括Akt和MAPK通路)的强效抑制作用。相比于BL-B01D1的裸抗SI-B001,J17具有更优越的药效学特征:实验显示,在A431和FaDu细胞中,SI-B001无法有效阻断HER3/Akt信号,J17能凭借其特有的双重阻断机制克服单靶点局限,表现出极佳的抑制活性。
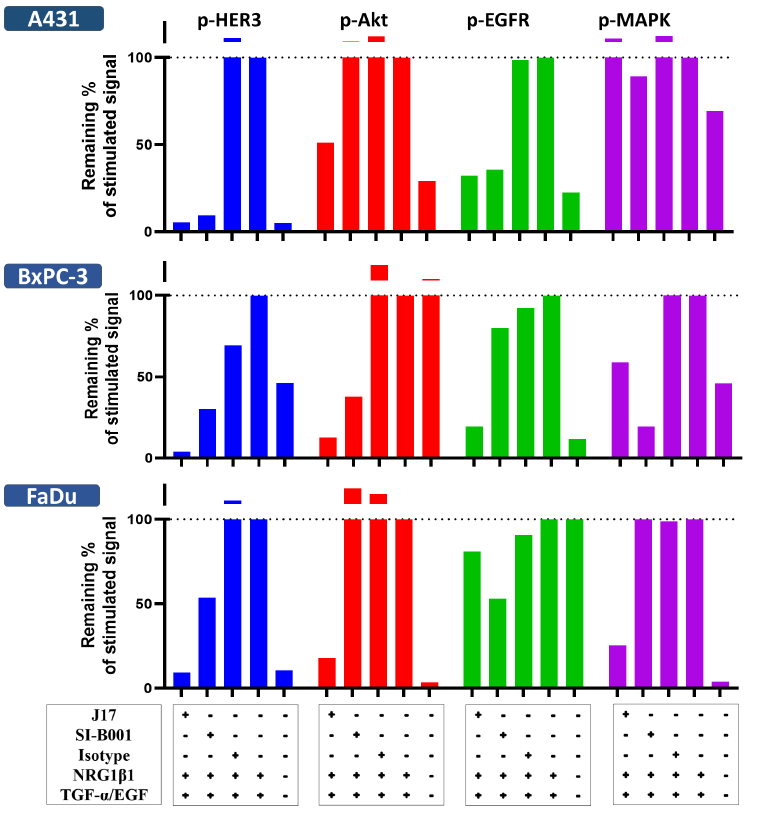
注:1)J17 为CS5007裸抗。2)BL-B01D1的裸抗SI-B001是根据已发表文献合成的。基线信号定义为使用收集自预刺激的肿瘤细胞(包括 BxPC-3、FaDu和A431)的细胞裂解液所检测到的信号。
精准靶向与快速内吞
基于Incucyte®活细胞成像评价显示,CS5007在6种肿瘤细胞系中均表现出与裸抗J17一致的靶点介导内化特征:呈浓度依赖性快速被摄取并高效进入溶酶体(阴性对照均无信号)。具体而言,其内化起效极快(在MDA-MB-468细胞中0小时即有信号,4小时达峰);且即使在EGFR低表达细胞(SW620)中,CS5007仍能通过HER3介导实现快速内化,依然保持了高效的药物递送能力。
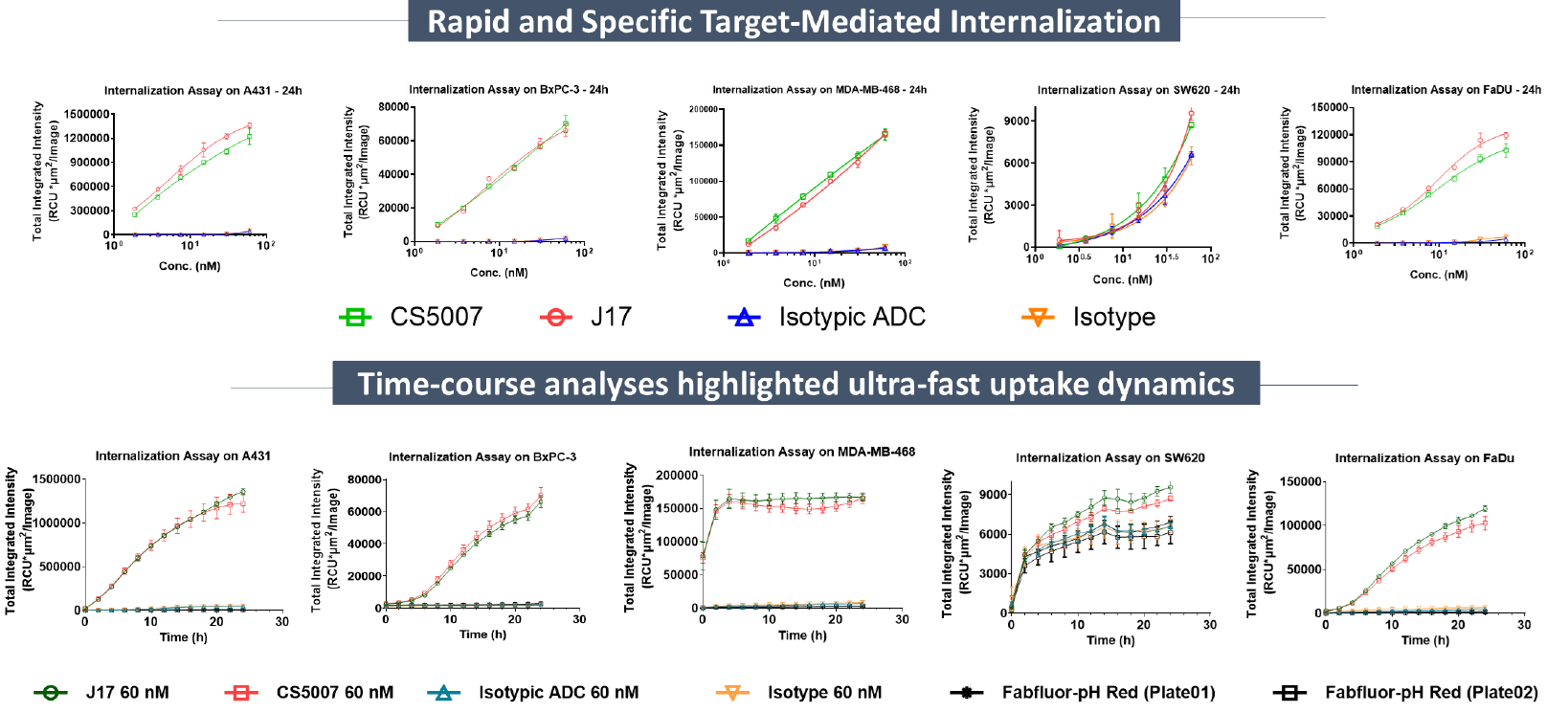
注:J17为CS5007裸抗。
强效且广谱的体外抗肿瘤活性
采用CellTiter-Glo®(CTG)发光法评价了CS5007对多种人肿瘤细胞系的体外增殖抑制作用。实验证实,其在包括非小细胞肺癌(NSCLC)、鳞状细胞癌(SCC)、结直肠癌(CRC)、头颈鳞癌(SCCHN)、胰腺癌(PANC)、及乳腺癌(BC)多种肿瘤细胞系中均表现出纳摩尔级别的强效细胞杀伤活性,且呈抗原依赖性。
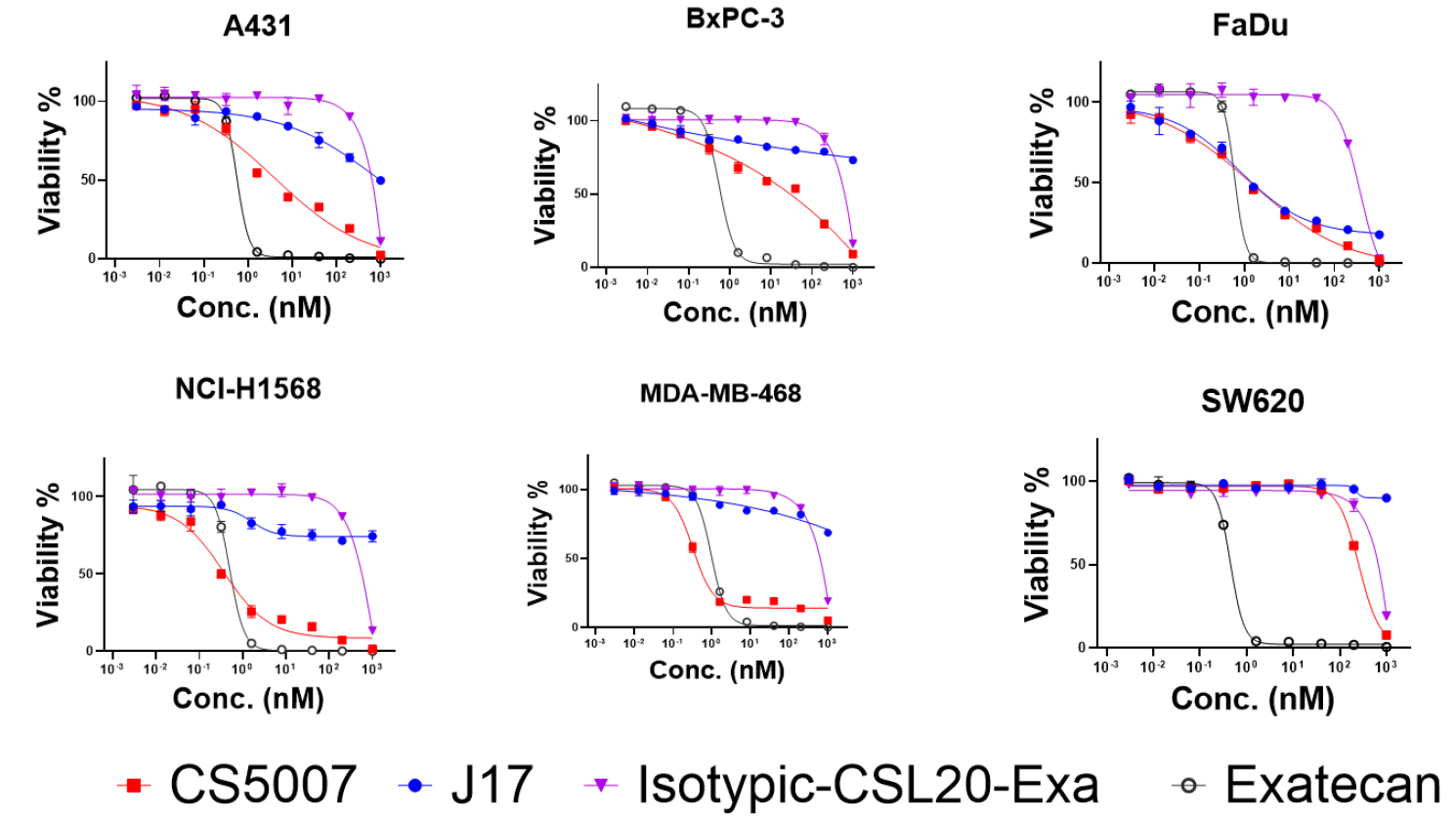
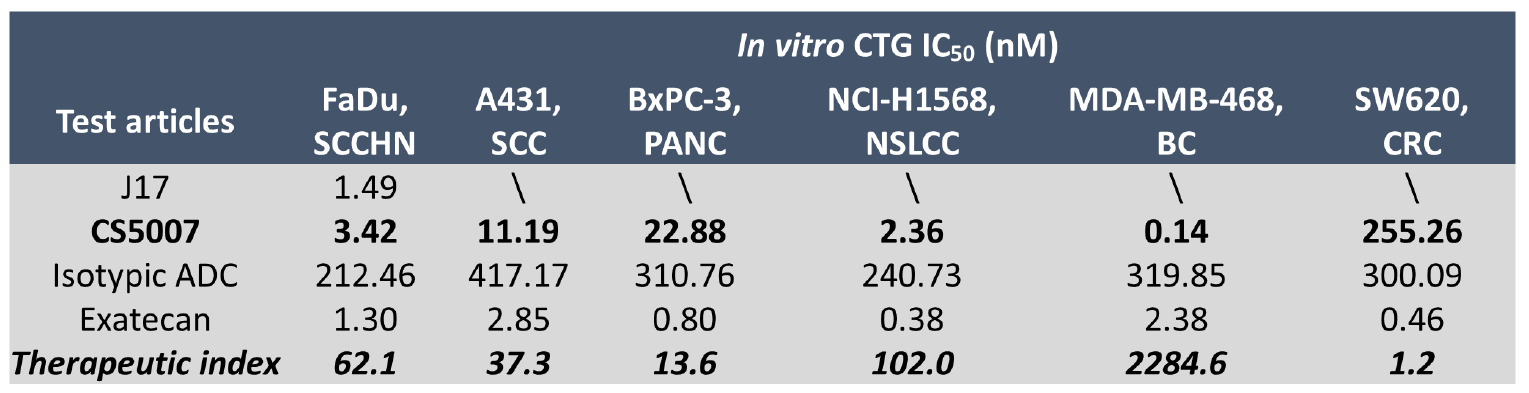
注:治疗指数 (TI) 的计算公式如下:TI = 同型对照 ADC 的 IC50 / CS5007 的 IC50
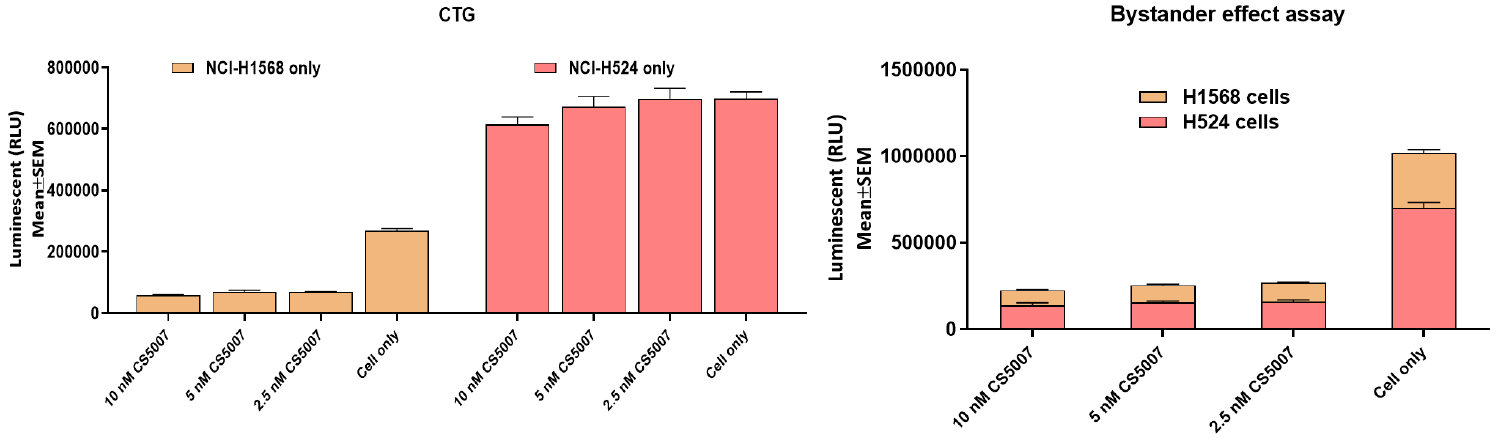
显著的旁观者杀伤效应
通过结合CTG与FCM(流式细胞术)分析,研究证实了CS5007具备卓越的旁观者杀伤效应。在单培养体系中,CS5007可对H1568细胞产生细胞毒性,而对HCI‑H524细胞无杀伤作用。在进一步构建的共孵育体系中,FCM的精确定量分析表明,CS5007在靶向杀伤阳性细胞(NCI-H1568)的同时,能够有效导致共同孵育的抗原阴性细胞(NCI-H524)死亡。这一特性使其能够有效应对实体瘤内部靶抗原表达的空间异质性挑战。
广谱的体内抗肿瘤活性与耐药模型突破
-
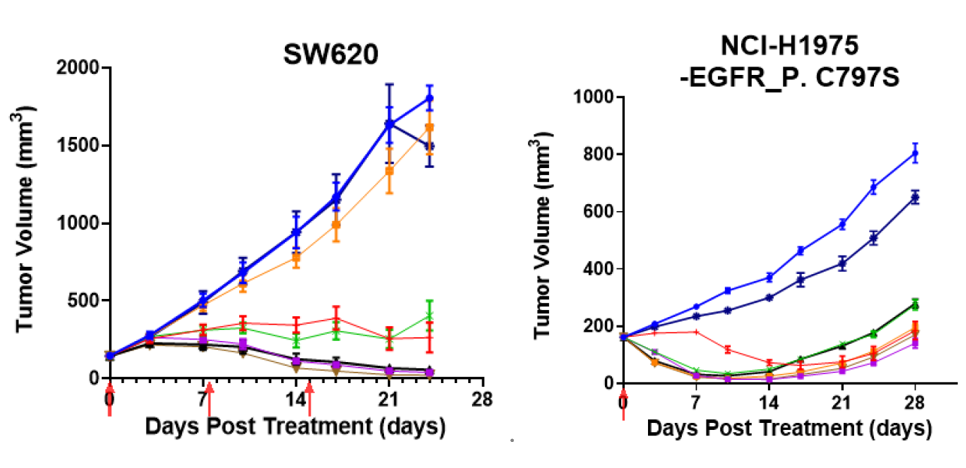
广谱有效:在源自多种肿瘤,包括NSCLC、CRC、BC、SCCHN和SCC的细胞系来源异种移植(CDX)模型中抑制了肿瘤生长。
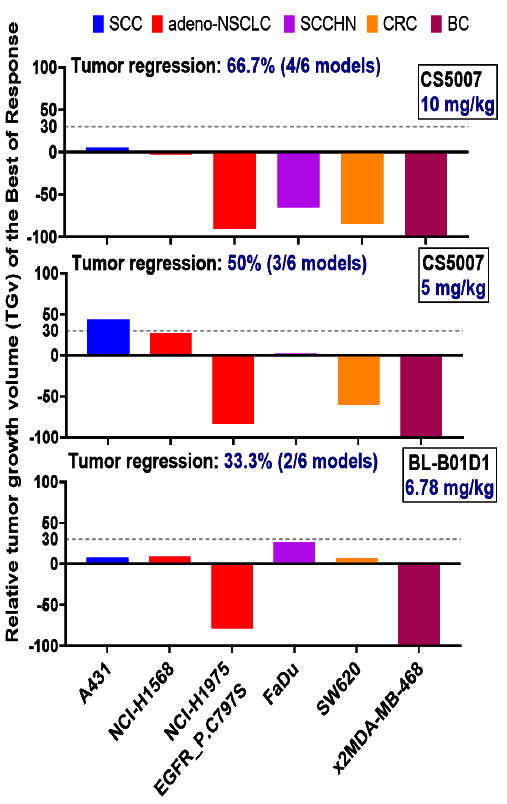
注:1)BL-B01D1,为根据公开文献数据合成的参考分子,采购于MCE。2)BL-B01D1的剂量设定为6.78 mg/kg(除了在FaDu模型中给药剂量为5 mg/kg),以确保其与10 mg/kg CS5007所携带的有效载荷具有相同的摩尔数。3)通过根据以下公式计算相对肿瘤生长体积(TGv,%)来评估抗肿瘤活性:如果在TGv计算日,抗体药物结合物(ADC)治疗组小鼠的平均肿瘤体积小于给药时(Ti < T0),则TGv(%) = 100 × (Ti - T0)/T0;如果不是,则TGv(%) = 100 × (Ti - T0)/(Vi - V0),其中Ti和Vi分别是TGv计算日治疗组和溶媒对照组的平均肿瘤体积;T0和V0分别是给药时治疗组和溶媒对照组的平均肿瘤体积。根据该公式,我们将TGv < 0定义为肿瘤消退。4)所展示的数据为第1周期治疗(7天)后的汇总最佳疗效。
-
耐药突破:在奥希替尼耐药的H1975模型(EGFR C797S突变)中依然有效。
-
低EGFR优势:在EGFR低表达、HER3高表达的SW620模型中,CS5007实现了肿瘤清除,而对照药物BL-B01D1在此模型中未展现出显著活性。
优异的PK/PD特征
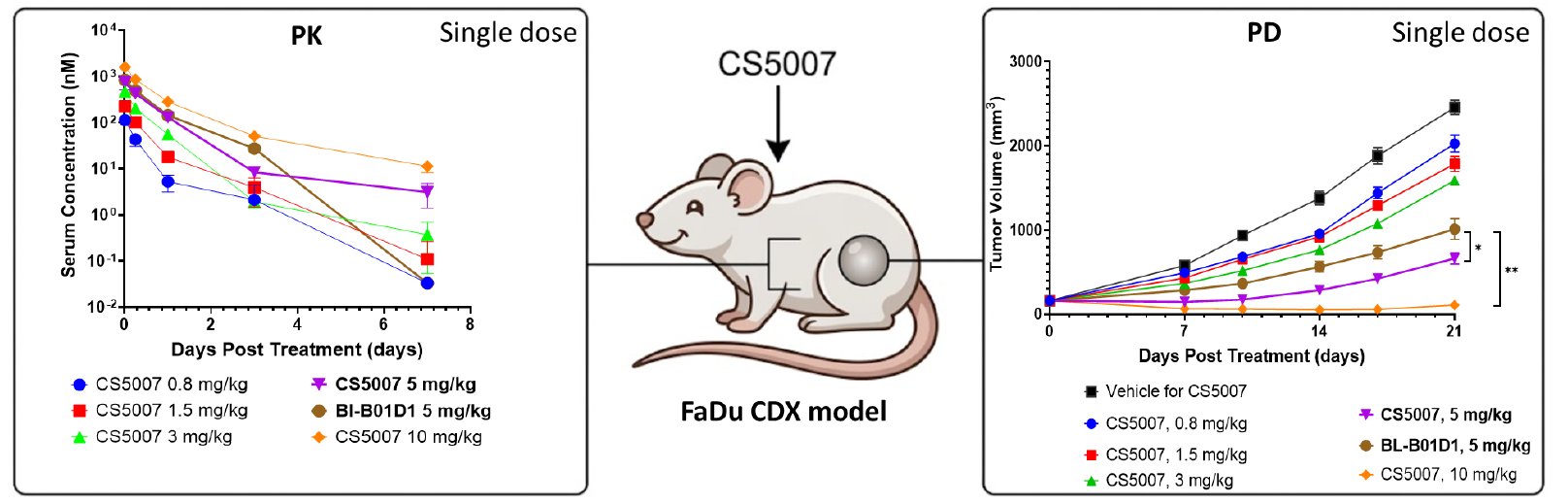
在小鼠模型中,CS5007展现出优于BL-B01D1的药代动力学(PK)/药效动力学(PD)特征:
-
更强效:在5 mg/kg剂量下,两者暴露量(AUC)相当,但CS5007组的肿瘤消退程度显著优于BL-B01D1(p<0.05)。
-
更长效:CS5007在各剂量组的半衰期均维持在约20小时,而BL-B01D1在5 mg/kg剂量下的半衰期约为10小时。
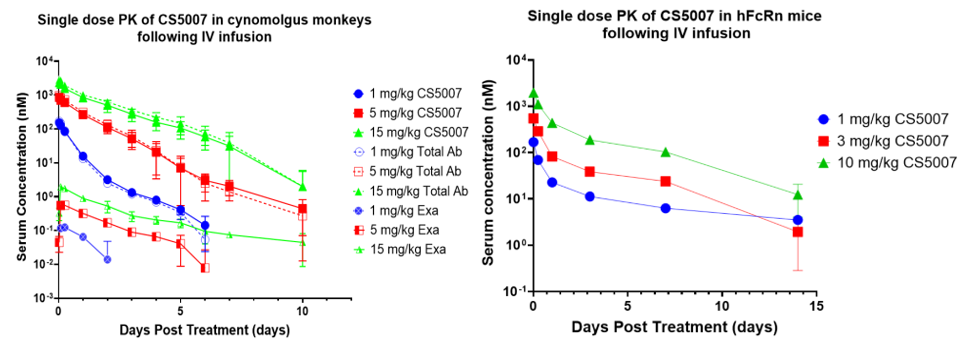
良好的安全性与耐受性
在非人灵长类动物(NHPs)中,CS5007表现出与同类EGFR靶向药物一致的良好代谢稳定性,NHP半衰期约2天,与报道的EGFR靶向的抗体或ADC在NHP中的PK相当。在人源FcRn转基因小鼠中,半衰期约2.5-8天。
-
毒性可控:GLP毒理研究确定其最高非严重毒性剂量(HNSTD)为30 mg/kg。
-
安全性窗口:未观察到致死性毒性,皮肤毒性仅出现在高剂量组,整体安全性风险可控,具有较宽的治疗窗口。
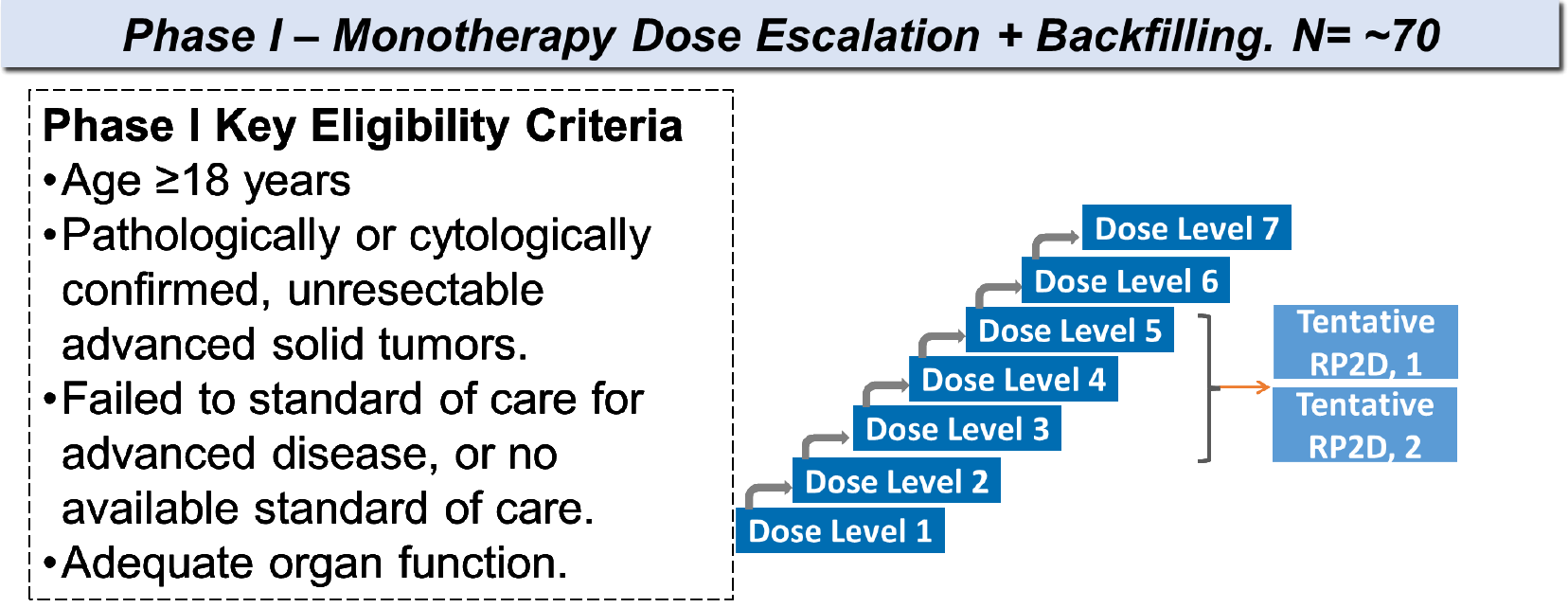
I期临床试验规划
基石药业计划于2026年上半年启动CS5007的新药临床试验(IND)申请。CS5007-101研究是一项单药剂量递增与扩展填充研究,旨在评估CS5007在经标准治疗后疾病进展、不符合标准治疗条件或无有效治疗方案晚期实体瘤患者中的安全性及二期推荐剂量(RP2D),预计入组70例患者。
总结CS5007(EGFR/HER3 ADC)
CS5007是一款极具潜力的双特异性ADC药物,兼具强效的抗肿瘤活性以及良好的安全性与PK特征。关键的临床前研究表明,CS5007不仅具备极高的结合亲和力,能在具有不同EGFR和HER3表达水平的肿瘤细胞中介导快速内化,还能有效阻断EGFR与HER3的下游信号传导,从而强效抑制肿瘤细胞增殖。此外,该药物展现出强大的旁观者效应,抑制肿瘤生长。综上所述,这些详实的临床前数据为推动CS5007在实体瘤领域的后续临床开发提供了坚实的科学依据。
关于基石药业
基石药业(香港联交所代码: 2616)成立于2015年底,是一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,致力于满足中国和全球患者的殷切医疗需求。截至目前,公司已成功上市4款创新药、获批21项新药上市申请(NDA)以及9项适应症。当前研发管线均衡配置了抗体偶联药物(ADC)、多特异性抗体、以及免疫疗法和精准治疗药物在内的16款候选药物。同时,基石药业拥有一支资深管理团队,“全链条”覆盖临床前探索、临床转化、临床开发、药物生产、商务拓展、商业运营等关键环节。