上海,2026年4月22日 —— 复宏汉霖(2696.HK)今日宣布,公司在2026年美国癌症研究协会(AACR)年会上以壁报形式首次公布了其在研新型CD3×CD28×STEAP1靶向三特异性T细胞衔接器(T Cell Engager, TCE)HLX3902的临床前研究数据。公司正持续推进该平台在更多“免疫荒漠”型实体瘤中的拓展应用,基于该平台已孵化了超过5款早期创新分子。
其中HLX3901(DLL3xDLL3xCD3xCD28四特异性抗体)和HLX3902(STEAP1×CD3×CD28 三特异性抗体)作为该领域的代表性资产,分别聚焦小细胞肺癌和前列腺癌等实体瘤的治疗,已加速推进至IND批准/受理阶段。值得一提的是,基于该平台开发的另一款分子HLX3901(DLL3xDLL3xCD3xCD28四特异性TCE)亦在临床前研究中展现出同类最优的治疗潜力,印证了该平台在实体瘤治疗领域的高效产出和可拓展性。
自建多特异性TCE平台:引入CD28共刺激信号,重塑实体瘤“免疫沙漠”——优效,更宽的治疗窗口
实体瘤治疗中,肿瘤微环境(TME)内T细胞浸润不足及免疫抑制状态是制约TCE疗效的关键瓶颈。为突破这一挑战并优化TCE在实体瘤中的治疗窗口,复宏汉霖开发了引入CD28共刺激信号的多特异性TCE平台。该平台通过同时提供CD3激活信号(第一信号)与CD28共刺激信号(第二信号),从而实现T细胞的定向募集与有效激活,并增强其活化、增殖水平,显著增强了T细胞在抑制性肿瘤微环境中的持久杀伤能力。

复宏汉霖对该TCE平台的机制设计进行了系统性优化:CD3激活采用靶点依赖性机制,在无肿瘤靶抗原存在时,不触发CD3激活信号,从而降低脱靶激活风险;CD28共刺激信号采用条件性激活设计,仅在CD3信号被触发后发生,并与CD3协同激活调控T细胞。此外,通过将CD3和CD28的结合区域置于TCE分子的同侧,促进其与同一T细胞上的CD3和CD28进行顺式结合(cis-结合),以减少非特意性的T细胞激活和互相攻击,进而有效控制了系统性毒性风险,实现了更宽的治疗窗口。
AACR展示:HLX3902(CD3×CD28×STEAP1 三抗TCE)在前列腺癌中实现强效持久抗肿瘤应答
STEAP1在前列腺癌中呈高表达,是理想的肿瘤特异性靶点。HLX3902是一款靶向STEAP1、CD3和CD28的三特异性TCE,在精准靶向前列腺癌中高表达STEAP1的同时,实现T细胞CD3与CD28的共激活,具备同类最优的治疗潜力,目前其IND申请已获中国国家药品监督管理局药品审评中心(CDE)受理。
-
体外研究表明,HLX3902可诱导靶点依赖性的T细胞活化及细胞毒性
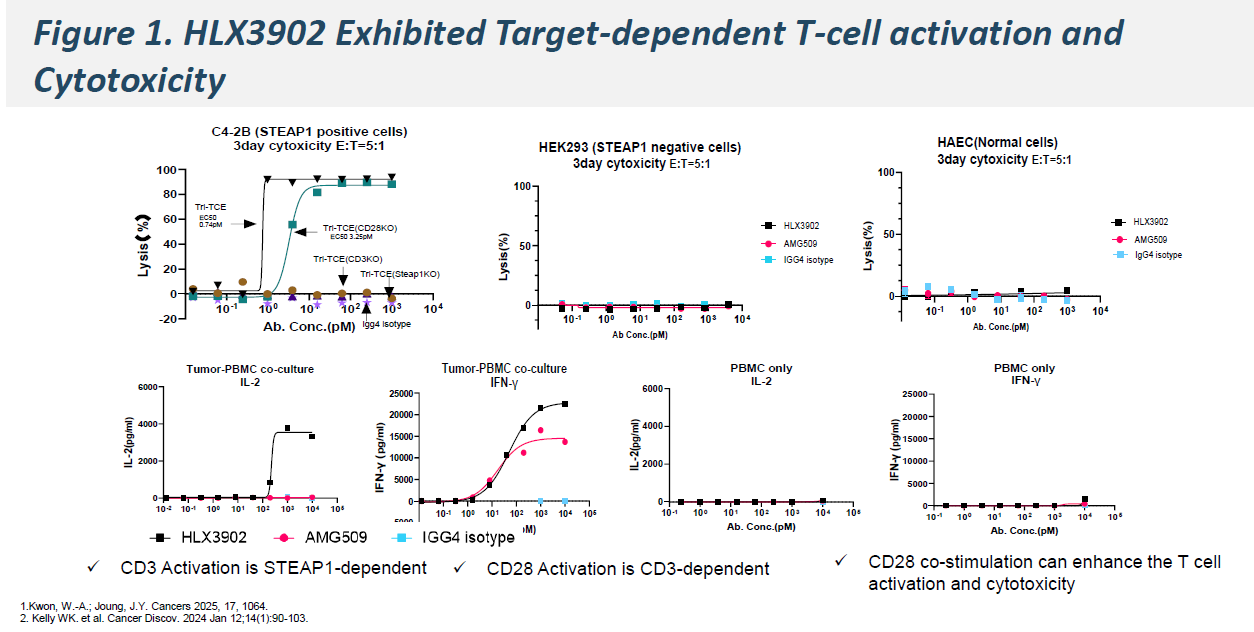
图1:HLX3902的靶点依赖性T细胞活化和细胞毒性数据
-
与仅靶向CD3的双特异性T细胞衔接器相比,HLX3902在低效应细胞/靶细胞比(E/T ratio)条件下(1:5-1:10)显示出更强的细胞毒活性。
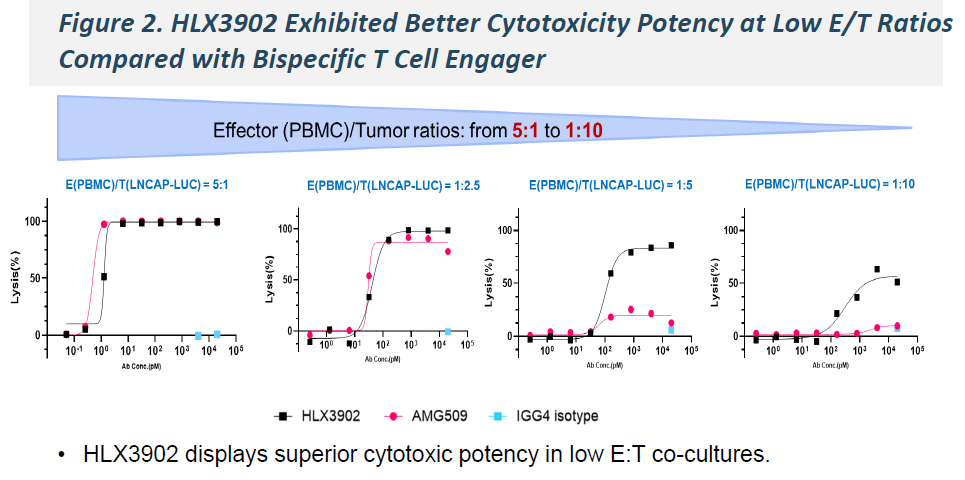
图2:HLX3902与双特异性TCE在低效靶比下的细胞毒性对比
-
在重复抗原刺激模型中,含有CD28共刺激信号的三特异性抗体HLX3902较CD3双特异性抗体表现出更持久的细胞毒性。该效应伴随更持续的T细胞活化、增殖,以及记忆T细胞扩增效应【包括中央记忆性T细胞(TCM)和效应记忆性T细胞(TEM)】。
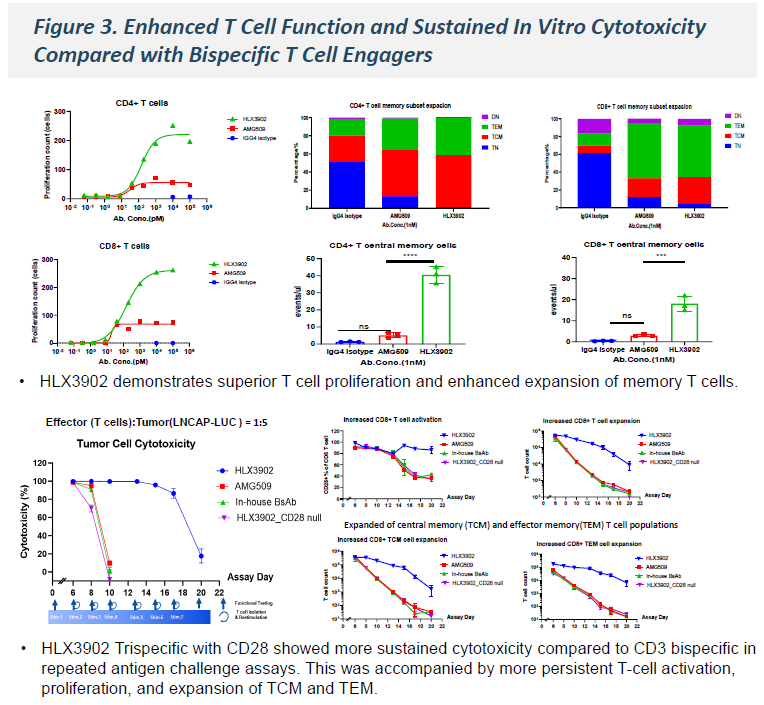
图3:与双特异性T细胞衔接器相比,HLX3902增强的T细胞功能及持久的体外细胞毒作用
-
体内抗肿瘤活性:在C4-2/hPBMX异种移植模型中,HLX3902表现出较双特异性TCE更强的抗肿瘤活性。组织学分析提示,增强的疗效与肿瘤微环境中T细胞浸润增加、T细胞活化增强及T细胞持久性提高相关。
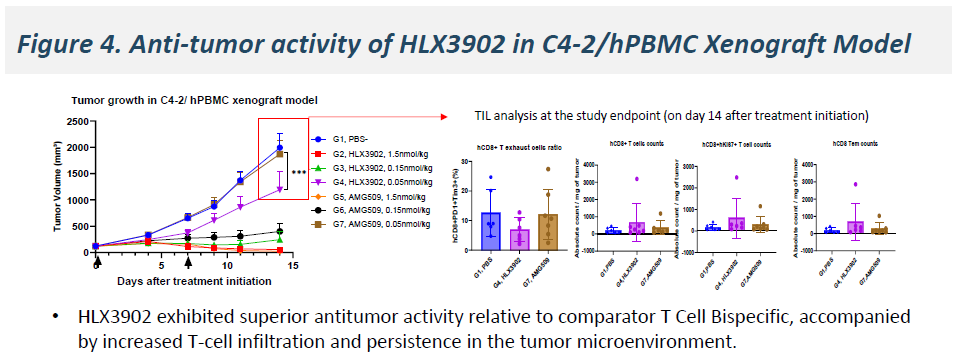
图4:HLX3902在C4-2/hPBMX异种移植模型中的抗肿瘤活性
-
体内抗肿瘤活性:在阿比特龙耐药的患者来源异种移植(PDX)/hPBMX模型中,HLX3902在0.05 nmol/kg(0.01 mg/kg)剂量下表现出显著优于AMG509的抗肿瘤疗效,该剂量为AMG509目标临床剂量范围内。
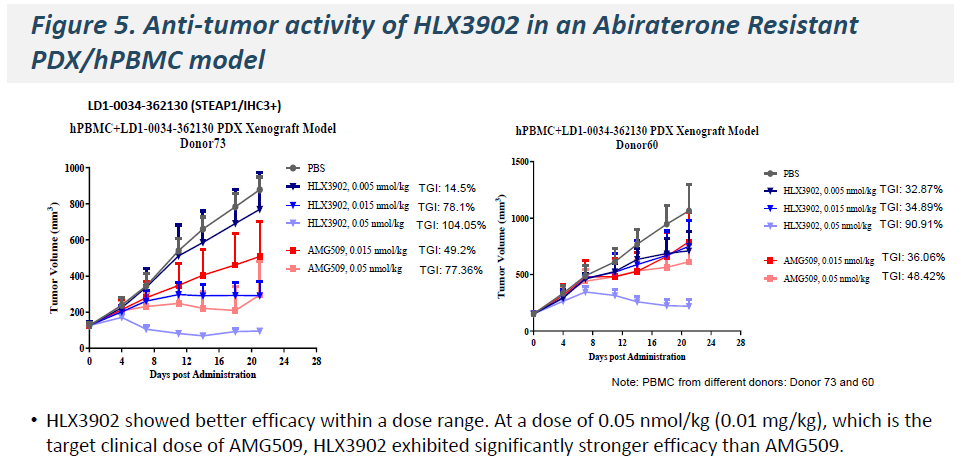
图5:HLX3902在阿比特龙耐药PDX/hPBMX模型中的疗效
-
安全性结果:在食蟹猴中开展的一项初步药代动力学及毒性研究中,HLX3902耐受性良好,安全性可控,支持其进一步临床开发。
AET 2025首次发布: AI驱动设计的新一代实体瘤TCE HLX3901(DLL3xDLL3xCD3xCD28四抗TCE)
HLX3901是基于该平台开发的另一款潜力TCE分子HLX3901为靶向DLL3双表位、CD3和CD28的四特异性抗体,其IND申请已于2026年3月获得国家药品监督管理局(NMPA)批准。HLX3901结合了公司AI驱动的智能药物设计与TCE平台技术,通过精巧的分子设计,该产品兼具持久的特异性T细胞激活、攻克低T细胞浸润肿瘤及显著降低细胞因子释放综合征(CRS)等多重优势,旨在克服第一代TCE在实体瘤治疗中的主要障碍。
-
HLX3901采用DLL3双表位设计,可同时结合DLL3两个不同表位以增强结合能力,增强靶向药效。
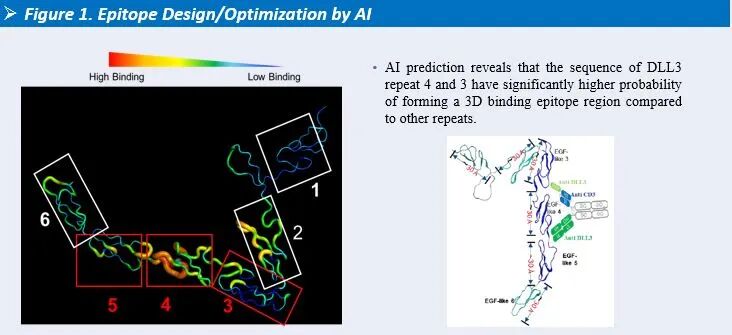
图1: HLX3901分子设计与人工智能驱动的表位优化
-
在表位发现阶段,复宏汉霖基于AI预测分析筛选DLL3潜在抗体结合区域,确定Repeat 3及Repeat 4为主要表位区域,并据此设计靶向EGF-like 3及EGF-like 4的双表位抗体。体外实验结果显示,该双表位设计在不同效靶比条件下均表现出更优的细胞毒活性。
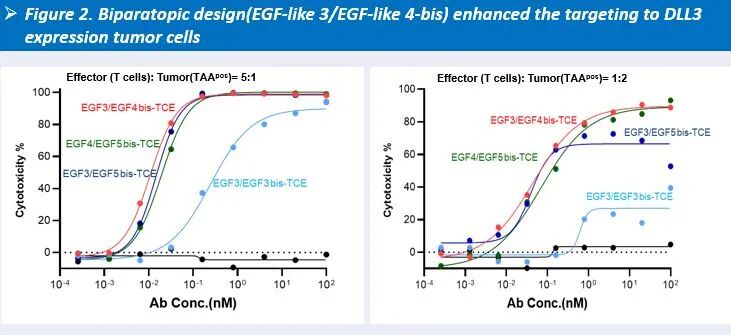
图2:双表位设计(EGF-like 3/EGF-like 4)增强DLL3表达肿瘤细胞靶向性
-
此外,HLX3901采用了Fc段沉默设计,在延长体内半衰期的同时,降低Fc介导的非特异性免疫效应,有助于提升安全性特征。
-
体外研究中:HLX3901在低/靶比条件下表现出优于对照分子(Tarlatamab)的细胞毒性效应。同时,HLX3901能够上调抗凋亡标志物Bcl-xL,并扩增记忆性CD8⁺ T细胞亚群,提示其具有促进T细胞存活及记忆形成的潜力。
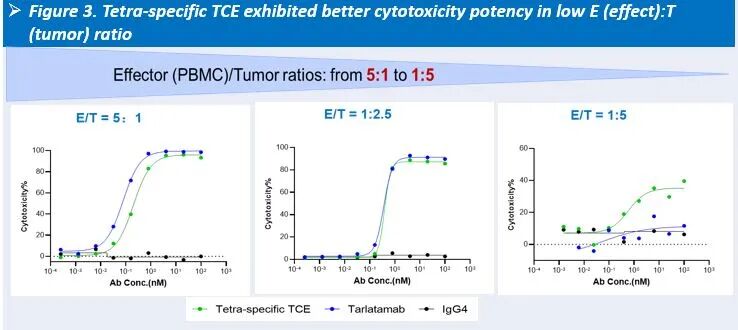
图3:HLX3901与Tarlatamab在低效靶比下的细胞毒性对比数据
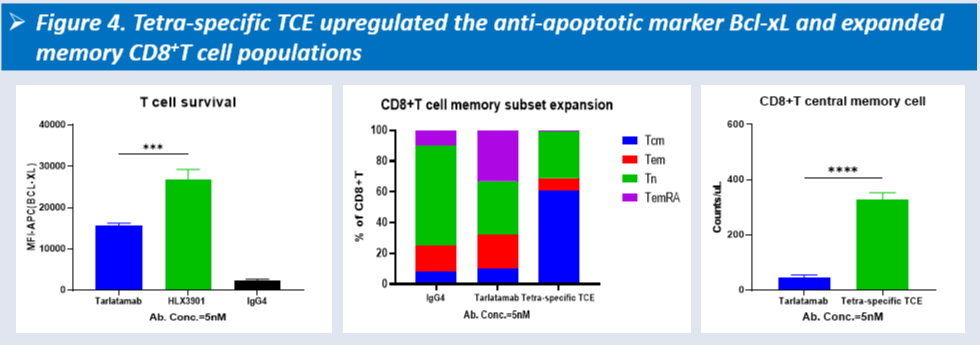
图4:HLX3901诱导Bcl-xL上调及记忆CD8⁺ T细胞扩增
-
体内抗肿瘤活性:在人类泛T细胞重构的SHP77细胞系来源异种移植(CDX)模型中,HLX3901在剂量依赖性条件下表现出显著的肿瘤抑制作用。与已上市的DLL3×CD3双特异性TCE Tarlatamab相比,HLX3901表现出更强且更持久的抗肿瘤活性。
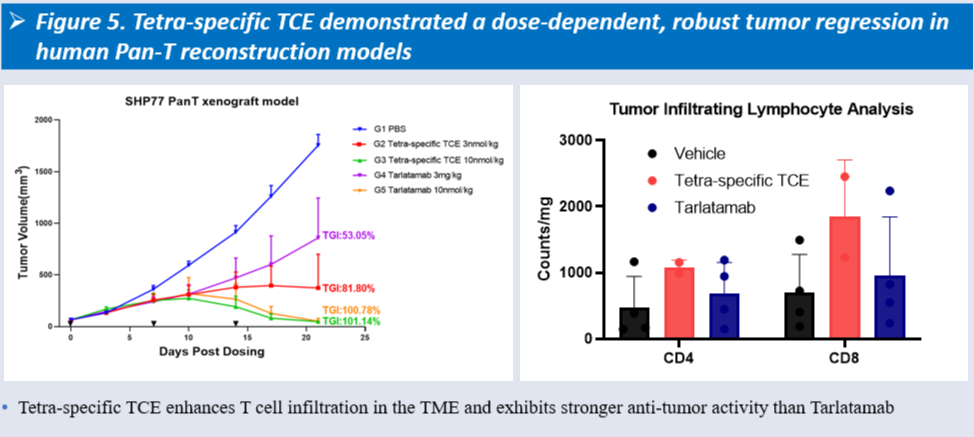
图5:HLX3901可增强T细胞在肿瘤微环境(TME)中的浸润,并展现出较Tarlatamab更强的抗肿瘤活性
-
安全性结果:与Tarlatamab相比,HLX3901在人类外周血单个核细胞(hPBMC)中诱导的非特异性CD4⁺及CD8⁺ T细胞活化显著减弱。在肿瘤细胞(SHP77)与hPBMC共培养条件下,HLX3901组的IL-2、IFN-γ、TNF-α及IL-6释放水平均低于Tarlatamab组,提示其具有更低的CRS风险。在食蟹猴的初步毒性研究中,HLX3901耐受性良好,未观察到不良反应剂量(NOAEL)为10 mg/kg,显示出较宽的治疗窗口。
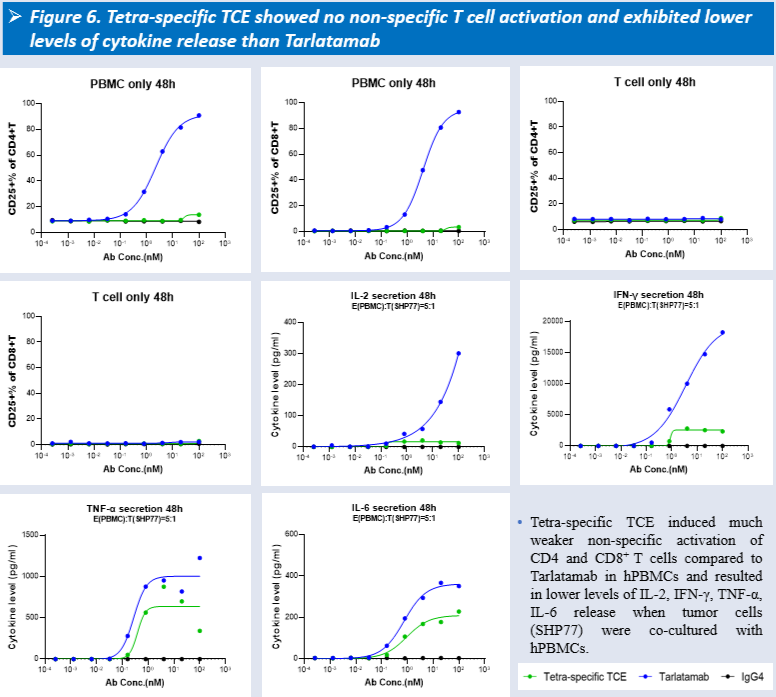
图6:HLX3901未观察到非特异性T细胞激活,且较Tarlatamab细胞因子释放水平更低
基于HLX3901的作用机制,其具备与复宏汉霖自研免疫肿瘤管线联合应用的战略潜力。例如,与抗PD-1单抗斯鲁利单抗(H药汉斯状®)联用,一方面可连接T细胞并诱导其产生针对小细胞肺癌的靶向杀伤,另一方面可解除由PD-L1/PD-1抑制信号通路介导的T细胞耗竭,从而实现协同增效的抗肿瘤疗效。
目前,复宏汉霖已全面建立起涵盖多特异性TCE、抗体偶联药物(ADC)及人工智能驱动早期研发平台等多元创新技术平台。未来,复宏汉霖将继续聚焦未满足的临床需求,依托平台化研发能力,加速创新成果向临床价值的转化,为全球患者提供更多高质量、可负担的治疗选择。
关于复宏汉霖
复宏汉霖(2696.HK)是一家国际化创新生物制药企业,致力于为全球患者提供高品质、可负担的生物药,产品覆盖肿瘤、自身免疫疾病、眼科疾病等领域。自2010年成立以来,公司已构建涵盖全球研发、临床、注册、生产及商业化的全产业链平台,拥有全球员工近4,000人,并在中国、美国和日本等多地设有运营及分支机构。依托生物类似药形成的稳健现金流反哺创新研发,复宏汉霖正稳步迈入“全球化2.0”阶段,持续打造可复制、可持续的全球增长模式。截至2026年初,公司共有10款产品在全球60个国家和地区获批上市,其中7款已在中国获批。在欧美主流生物药市场,复宏汉霖亦取得多项里程碑式突破,已有4款产品获得美国FDA批准、4款产品获得欧盟EC批准,充分体现了公司在研发体系、质量管理及生产能力方面已全面对标国际最高标准。
在创新驱动方面,复宏汉霖依托上海、美国等多地协同布局的研发体系,构建了多元化、平台化的创新技术矩阵,覆盖免疫检查点抑制剂、免疫细胞衔接器(包括多特异性TCE)、抗体偶联药物(ADC)以及AI驱动的早期研发平台等前沿方向。目前,公司拥有50余项处于早期阶段的创新资产,其中约70%具备同类最佳(Best-in-Class)潜力,并在全球同步推进30余项临床研究。核心产品H药 汉斯状®(斯鲁利单抗,欧洲商品名:Hetronifly®)作为全球首个获批一线治疗小细胞肺癌的抗PD-1单抗,正加速全球布局,已在全球40余个市场获批上市;同时,多款潜力创新资产,包括PD-L1 ADC HLX43及新表位HER2单抗HLX22正全面推进全球关键性临床研究。依托通过中、欧、美三地GMP认证的生产体系,复宏汉霖已建成总产能达84,000升的生物药生产平台,形成覆盖全球六大洲的稳定供应网络。未来,复宏汉霖将始终坚持以患者为中心,聚焦未满足的临床需求,持续推动创新成果向临床价值与患者可及转化,在全球生物医药创新生态中创造长期而稳健的价值。