-
在ADlong 3b期研究中,几乎所有接受lebrikizumab治疗的患者都实现了显著的皮肤改善 (EASI-75) 长达四年
-
75%的患者达到了皮损几乎完全清除的高标准(EASI-90),78%的患者瘙痒症状明显缓解(瘙痒NRS≤4),而瘙痒是患者最为困扰的症状之一
-
80%的患者无需外用糖皮质激素即可取得持久效果
声明:
1. 本文中所述药物及相关适应症尚未在中国大陆获批
2. 礼来不推荐任何未获批的药品和/或未获批适应症的使用
近日,礼来公司公布了新的长期数据,数据显示lebrikizumab在一项提供每月一次维持注射的开放标签扩展研究中,为中重度特应性皮炎(湿疹)患者带来了长达四年的持久皮损清除和持续瘙痒缓解。ADlong 3b 期研究第一年的中期结果已经在3月27日至31日在丹佛举行的美国皮肤病学会(AAD)年会上公布。1
礼来公司执行副总裁兼免疫学事业部总裁Adrienne Brown表示:“这些数据进一步凸显了我们坚定不移地致力于拓展中重度特应性皮炎患者通过治疗所能实现的治疗成效。长期以来,治疗的重点一直集中在症状管理上,尽管反复使用外用药治疗,许多患者仍然难以实现持续稳定的疾病控制。Lebrikizumab正在帮助改变这种治疗模式—让患者有机会重新想象不再被疾病反复发作或每天2-3次外用药治疗所频繁干扰的生活。”
Lebrikizumab是一种白细胞介素13(IL-13)抑制剂,可选择性阻断 IL-13 信号传导, 具有高结合亲和力和缓慢的解离速率。2、3、4细胞因子IL-13是特应性皮炎的关键致病细胞因子,驱动皮肤2型炎症反应循环,导致皮肤屏障功能障碍、瘙痒、皮肤增厚和感染。 5,6
在ADlong研究中,大多数患者在接受长达四年的持续lebrikizumab治疗后,实现了皮损几乎完全清除的高标准和显著的瘙痒缓解。大多数患者 (77%) 接受lebrikizumab单药治疗,80%的患者在未使用外用糖皮质激素的情况下取得了疗效。此外,在研究期间,80%的患者通过每月一次的lebrikizumab维持剂量实现了上述治疗效果。
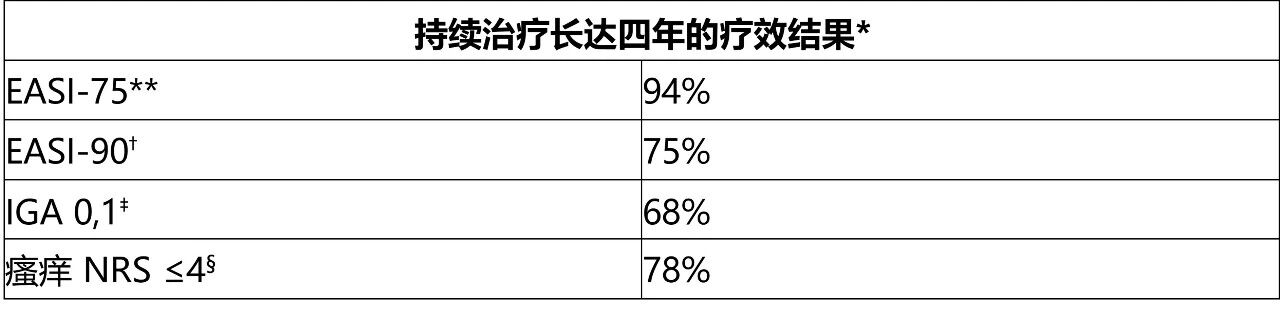
* 数据按观测值报告
** EASI=湿疹面积和严重程度指数; EASI-75=EASI评分较基线降低≥75%
† EASI90= EASI 评分较基线降低≥90%
‡ IGA 0,1=研究者总体评估0或1(“清除”或“几乎清除”)
§ 瘙痒 NRS=数字评定量表将瘙痒程度评定为 0-10,其中10表示过去24小时内最严重的瘙痒
在ADlong研究第一年中,无论给药频率如何,lebrikizumab的安全性均与其在中重度特应性皮炎患者中的既往已知安全性特征一致,且未观察到新的安全性信号。大多数不良事件为轻度或中度,且未导致治疗中断。研究中报告的治疗相关不良事件包括结膜炎(6.9%)和注射部位反应(0.6%)。
ADlong研究仍在进行中,并将再持续一年。这些结果进一步强化了此前已报道的lebrikizumab在中重度特应性皮炎患者中的长期研究结果。此外, 在2026年Maui Derm Hawaii会议上公布的一项针对EASI‑75稳定应答者的事后分析显示,接受lebrikizumab每月一次维持剂量单药治疗时,每位患者每年发作次数少于一次。7
纽约西奈山伊坎医学院皮肤科沃尔德曼教授、卫生系统主任Emma Guttman-Yassky博士表示:“中重度特应性皮炎患者仍然存在尚未满足的治疗需求。这些患者常常经历不可预见的疾病发作,亟需不仅仅停留在症状缓解层面、而是能够针对驱动皮肤症状和持续瘙痒的潜在炎症的治疗选择。为期四年的研究结果进一步强化了lebrikizumab在实现持久疾病控制方面的潜力,可帮助患者在无论是否联合外用治疗的情况下均减少疾病发作。”
礼来公司致力于持续提高皮肤病治疗标准,并积极投资下一代免疫学创新, 包括对新一代治疗模式的重点布局、有针对性地拓展小分子药物,以及推进探索肠促胰岛素潜力的前沿科学研究。礼来公司近期公布了TOGETHER-PsA和TOGETHER-PsO试验的主要结果,这些试验研究了同时使用依奇珠单抗和基于肠促胰岛素的疗法来治疗同时患有银屑病疾病和肥胖或超重(并伴有至少一种体重相关合并症)的成人患者。礼来公司的研究疗法包括DC-853(一种正在研究用于治疗银屑病的新型口服 IL-17 抑制剂)和eltrekibart(一种靶向中性粒细胞驱动炎症、正在化脓性汗腺炎中进行评估的新型单克隆抗体)。
礼来拥有在美国和除欧洲以外的全球其他地区开发和商业化lebrikizumab的独家权力。礼来的合作伙伴Almirall拥有在欧洲开发和商业化lebrikizumab的权利,用于包括特应性皮炎在内的皮肤科适应症。
关于ADlong
ADlong (NCT05916365) 是一项开放标签扩展研究,旨在评估lebrikizumab 250mg每4周一次(Q4W)用于中重度特应性皮炎患者的长期安全性和有效性,总研究周期为108周。来自欧洲部分国家、已完成100周ADjoin延长期研究的成人及青少年患者12–17岁,体重≥40kg)可入组ADlong;其中包括完成ADore试验(52周)、ADhere试验(16周)的患者,以及完成 ADvocate 1 和 2 试验(52周)的第16周应答者。本次分析纳入的患者(N=174)均接受开放标签 lebrikizumab 250mg Q4W 给药,且不受其在ADjoin中既往给药方案(Q2W或 Q4W)的影响。lebrikizumab的获批维持剂量为每月一次250mg;在完成为期4个月的初始给药阶段(每2周一次)后,或在之后达到充分临床应答后,可调整为该维持方案。8 研究允许间歇性使用外用补救药物和短期全身治疗。1 若疗效应答低于EASI-50,可以使用Q2W,然后可以恢复Q4W。
关于lebrikizumab
Lebrikizumab是一种单克隆抗体,能够以高结合亲和力和缓慢解离速率选择性地靶向并中和 IL-13。3、4、8 Lebrikizumab与IL-13细胞因子结合的位置与IL-13Rα1/IL-4Rα异源二聚体中 IL-4Rα 亚基的结合位点重叠,从而阻止该受体复合物的形成并抑制IL-13信号传导。IL-13被认为是与湿疹病理生理密切相关的主要细胞因子,驱动皮肤中的2型炎症循环,而lebrikizumab则选择性地靶向 IL-13。8
Lebrikizumab特应性皮炎3期计划由七项关键的全球研究组成,评估了1,600多名患者,其中包括两项单药治疗研究(ADvocate 1 和 2)、一项与外用皮质类固醇联合治疗的研究(ADhere)、长期扩展研究(ADjoin)、以及青少年开放标签研究(ADore)和儿科研究(ADorable 1 和 2)的组合研究。Lebrikizumab还在过敏性鼻炎和伴有鼻息肉的慢性鼻窦炎中进行研究。
Lebrikizumab已于2024年在美国,日本和加拿大获得批准,并于2023年在欧盟获批。Lebrikizumab作为一种首选单药生物治疗方案,适用于体重至少88磅(40公斤)、12岁及以上的中度至重度特应性皮炎患者,这些患者使用处方外用药物控制效果不佳。8 Lebrikizumab 250毫克/2毫升注射剂在初始治疗阶段后按每月一次的维持剂量注射。推荐的初始剂量为500毫克(两次250毫克注射),分别在第0周和第2周注射,然后每两周注射250毫克,直到第16周或之后达到充分的临床应答;之后的维持剂量为每四周注射一次250毫克。8
关于礼来公司
礼来公司是一家致力于通过科学创新改善人类健康水平,惠及全球患者的医药公司。作为医疗健康行业的领军者,礼来公司拥有近150年的历史。今天,我们的药物已帮助全球数千万人。运用生物技术、化学和基因医学的力量,我们的科学家正在积极推动新的医学进展,以应对严峻的全球健康挑战。重新定义糖尿病与肥胖疗法,减少肥胖对人体的长期影响;助力阿尔茨海默病的防治行动;为一系列威胁人类健康的免疫性疾病提供解决方案;以及将难以治愈的癌症转变为可控的疾病。礼来公司迈向健康世界的每一步,都源自于我们“致力于让数百万患者生活得更美好”的信念。这包括致力于解决全球多重挑战的创新临床试验,同时确保药物的可及性和可负担性。
参考文献
Please scroll down for more.
1 Weidinger S, et al. Efficacy and Safety of Lebrikizumab is Maintained up to 4 Years in Patients With Moderate-to-Severe Atopic Dermatitis: first year of ADlong Long-Term Extension Trial. American Academy of Dermatology Annual Meeting. March 2026
2 Simpson EL, et al. Efficacy and safety of lebrikizumab (an anti-IL-13 monoclonal antibody) in adults with moderate-to-severe atopic dermatitis inadequately controlled by topical corticosteroids: A randomized, placebo-controlled phase II trial (TREBLE). J Am Acad Dermatol. 2018;78(5):863-871.e11. doi:10.1016/j.jaad.2018.01.017
3 Okragly A, et al. Binding, Neutralization and Internalization of the Interleukin-13 Antibody, Lebrikizumab. Dermatol Ther (Heidelb). 2023;13(7):1535-1547. doi:10.1007/s13555-023-00947-7
4 Ultsch M, et al. Structural basis of signaling blockade by anti-IL-13 antibody Lebrikizumab. J Mol Biol. 2013;425(8):1330-1339. doi:10.10116/j.jmb.2013.01.024
5 Bieber T. Interleukin-13: Targeting an underestimated cytokine in atopic dermatitis. Allergy. 2020;75(1):54–62. doi:10.1111/all.13954
6 Tsoi LC, et al. Atopic Dermatitis Is an IL-13-Dominant Disease with Greater Molecular Heterogeneity Compared to Psoriasis. J Invest Dermatol. 2019;139(7):1480-1489. doi:10.1016/j.jid.2018.12.018
7 Merola J, et al. Patients with Atopic Dermatitis with a Stable Response to Lebrikizumab Flare Less in a Long-Term Study: A Post-hoc Analysis of the ADjoin Study. Maui Derm
Hawaii. January 2026
8 EBGLYSS. Prescribing Information. Lilly USA, LLC.