• TfR1-AOC在肝脏的siRNA暴露量是肌肉的50到数百倍,虽然功能性敲低只发生在肌肉和心脏,但庞大的骨骼肌质量和广泛受体分布,剂量效率劣势可能导致其被αvβ6等更高效路线超越;
• 脂质工程、化学修饰、靶向配体设计和抗体优化等工程化技术对递送效率的影响非常大,工程化水平也是技术平台级企业的关键竞争力;
• 必须以NHP数据为金标准,同一分子在小鼠和食蟹猴中的递送效率差异可能会非常大;
• 对于递送靶点的选择,即使其表达不是非常高,仍能通过循环暴露、接触概率和内吞效率进行一定的补偿;
• 受体表达谱、病理机制和可接受的部分敲低安全窗口等关键因素,共同定义了每个平台的“黄金适应症”;
• 当递送效率达到治疗阈值后,给药方式成为关键变量,皮下注射通常更具产品化优势;
• 肝外递送的核心不是单纯提高组织暴露量,而是同时解决组织到达、细胞摄取和胞质释放三个层面的效率瓶颈。
撰文|濠麦科技技术挖掘与研判部
RNA干扰(RNAi)技术自诞生以来,已在临床转化中取得了令人瞩目的成就。以Alnylam为代表的biotech公司成功将siRNA药物推向市场,Patisiran采用LNP/lipid complex;Givosiran、Lumasiran、Inclisiran等采用GalNAc(N-乙酰半乳糖胺)肝靶向递送。GalNAc通过与肝细胞表面高表达的去唾液酸糖蛋白受体(ASGPR)高效结合,实现了siRNA的肝实质细胞靶向递送,其递送效率之高、组织选择性之强,堪称RNAi药物递送的标杆范式。
但生命科学的需求从未止步于肝脏。心脏、骨骼肌、肾脏、肺、中枢神经系统、脂肪组织、皮肤等肝外器官和组织,同样承载着大量未被满足的临床需求。与肝脏递送相比,肝外递送面临的核心挑战在于:第一,肝外组织缺乏类似ASGPR那样高表达、高效内吞、快速循环的受体系统;第二,许多靶器官具有独特的组织结构和生理屏障,药物渗透难度极大;第三,非靶组织的广泛暴露可能带来安全性隐患,尤其是造血系统、内分泌系统和神经系统对脱靶效应极为敏感;第四,各物种间受体表达谱和组织结构的差异导致临床前数据向人体转化的种属差异巨大,为剂量设计和疗效预测带来极大不确定性。
尽管如此,近年来肝外递送领域捷报频传。罗氏的Brainshuttle技术在阿尔茨海默病药物trontinemab中完成临床验证,并与Manifold Bio以20亿美元级的交易合作开发下一代BBB shuttle ;Avidity的del-desiran(formerly AOC 1001)在DM1中实现42%肌肉靶点敲低并获BTD认定,已进入III期临床试验;心脏递送以Atrium(Avidity被收购后独立拆分)为代表,其基于TfR1抗体偶联的siRNA系统已在非人灵长类动物中实现心肌组织特异性基因沉默,验证了AOC平台向心脏适应症扩展的可行性;Judo Bio的STRIKE™平台基于Megalin受体实现肾脏近端小管递送,即将提交IND申报;Alnylam将递送版图扩展至脂肪组织(ALN-2232/4324进入临床),Arrowhead-ARO-RAGE公司通过αvβ6小分子配体,成功将siRNA送进肺上皮细胞,该药物也已进入临床阶段。这些突破标志着siRNA肝外递送正从概念验证走向产业化开发的关键拐点。
本文将分上下两篇,系统梳理当前心、肾、肺、脑、肌肉、脂肪、皮肤七大肝外器官/组织的siRNA递送技术进展,深度解析代表性平台的设计原理、临床前数据、核心瓶颈与发展前景,为关注RNA疗法前沿的研究者和从业者提供一份全面而深入的参考资料。
为方便面对面交流,5月22日,濠麦科技将联合研发客在横琴举办第十六次主题为 “破局肝外小核酸递送:平台技术拆解、产业化挑战与机遇” 的闭门头脑风暴会议。将围绕研发前沿、技术壁垒、研发策略、以及投资与交易机会等核心议题展开深入探讨。名额有限,报名请咨询濠麦同事:
蔡鸿 技术挖掘与研判部负责人
电话:18578675942
邮箱:alex@hq-haomai.com
一、骨骼肌靶向递送
骨骼肌约占人体体重的40%,是人体最大的组织器官。从临床需求的角度来审视,肌肉疾病数量庞大且治疗手段匮乏。例如,杜氏肌营养不良症(DMD)、面肩肱型肌营养不良症1型(FSHD1)、强直性肌营养不良1型(DM1)、肢带型肌营养不良(LGMD)等多种遗传性肌病长期面临“无药可治”的困境。从生物学机制角度,许多肌肉疾病由单基因突变驱动,靶点极为明确,RNAi干预具有清晰的药理逻辑。从组织学特征角度来看,骨骼肌分布广泛,如果局部注射,药物无法覆盖全身,必须依赖系统性递送技术。这些特征使得骨骼肌成为肝外siRNA递送最具商业价值和科学意义的优先赛道。
当前肌肉递送领域的代表性技术路线包括:TfR1(转铁蛋白受体1)抗体偶联路线(以Avidity为代表)、αvβ6整合素配体偶联路线(以Arrowhead和Alnylam为代表)。
1.1 Avidity AOC平台:TfR1抗体的开创性探索
Avidity Biosciences是AOC(抗体-寡核苷酸偶联物)概念的先驱。其核心设计是将siRNA通过化学链接子与靶向TfR1的全长单克隆抗体偶联,利用TfR1在骨骼肌细胞表面的高表达实现靶向递送。TfR1是经典的内吞型受体,在介导铁-转铁蛋白复合物内吞的同时持续循环于细胞膜与内涵体之间,理论上非常适合作为药物递送的“入口”。
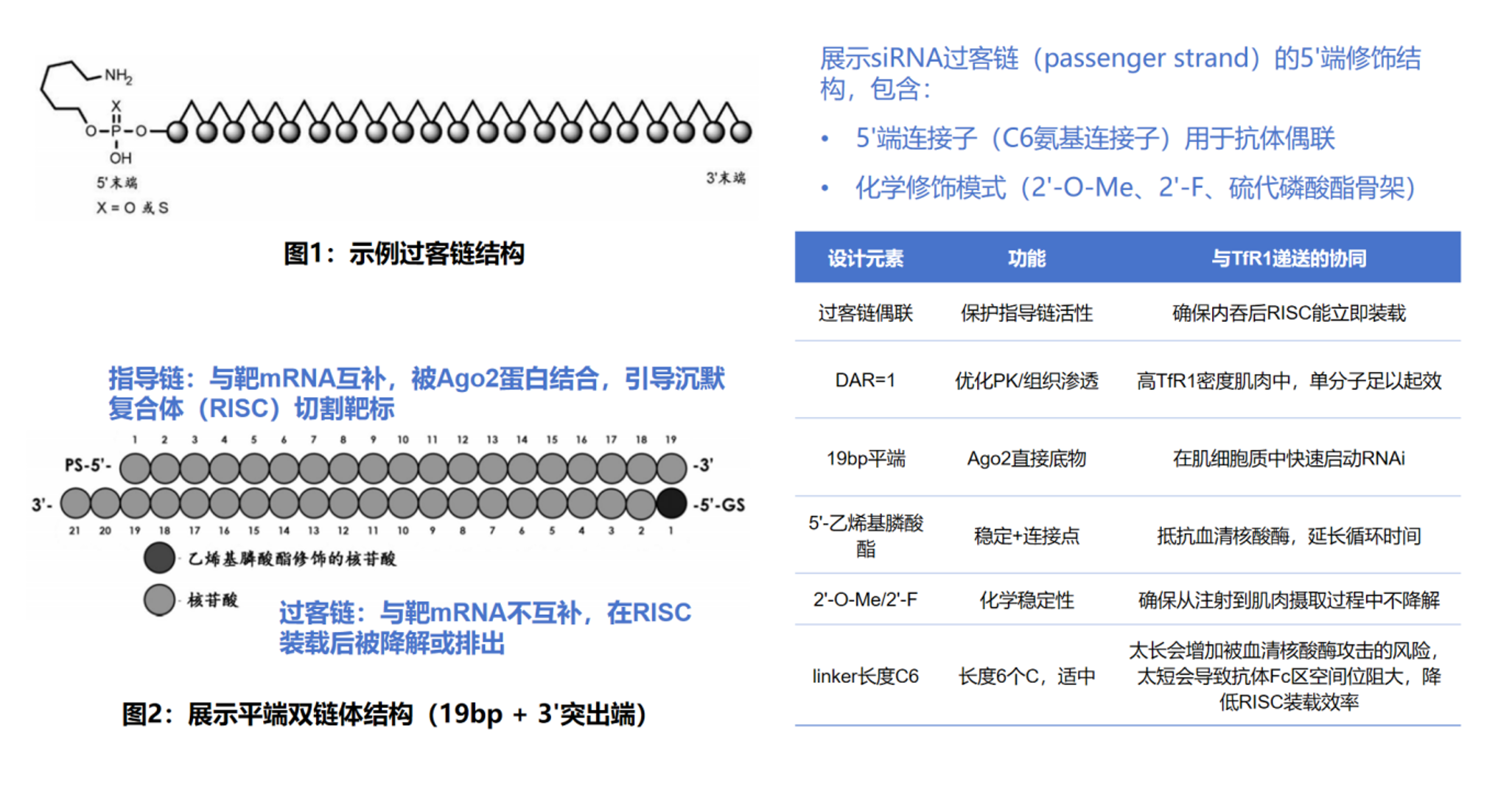
从分子设计层面来看,Avidity在专利WO2020132584A1(于2019年申请)中详细描述了其siRNA的化学修饰策略和偶联方案。siRNA采用19bp平端双链体结构,可作为Ago2蛋白的直接底物,在肌细胞质中快速启动RNAi。过客链的5’端通过C6氨基连接子与抗体偶联(这一链接子长度经过精心优化:过长会增加被血清核酸酶攻击的风险,过短则会导致抗体Fc区产生空间位阻、降低RISC装载效率)。siRNA的化学修饰模式包括2’-O-Me、2’-F以及硫代磷酸酯骨架修饰,其中5’-乙烯基膦酸酯修饰在赋予核酸酶抗性的同时提供了稳定的连接位点。药物抗体比(DAR)值设定为1,这一设计在优化药代动力学和组织渗透之间取得了平衡,在TfR1高密度的肌肉组织中,单个siRNA分子足以触发有效的基因沉默。
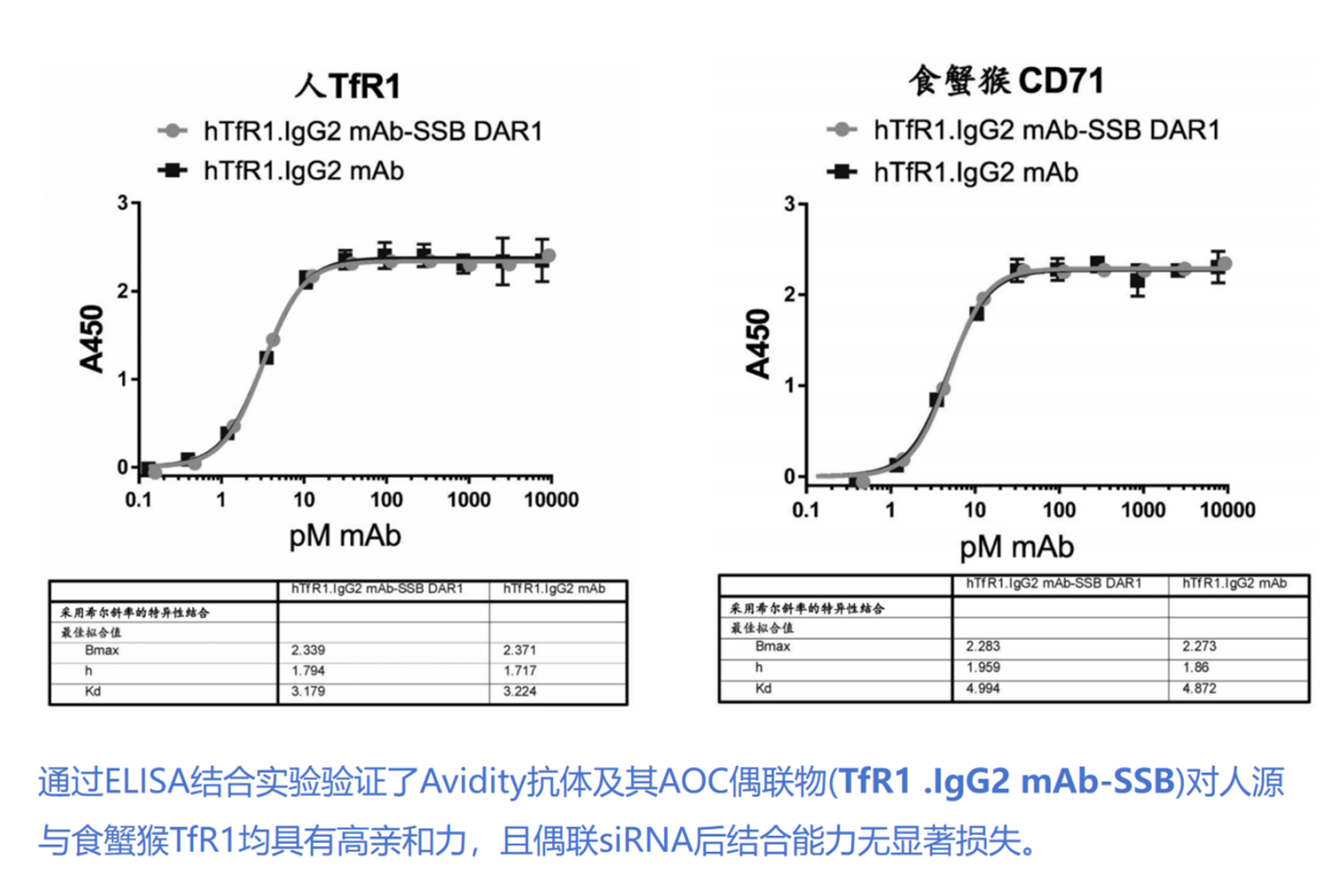
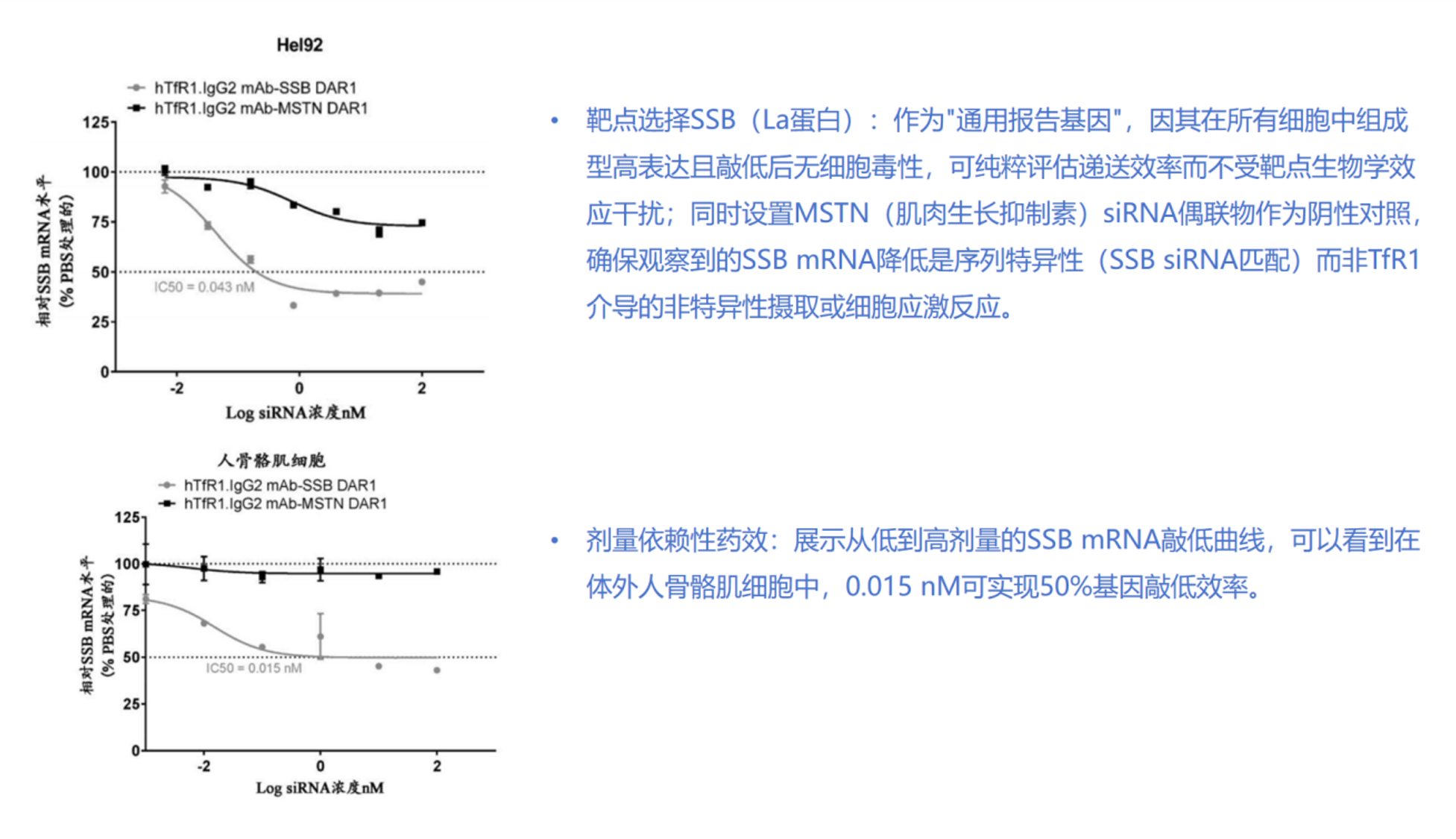
体外验证数据显示,Avidity AOC在细胞层面展现出高效的递送活性。研究人员选择SSB(La蛋白)作为“通用报告基因”,因该蛋白在所有细胞中组成型高表达且敲低后无细胞毒性,可纯粹评估递送效率而不受靶点生物学效应干扰。同时设置MSTN(肌肉生长抑制素)siRNA偶联物作为阴性对照,确保观察到的SSB mRNA降低是序列特异性的TfR1介导摄取而非非特异性细胞应激反应。在人骨骼肌细胞中,AOC展现出剂量依赖性的基因沉默效果,最低在0.015 nM浓度即可实现50%的基因敲低。
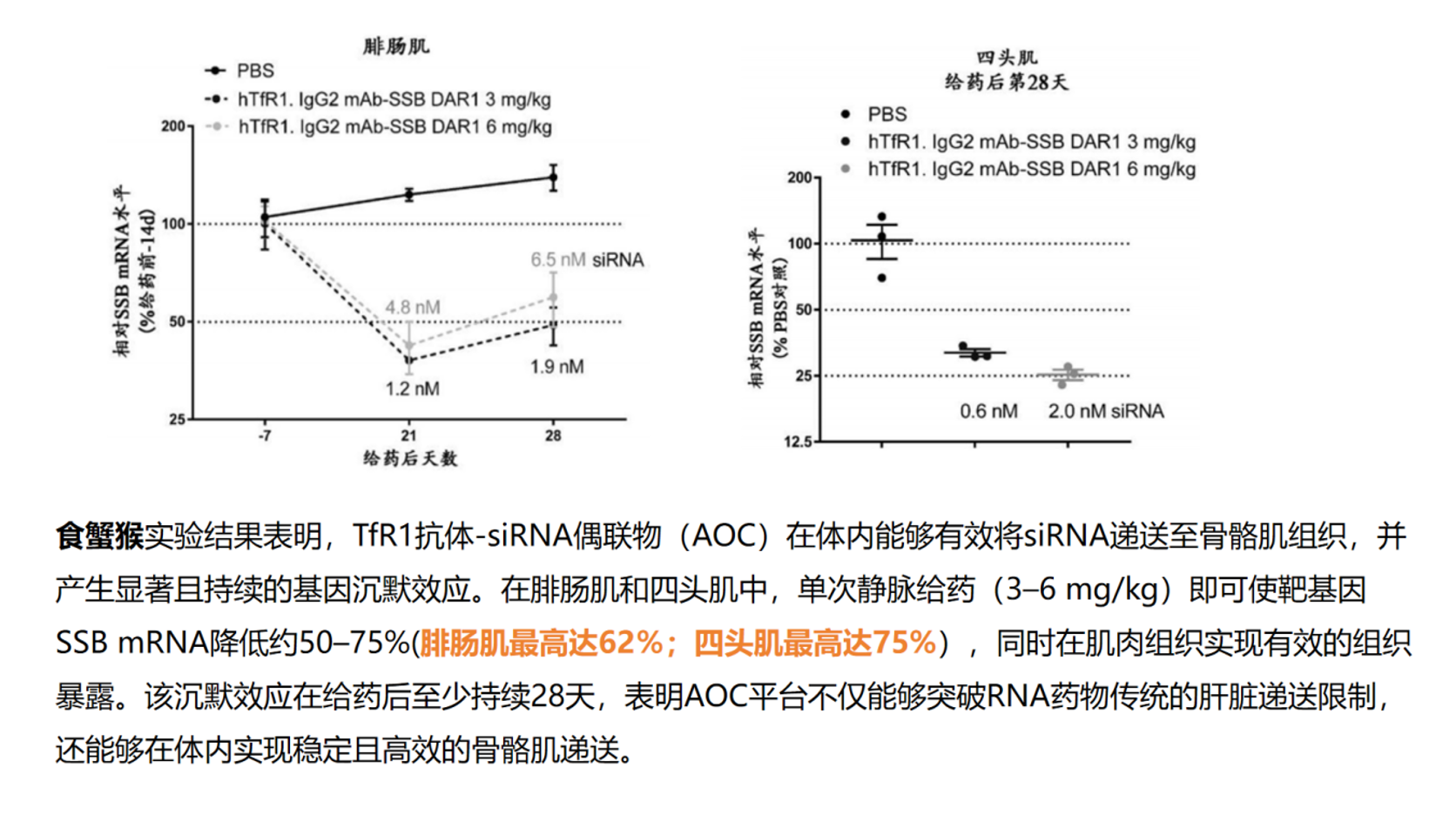
食蟹猴体内的研究数据进一步验证了平台的临床转化潜力。单次静脉给药3~6 mg/kg后,腓肠肌和股四头肌中SSB mRNA分别降低约50%~62%和50%~75%,且药效在给药后至少持续28天。
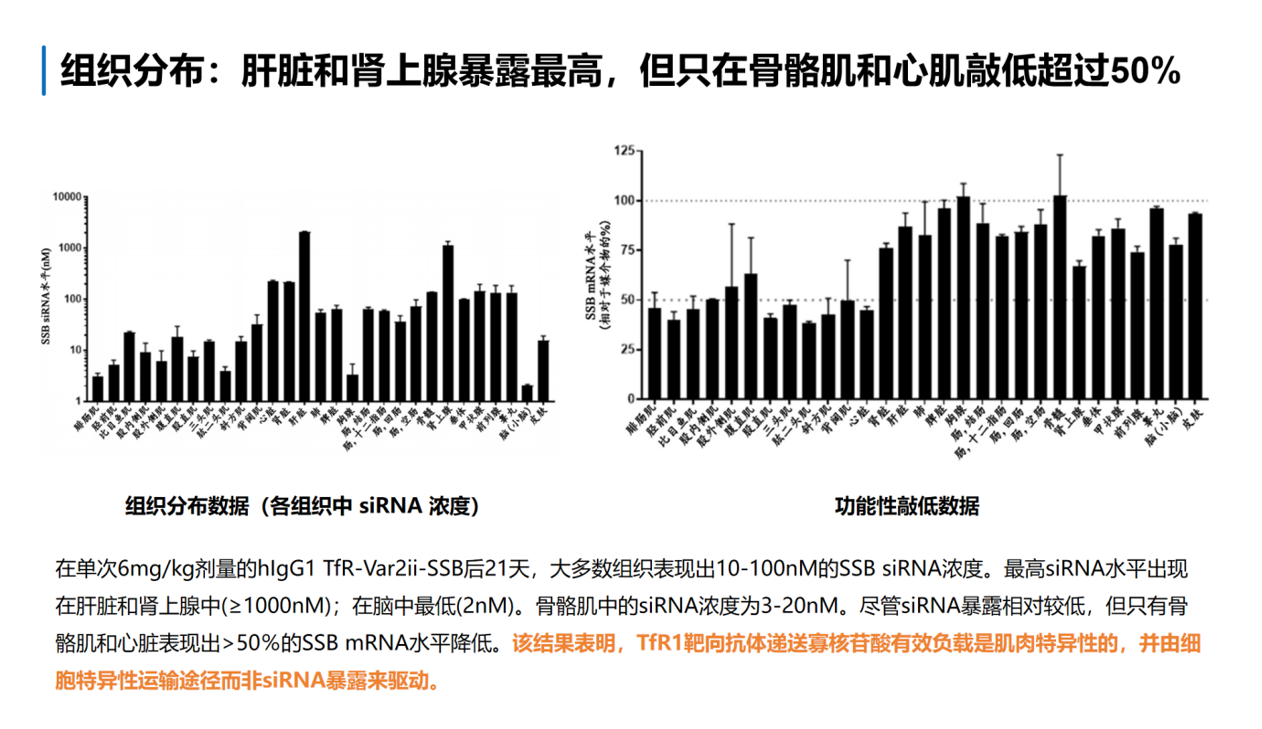
组织分布数据显示,尽管siRNA在肝脏和肾上腺中的暴露量最高(≥1000 nM),远高于骨骼肌(3~20 nM),但功能性敲低仅发生于骨骼肌和心肌(>50% mRNA降低),其他组织未见沉默。这一发现表明,TfR1靶向抗体递送siRNA的肌肉选择性并非由siRNA暴露量驱动,而是由细胞特异性的TfR1介导运输途径决定。
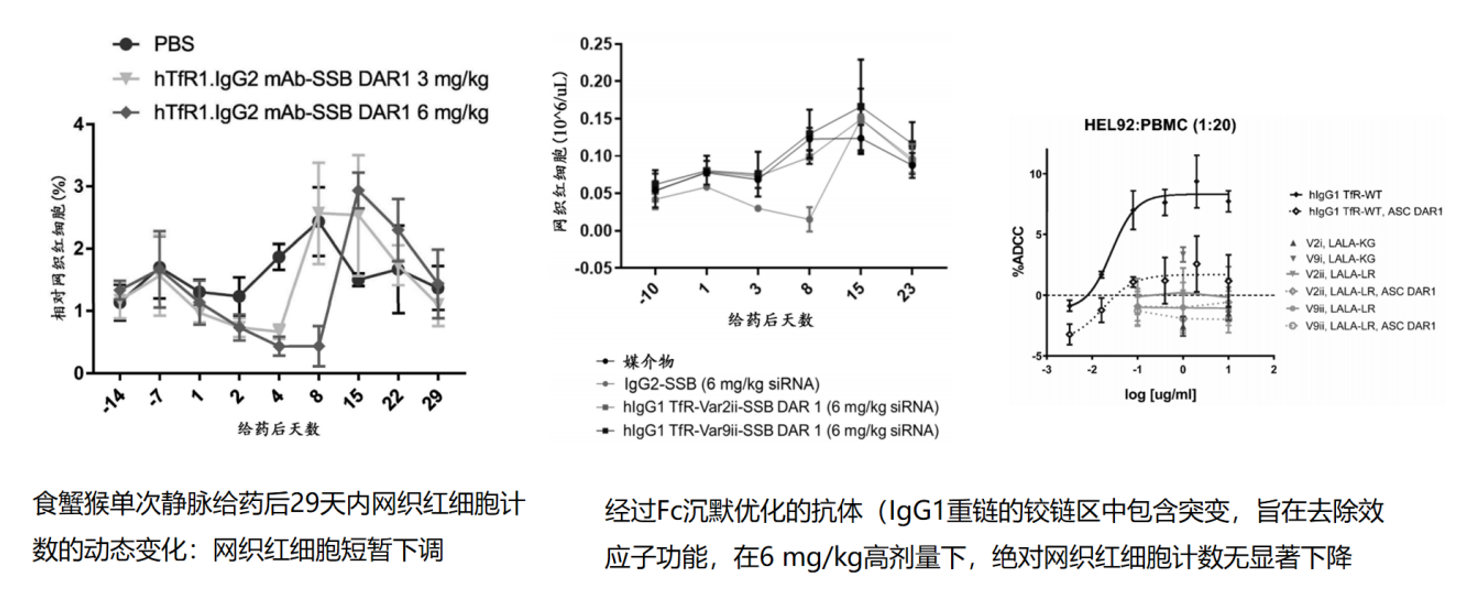
安全性方面,TfR1路线最受关注的是网织红细胞毒性。TfR1介导铁摄取,是血红素合成的限速步骤。TfR1-AOC暂时占据受体可阻碍铁摄取,导致红系前体细胞成熟受阻。Avidity通过Fc沉默优化(在IgG1重链铰链区引入突变去除效应子功能)显著缓解了这一毒性,在6 mg/kg高剂量下,绝对网织红细胞计数无显著下降。值得注意的是,在灵长类动物中,高表达TfR1的网织红细胞比例远低于啮齿类,因此网织红细胞消耗更为短暂,这一点对临床转化是利好。
然而,TfR1的路线也面临两个结构性风险。其一,TfR1广泛表达于人体多种组织和细胞类型,带来潜在脱靶风险;其二,庞大的骨骼肌质量和广泛受体分布导致剂量-药效平衡困难,Avidity的AOC 1001在临床中需要多次给药才能达到理想肌肉浓度。这些局限性促使产业界持续探索更具选择性的替代方案。
1.2 Arrowhead αvβ6路线:多肽偶联的系统优化
Arrowhead选择了另一条截然不同的技术路径,他们利用αvβ6整合素作为肌肉递送的入口。αvβ6是一种异二聚体整合素,在健康组织中低表达,但在损伤修复、纤维化、慢性炎症、肿瘤和特定条件下的肌肉和脂肪中会表达上调。与TfR1相比,αvβ6整合素约40%始终位于细胞表面(TfR1仅约5%),且其介导的内吞效率较高,理论上可带来更高的肌肉递送效率和更安全的剂量窗口。
Arrowhead在专利WO2022056277A1(于2021年申请)中系统披露了其技术平台和优化历程。其分子设计包含3个核心模块:αvβ6靶向肽(Pep1为主力配体)、siRNA载荷(靶向MSTN、SOD1等报告基因)及脂质PK/PD调节剂。这一设计的独特之处在于引入了“PK/PD调节剂”的概念,通过特定脂质结构(如LP38b、LP33b、LP29b等)与靶向肽-siRNA偶联物组合,系统优化分子的脂水分配系数、血浆半衰期和组织渗透能力。
专利中实施了从实施例7到实施例24共18组体内实验,堪称肝外递送领域最详尽的构效关系研究之一。这些数据揭示了几个关键规律:
第一,靶向配体的选择非常重要。在比较Pep1、Pep5、Pep6等多种αvβ6靶向肽的实验中,Pep1(αvβ6肽1)持续性的展现出最优的肌肉递送效率,在小鼠三头肌中实现75%-85%的MSTN抑制率,腓肠肌达65%-80%。
第二,脂质PK/PD调节剂的结构影响递送效率。Arrowhead测试了数十种脂质结构(LP1、LP29b、LP33b、LP38b、LP41b、LP53b等),发现含特定脂质链和PEG长度的结构可实现>85%的基因抑制率。这些优化结构具有平衡的亲水性和疏水性,能有效穿透肌肉组织细胞膜,同时保持良好的体内稳定性。
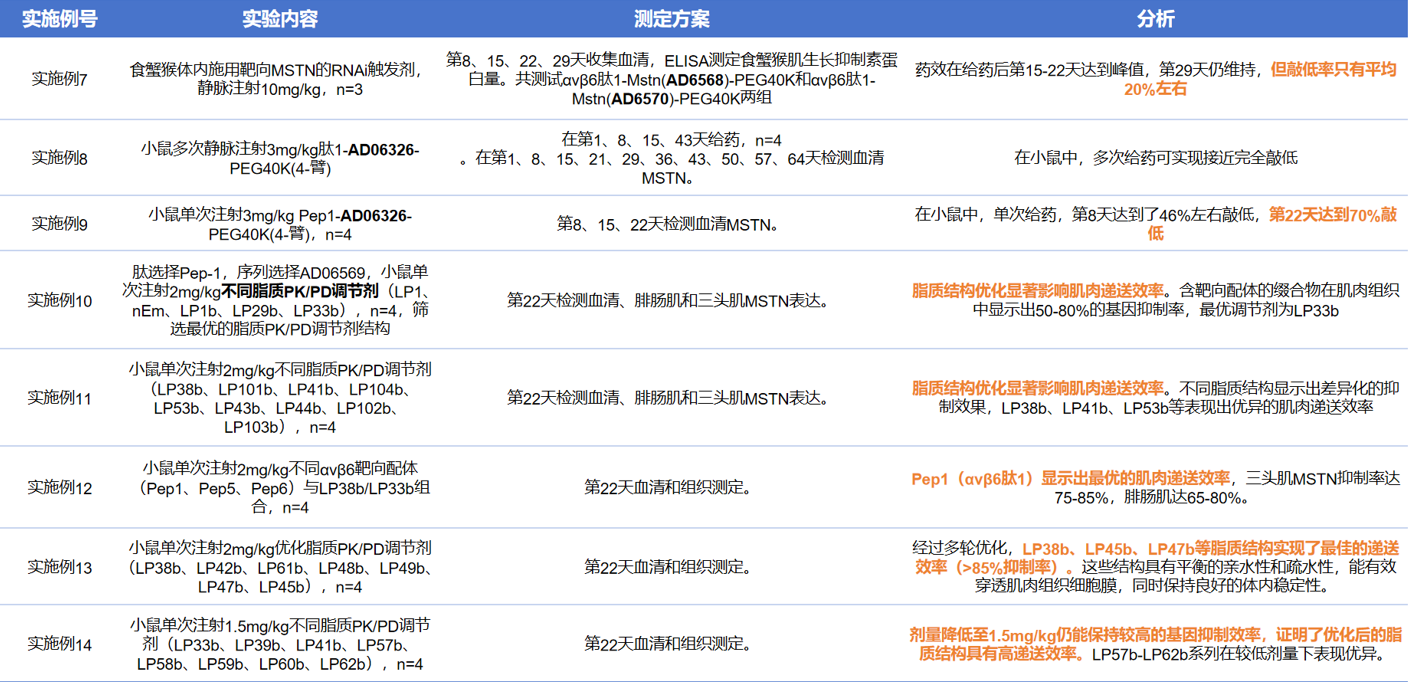
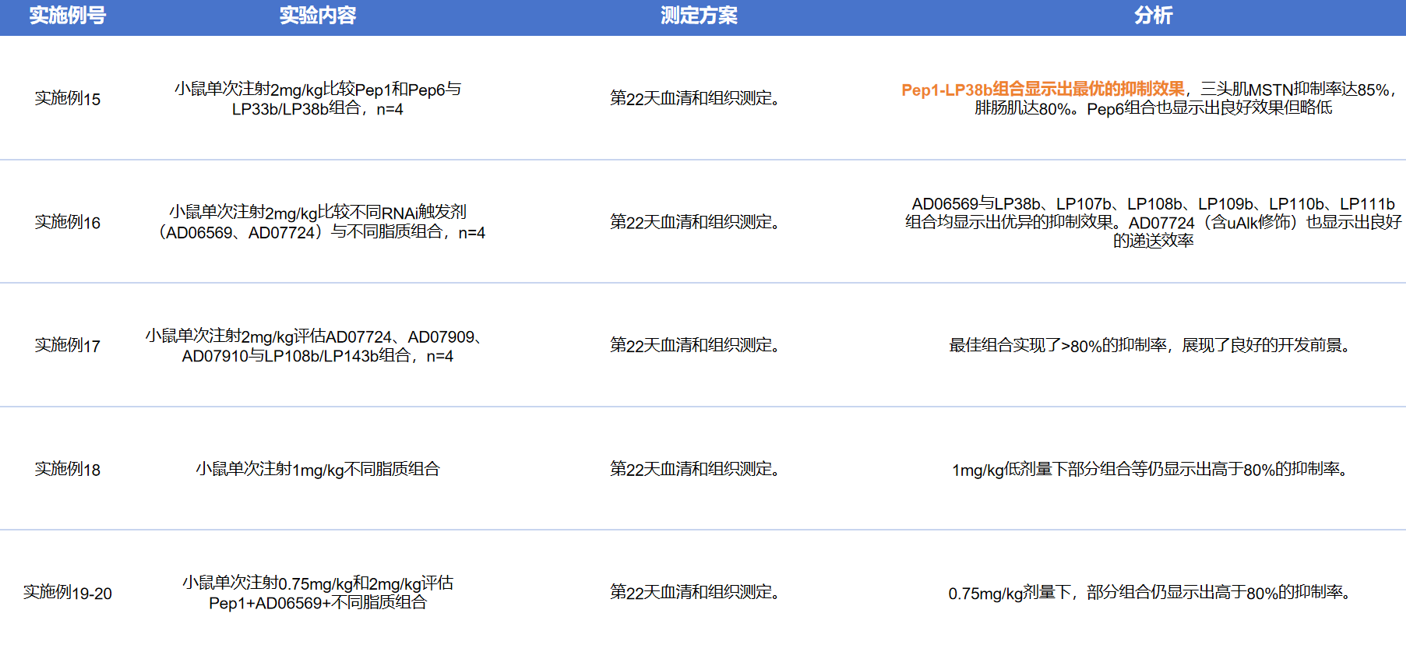

实施例22~23是Arrowhead的食蟹猴实验,多次注射10 mg/kg可实现稳健持续的靶基因敲低,单次给药5 mg组最高敲低约30%,10 mg组约50%,20 mg组在第36天达到峰值接近80%并能维持至120天。
Arrowhead的αvβ6路线最终通过与Sarepta的合作走向临床。2026年3月25日披露的Ⅰ/Ⅱ期早期试验数据显示,SRP-1001(靶向FSHD1)在低剂量4.08 mg/kg给药42天后肌肉浓度达28.4 nM,SRP-1003(靶向DM1)在低剂量1.02 mg/kg单次给药后肌肉浓度达12.2 nM,且DM1适应症的安慰剂矫正敲低效率达50%。这些数据不仅验证了αvβ6路线的临床可行性,更值得关注的是其肌肉暴露量高于TfR1-AOC平台,SRP-1001的28.4 nM vs. AOC的4.5 nM,SRP-1003的12.2 nM vs. Dyne TfR1 Fab-ASO的1.86 nM和Avidity AOC的1.43 nM。更高的肌肉暴露预示着潜在的更强药效和更宽的治疗窗口。
1.3 Alnylam αvβ6双修饰路线:从骨骼肌到心肌的跨界突破
Alnylam作为RNAi领域的领军企业,在肝外递送领域采取了更为精细化的分子工程策略。其αvβ6路线采用小分子配体+脂质双修饰的设计,在Arrowhead多肽路线基础上进一步升级,通过偶联特定亲脂基团(长碳链,C22最优)增强体内递送效率。
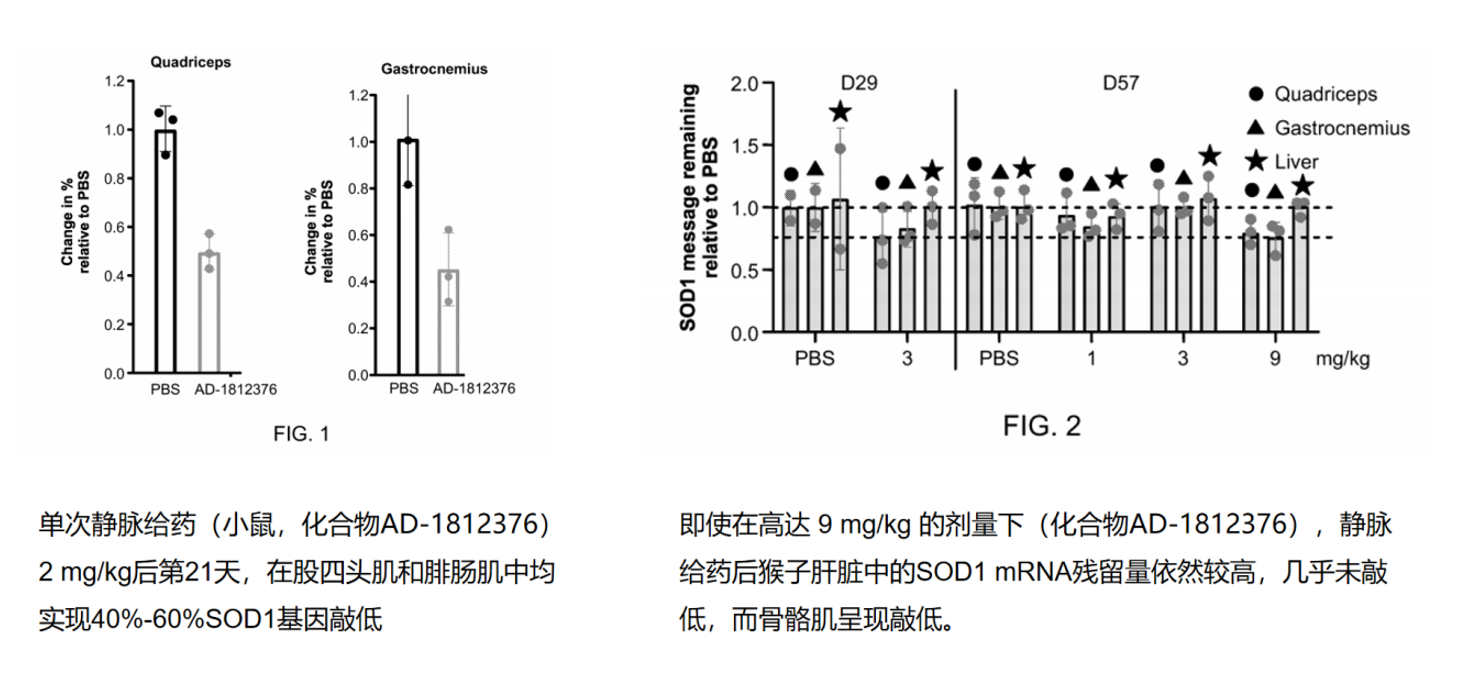
在专利WO2025259743A1(于2025年申请)中,Alnylam展示了令人印象深刻的临床前数据。在小鼠模型中,单次静脉给药2 mg/kg(化合物AD-1812376)后第21天,股四头肌和腓肠肌中SOD1基因敲低达40~60%;
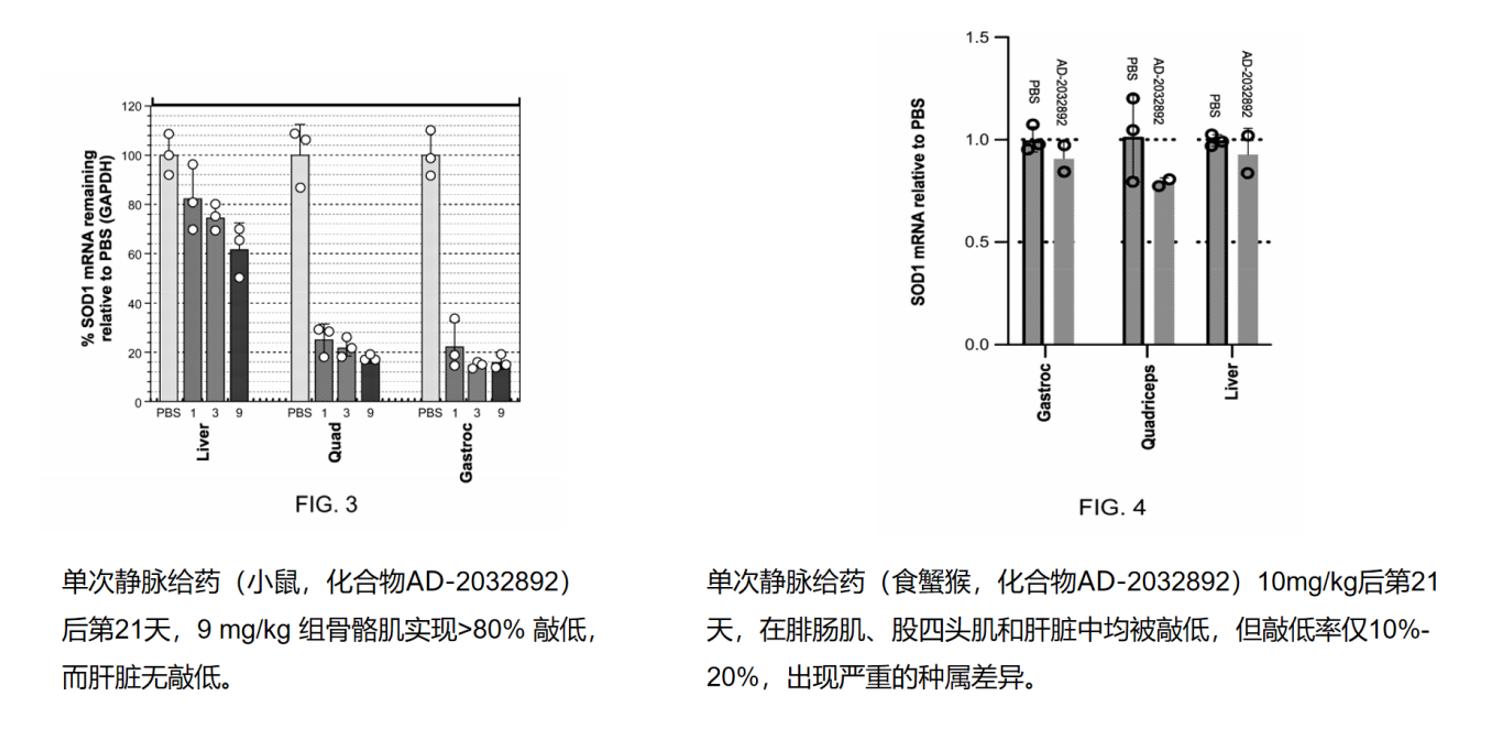
化合物AD-2032892在9 mg/kg剂量下骨骼肌敲低超过80%,且肝脏几乎无敲低。然而,与小鼠数据形成鲜明对比的是,同一化合物在食蟹猴10 mg/kg单次给药后第21天,腓肠肌、股四头肌和肝脏中敲低率仅为10-20%,暴露出严重的种属差异问题。这一数据再次印证了肝外递送必须以NHP数据为金标准的行业共识。
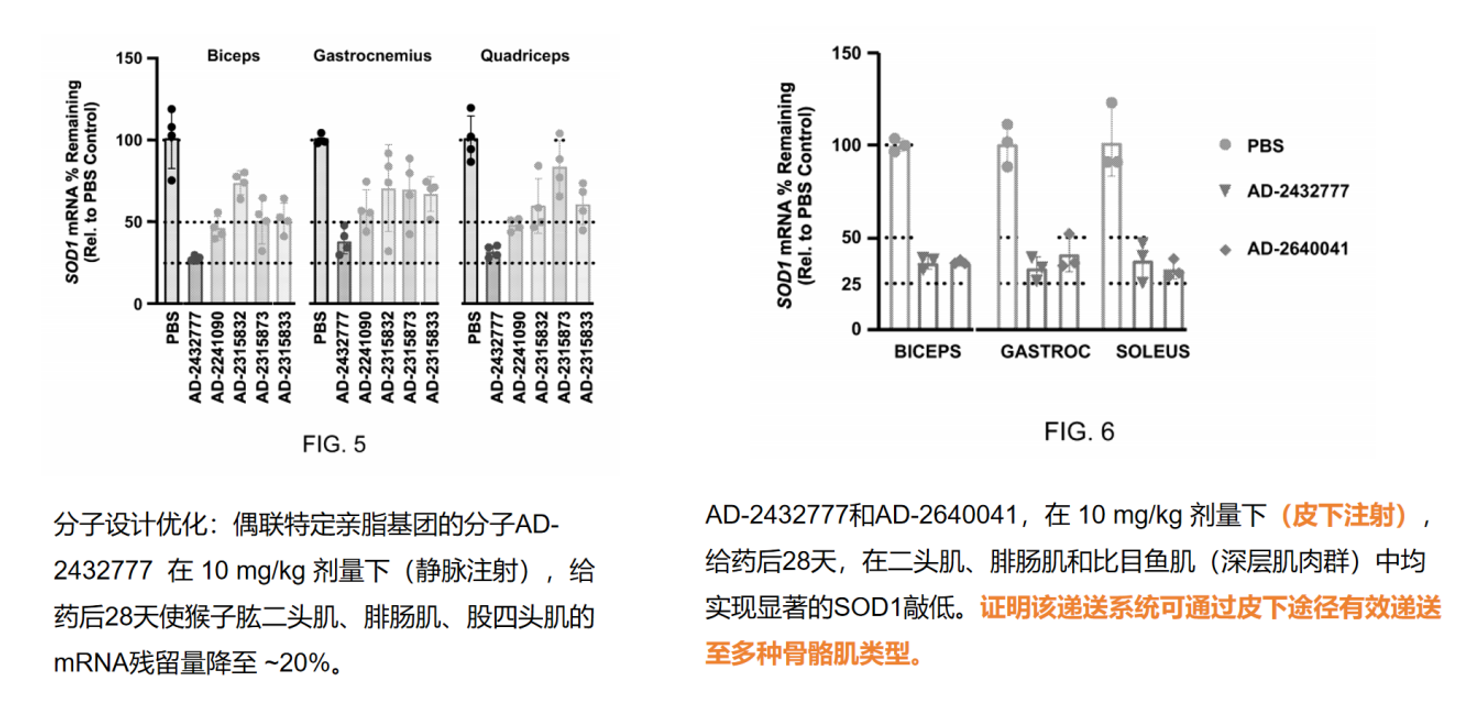
Alnylam的突破性进展体现在两个维度。第一,实现了皮下给药途径。化合物AD-2432777和AD-2640041在10 mg/kg皮下注射后28天,在小鼠二头肌、腓肠肌和比目鱼肌(深层肌肉群)中均实现显著SOD1敲低。皮下给药的可及性对慢病长期管理意义重大。
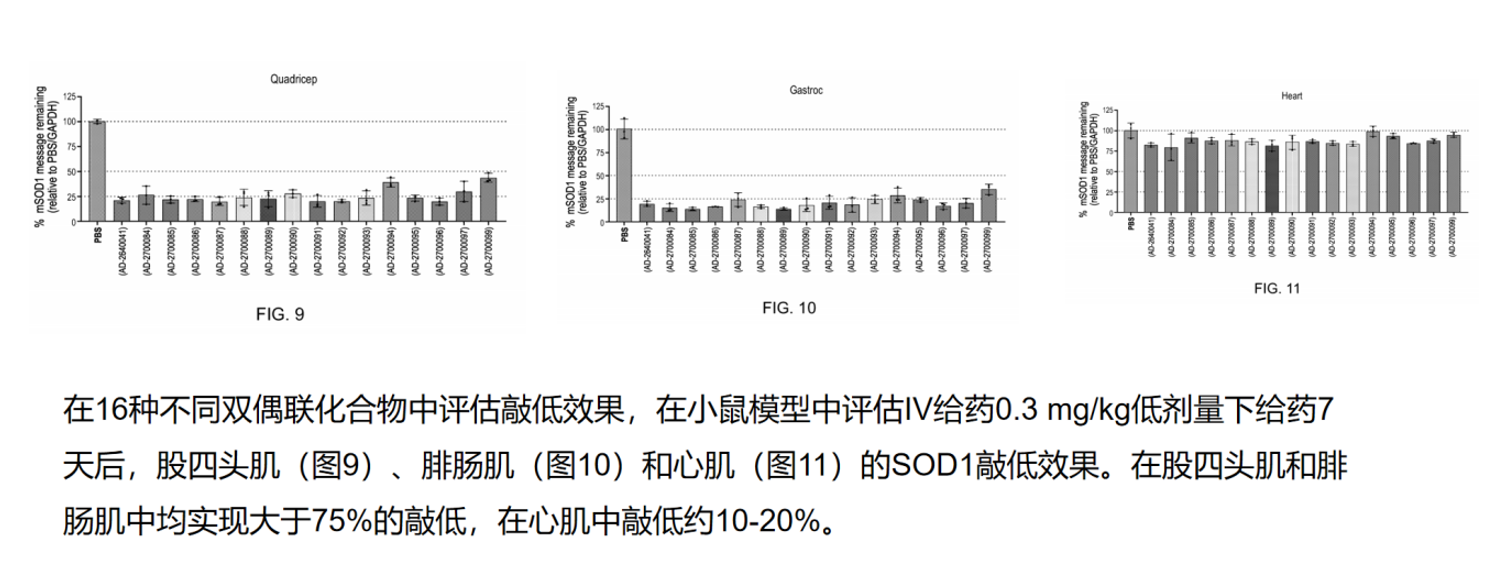
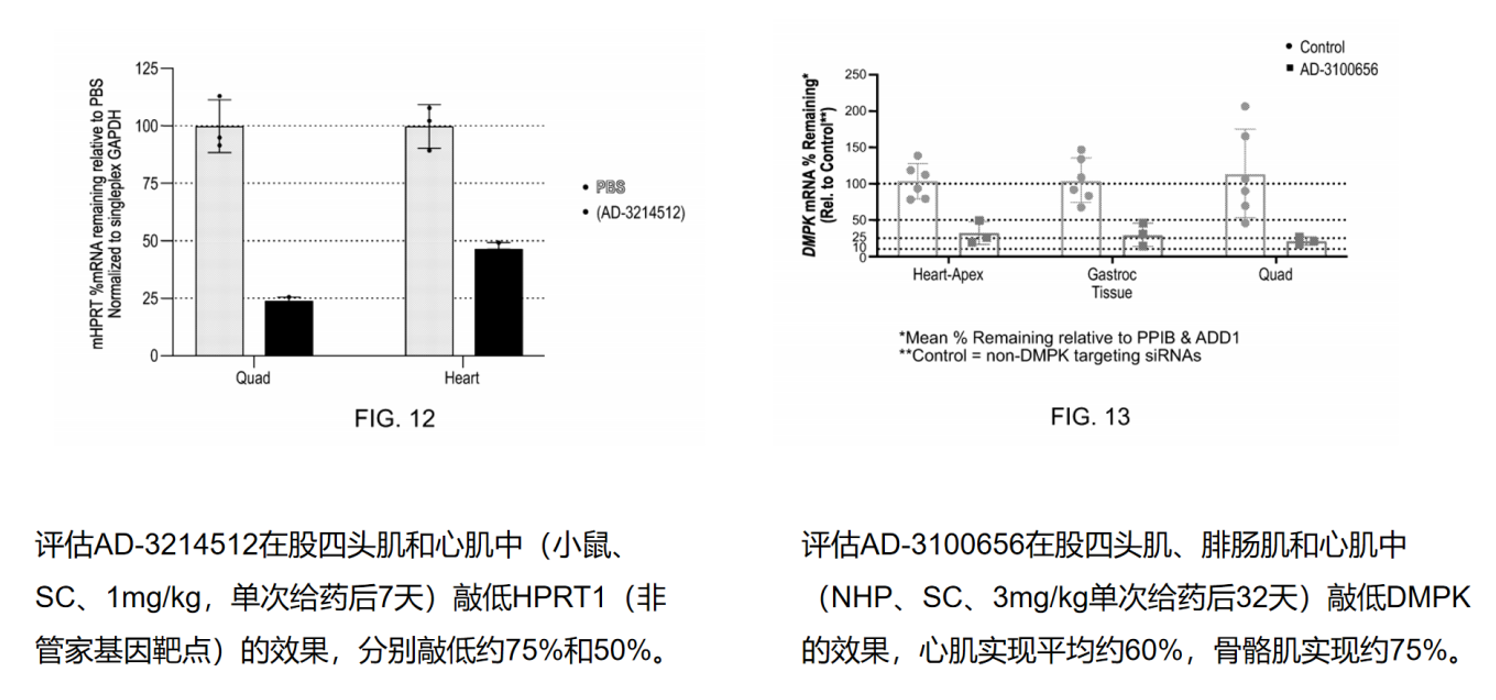
第二,证明了心肌递送能力。在NHP模型中,化合物AD-3100656单次皮下给药3 mg/kg后第32天,心肌实现平均约60%的DMPK敲低,骨骼肌约75%。这意味着αvβ6路线不仅是“肌肉递送平台”,更可能成为“泛肌肉递送平台”,覆盖骨骼肌和心肌两大关键组织。
1.4 肌肉递送技术路线对比与关键启示
-
TfR1作为进展最快的肌肉靶向技术路线,存在两个较大的风险点:1.TfR1生理功能带来的贫血风险(Avidity及罗氏的Brainshuttle来看,这一点可以通过工程化优化解决);2.TfR1广泛表达于人体各种组织和细胞类型,这会带来潜在的脱靶风险,同时也会导致剂量-药效难以平衡。
-
从Avidity专利中可以看出,TfR1靶向抗体递送siRNA在肌肉中低暴露(远低于肝脏和肾上腺)。
-
在灵长类动物中,表达高TfR1水平的网织红细胞的比例低,因此网织红细胞的消耗较短暂,不如啮齿类明显。
-
一些疾病状态下(如DMD),αvβ6约40%始终位于细胞表面(TfR1仅5%),且肌肉中高表达,从理论上带来了两个潜在优势:更高的肌肉递送效率和更安全的剂量窗口。
-
递送效率对靶向配体的亲和力、PK/PD调节剂的脂水分配系数非常敏感,Arrowhead在专利中做了大量组合(靶向肽-linker-siRNA序列-脂质PK/PD调节剂)并测试最优组合。
-
肌肉递送种属差异很大(参见Alnylam Fig3和Fig4,在小鼠中敲低80%,转化到NHP中只有20%)。NHP数据应作为转化判断的关键权重。Arrowhead与Alnylam都采用αvβ6路线,但Arrowhead采用靶向肽+脂质PK/PD调节剂(于2021年申请专利),Alnylam采用小分子配体+体内递送增强基团(长碳链、C22最优,于2025年申请专利)。
从结果来看,Alnylam的临床前结果非常惊艳,不仅实现了皮下给药,同时证明了心肌递送效果(同等剂量下,略低于骨骼肌)以及更低的给药剂量(NHP中3mg/kg即可实现75%-80%敲低,Arrowhead是13.3mg/kg,Avidity需要多次给药)
二、心脏靶向递送
2.1 心脏递送的技术路线全景
心脏是全身血液循环的动力中枢,也是众多重大疾病的原发灶。例如,肥厚型心肌病(HCM)、扩张型心肌病(DCM)、心脏淀粉样变性(ATTR-CM)、心力衰竭等疾病严重影响患者生存质量和预期寿命。与骨骼肌相比,心脏递送面临更为复杂的挑战:心肌组织血供极其丰富(冠状动脉循环),但心肌细胞属于终末分化细胞,内吞活性相对较低;同时,心脏持续处于收缩-舒张的动态力学环境中,药物在组织内的滞留和渗透受到显著影响。

围绕心脏siRNA递送这一前沿方向,我们基于心脏及核酸递送相关关键词及其变体进行了系统性的全球专利扫描,初步获得超过3万项专利家族。通过自主构建的数据标注与降噪模型筛选,最终识别出700余项真正与心脏递送高度相关的核心专利。在此基础上进一步开展landscape分析,可以清晰地将当前技术演进路径划分为六大主流路线,基本勾勒出该领域的整体竞争格局与技术演化方向。
具体而言,六大路线包括:
1.病毒载体路线;
2. 脂质纳米颗粒(LNP)路线;
3. 小分子/配体偶联路线;
4. AOC(抗体偶联)路线;
5. 外泌体路线;
6. 其他路线。
在六大技术路线中,小分子配体偶联路线与抗体-寡核苷酸偶联物(AOC)路线被认为是当前最具转化潜力的两条核心路径。本质上,这两类技术均属于“主动靶向递送”范式,其优势在于能通过受体介导机制实现更高效、更可控的组织或细胞特异性摄取,从而在理论上具备更优的剂量效率与安全性窗口。
2.2 Arrowhead GLP-1R路线:更接近心脏定向递送的系统性平台
Arrowhead在心脏递送领域的布局代表了当前最具创新性的技术突破。其核心策略是利用GLP-1受体(GLP-1R)作为心肌靶向的入口,GLP-1R在心肌细胞表面有基础表达,尤其在心房组织中密度相对较高。与传统认知不同,Arrowhead的设计逻辑并非单纯依赖受体高表达,而是巧妙利用心脏作为全身灌注最充分的器官之一这一解剖学优势:在持续高频的循环灌注下,即使单位面积受体密度不高,单位时间内与受体发生接触和结合的siRNA分子总量依然可观。这一循环暴露×受体接触概率×内吞效率的乘积效应,是GLP-1R路线可行性的关键科学基础。
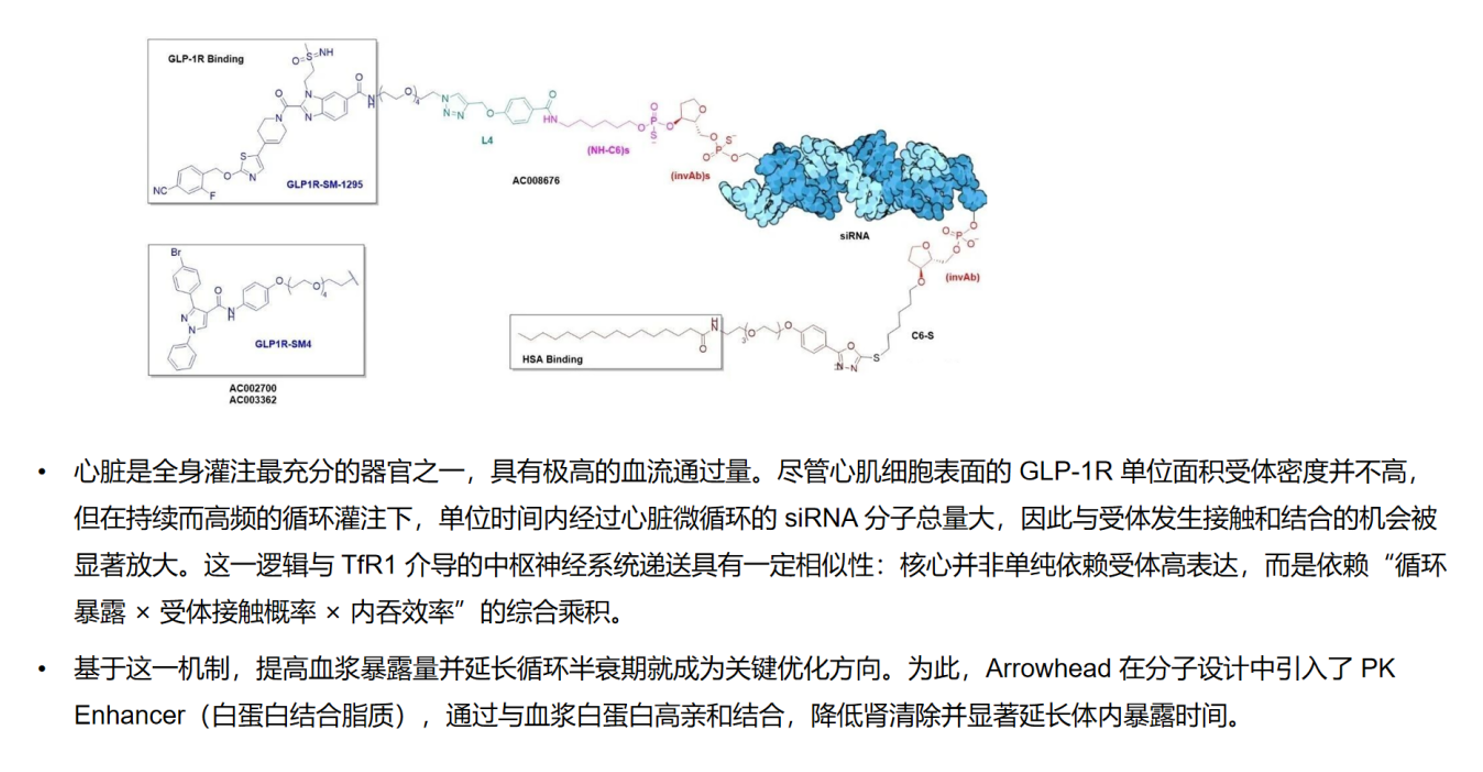
为了最大化这一乘积效应,Arrowhead在分子设计中引入了PK Enhancer(白蛋白结合脂质),通过与血浆白蛋白高亲和结合,降低肾清除率并显著延长循环半衰期。在专利WO2026030212A1(于2025年7月申请)中,Arrowhead系统披露了从分子设计到NHP验证的全链条数据。
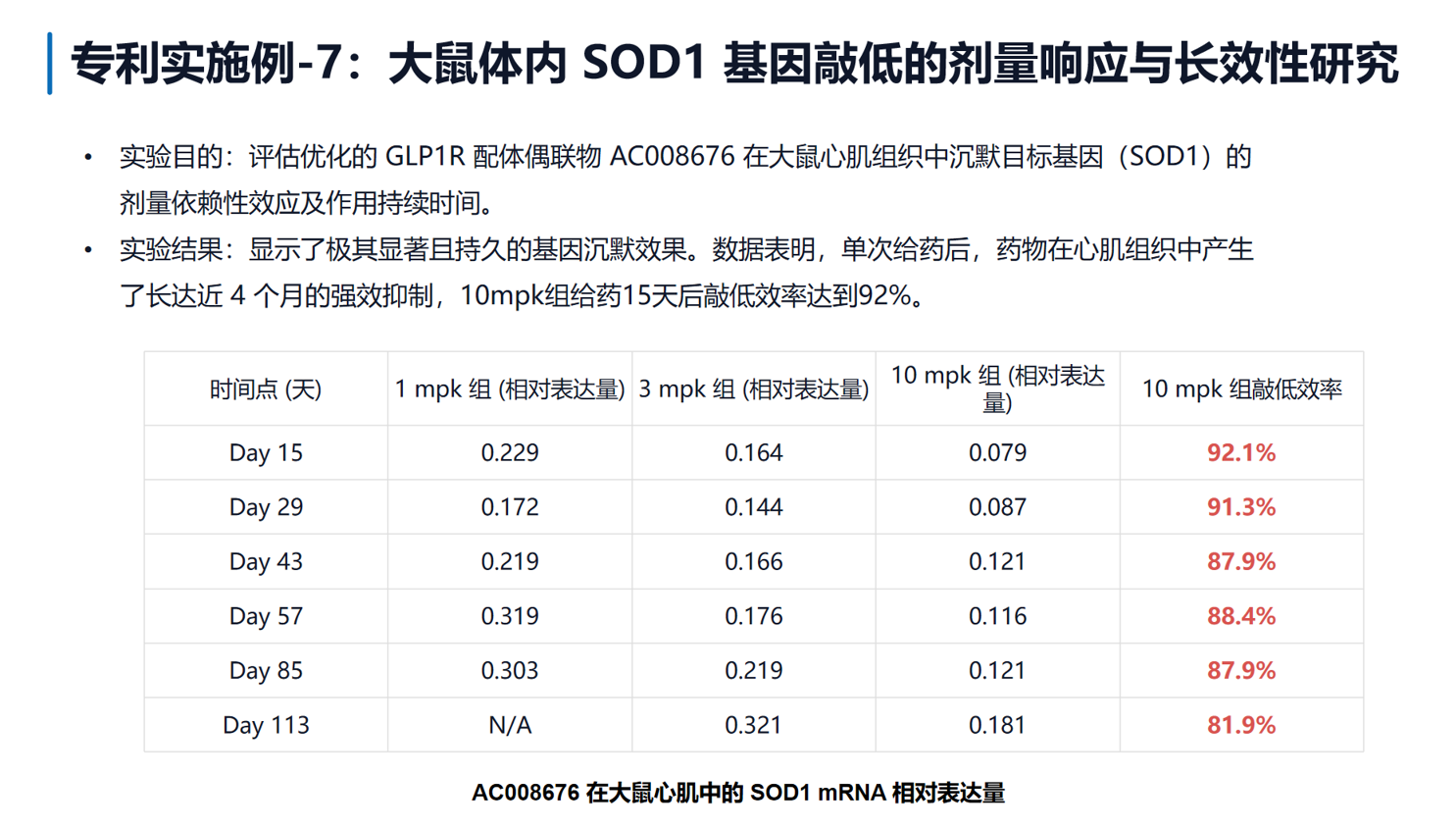
大鼠体内数据展现了惊人的长效性。优化后的GLP1R配体偶联物AC008676在大鼠心肌中产生了长达近4个月的强效基因沉默:10 mg/kg剂量下第15天SOD1敲低效率超过92%,第113天仍维持在80%以上;即使低剂量1 mg/kg,在第29天也达到了约83%的敲低。
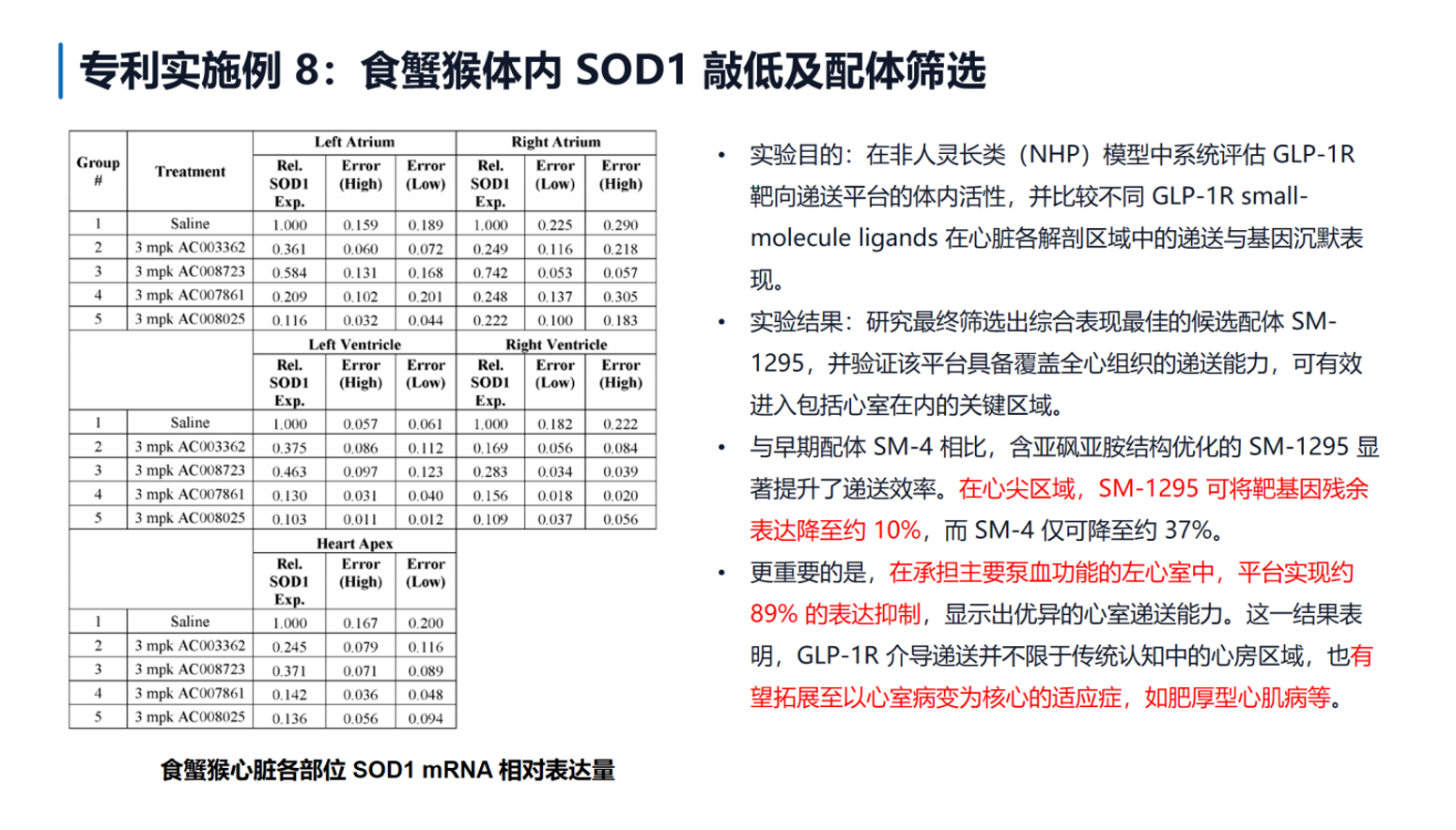
食蟹猴数据是该路线最核心的验证。研究筛选出综合表现最佳的候选配体SM-1295,其含亚砜亚胺结构优化显著提升了递送效率。在心脏各解剖区域中,SM-1295在心尖区域可将靶基因残余表达降至约10%,在早期配体SM-4仅降至约37%的基础上实现了质的飞跃。最关键的发现是左心室(体循环泵血功能)实现了约89%的敲低,这打破了以往认为GLP-1R仅在心房高表达、难以治疗心室疾病(如肥厚型心肌病)的传统认知。
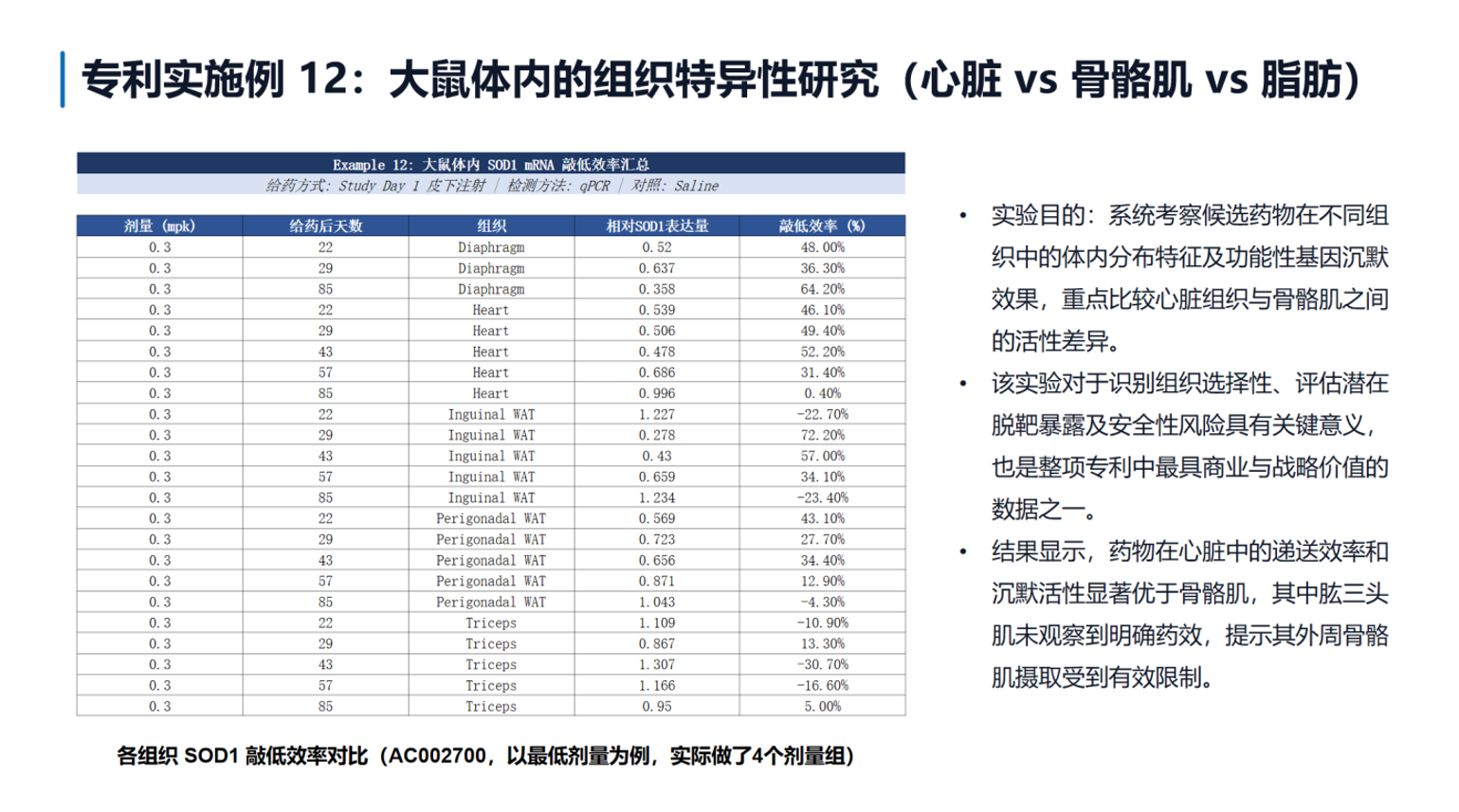
组织选择性数据进一步凸显了GLP-1R路线的独特优势。在大鼠组织特异性研究中(实施例12),AC002700皮下给药0.3 mg/kg后,心脏中SOD1敲低效率达31-52%(22-85天内),而骨骼肌(肱三头肌)完全无效。这一强心脏/弱骨骼肌的选择性模式与TfR1和αvβ6路线的泛肌肉特征形成鲜明对比。
2.3 Alnylam αvβ6路线:心肌与骨骼肌的双重覆盖
Alnylam在αvβ6路线上的心脏递送探索与肌肉递送一脉相承。如前文所述,αvβ6整合素在心肌中也有一定表达,因此αvβ6配体偶联的siRNA天然具备跨肌肉-心脏递送的潜力。在专利WO2025259743A1的实施例12-18中,Alnylam系统验证了这一假说。
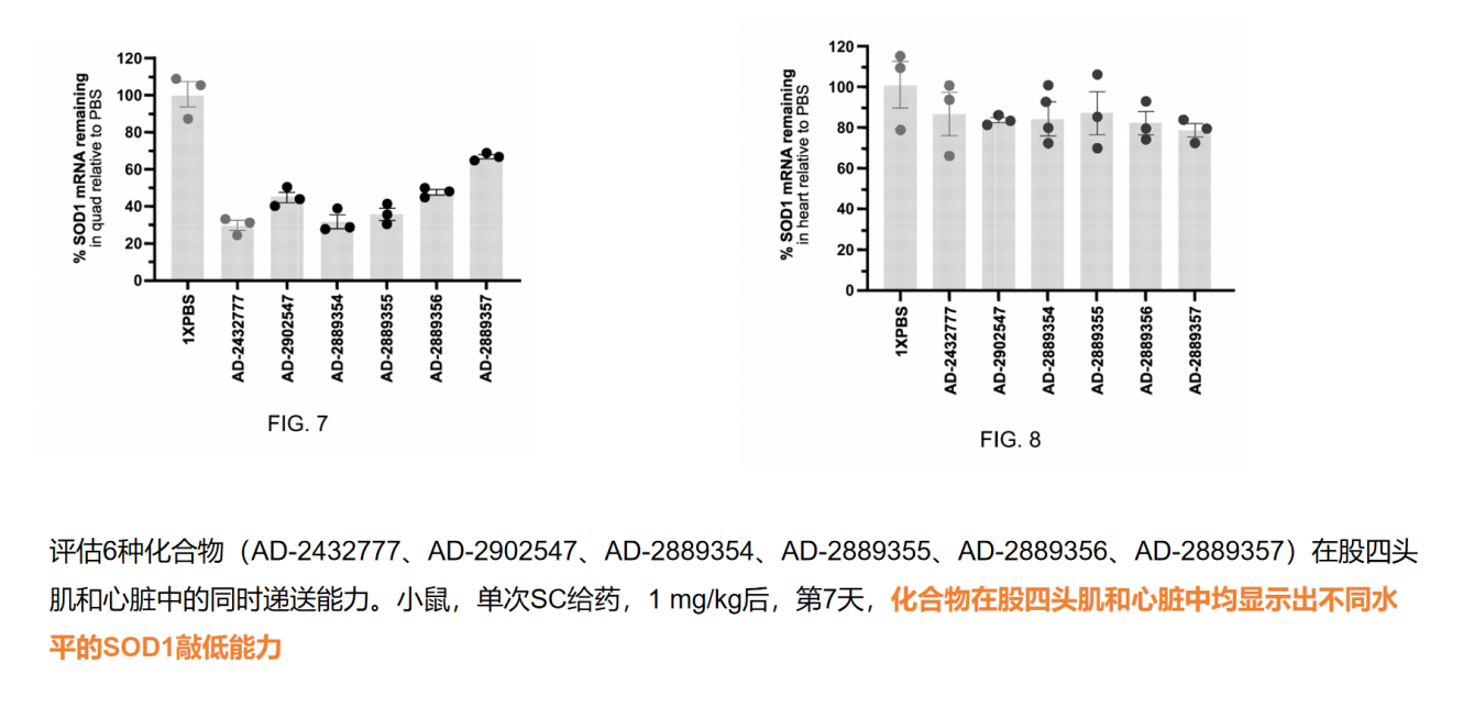
在小鼠模型中,6种化合物(AD-2432777、AD-2902547等)在1 mg/kg皮下给药后第7天,同时在股四头肌和心脏中实现了SOD1敲低。在更严格的低剂量IV给药(0.3 mg/kg)筛选中,16种双偶联化合物在股四头肌和腓肠肌中均实现>75%敲低,在心肌中敲低约10%~20%。这一数据说明在小鼠中αvβ6路线的心脏递送效率约为骨骼肌的1/4~1/3。
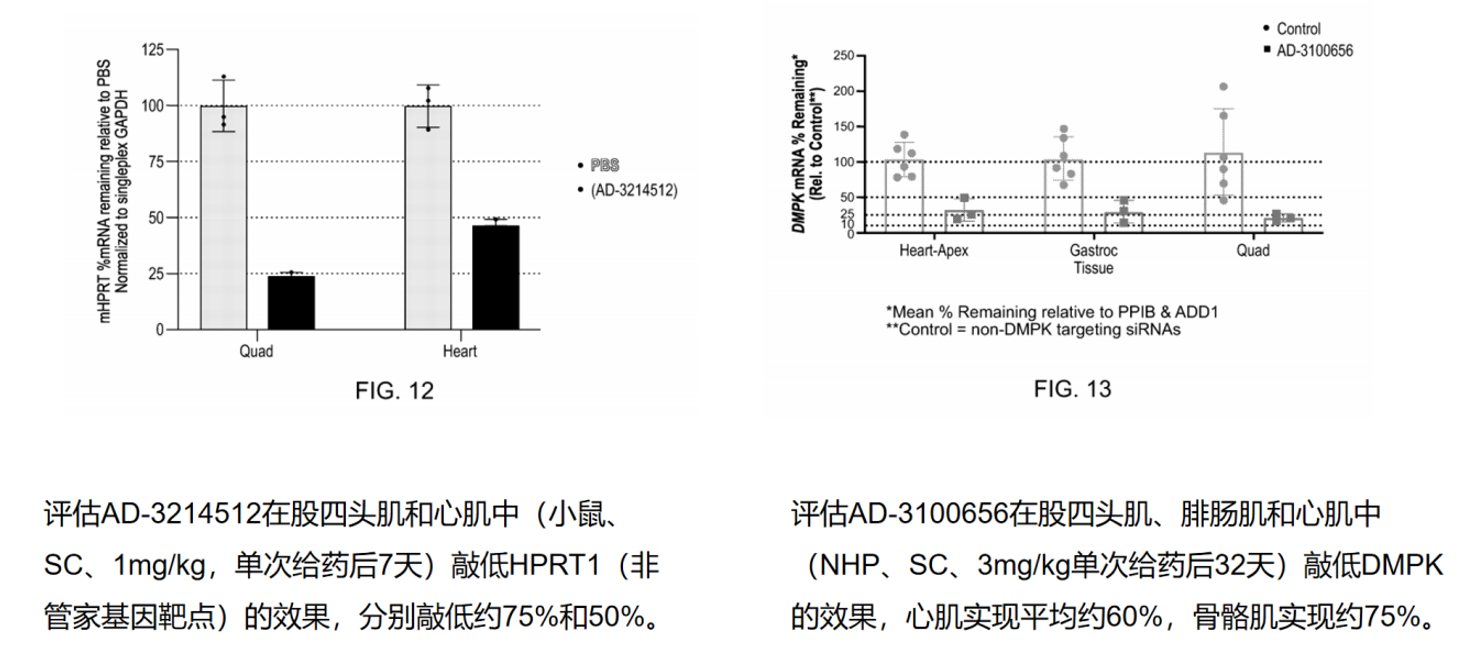
在疾病相关基因的验证中,化合物AD-3100656在NHP中皮下给药3 mg/kg后第32天敲低DMPK,心肌实现平均约60%的沉默,骨骼肌约75%。这一数据证实αvβ6路线在灵长类中确实具备心脏递送能力,虽然效率略低于骨骼肌,但对许多心脏适应症而言已具治疗意义。
值得注意的是,Alnylam在小鼠中测试了非管家基因HPRT1的敲低(AD-3214512,SC 1 mg/kg,第7天),在股四头肌和心肌中分别实现约75%和50%的敲低。使用非管家基因作为靶点排除了SOD1报告基因可能带来的系统偏差,增强了数据的可信度。
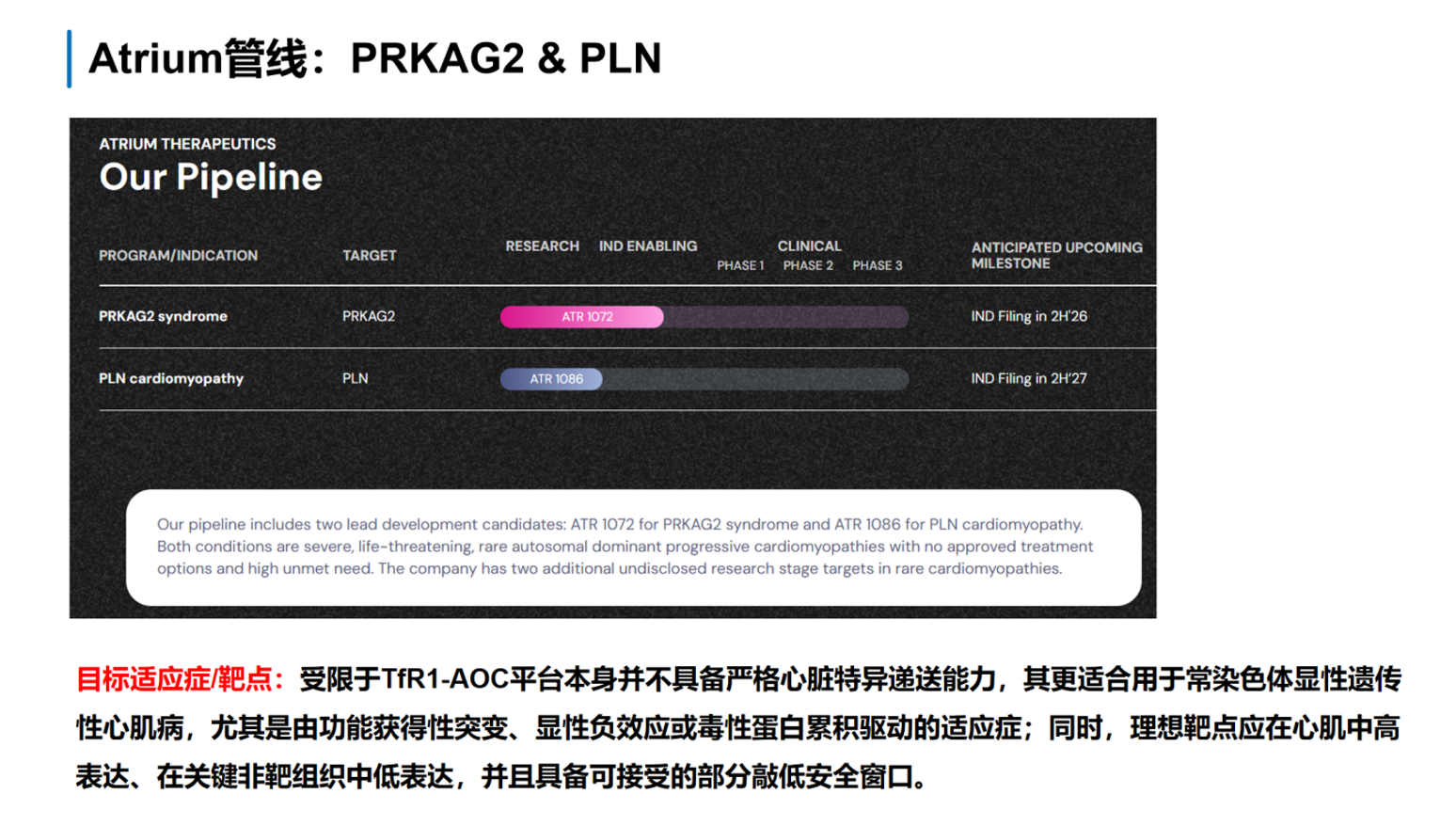
2.4 Atrium:TfR1 AOC在心脏的应用延伸
2026年从Avidity拆分独立上市的Atrium Therapeutics,传承了TfR1-AOC平台的技术积累,将其聚焦于心脏疾病领域。Avidity的原始组织分布数据已证明TfR1-AOC能够实现心肌有效敲低:在食蟹猴单次6 mg/kg给药后,尽管肝脏和肾上腺siRNA暴露最高,但只有骨骼肌和心脏表现出>50%的功能性敲低。
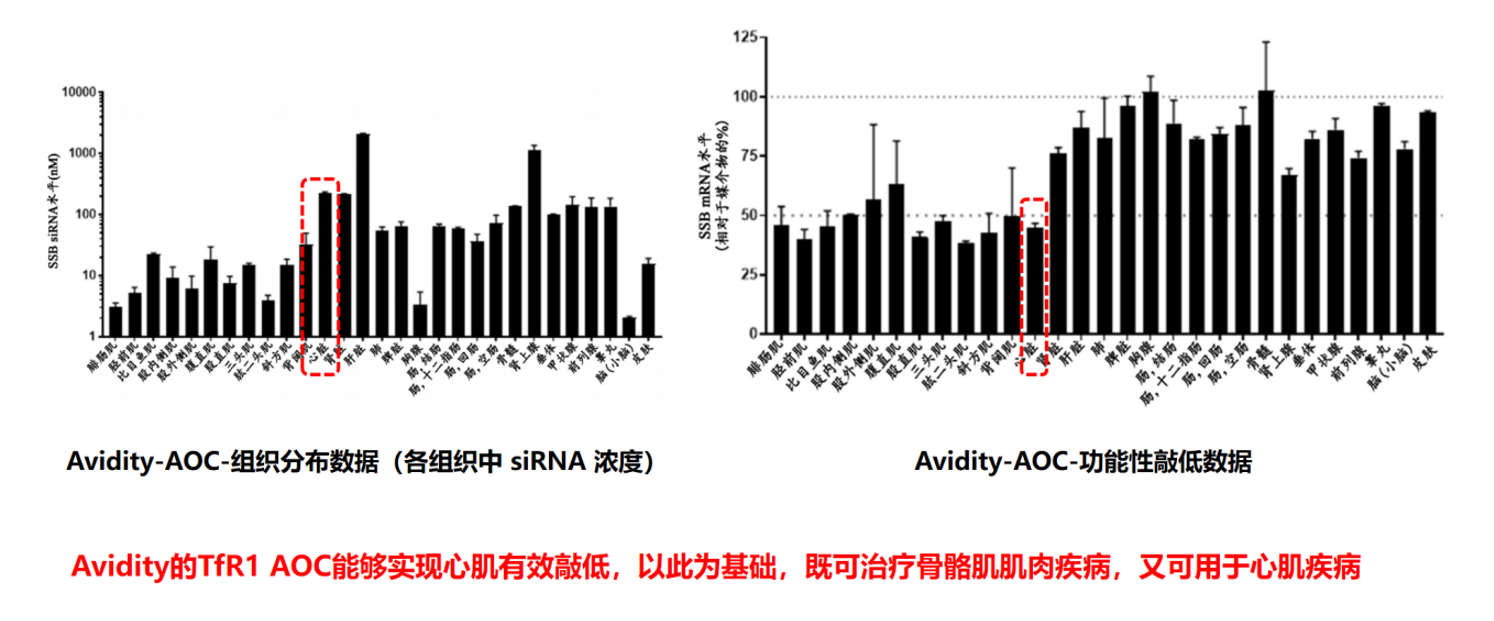
Atrium的战略定位在于利用TfR1-AOC治疗常染色体显性遗传性心肌病,尤其是由功能获得性突变、显性负效应或毒性蛋白累积驱动的疾病,如PRKAG2心肌病和PLN(受磷蛋白)R14del心肌病。这类疾病的共同特点是:靶点在心肌中高表达、在关键非靶组织中低表达,且具备可接受的部分敲低安全窗口。TfR1-AOC虽不具备严格的心脏特异递送能力,但对于显性遗传病而言,只要在心肌中实现足够深度的靶基因沉默,骨骼肌等外周组织的平行敲低未必构成治疗障碍。
2.5 心脏递送路线的战略抉择
当前心脏 siRNA/RNAi 递送正在形成三条代表性技术路线:TfR1(Avidity)、αvβ6(Alnylam)与 GLP-1R(Arrowhead)。三者本质区别在于进入心脏的同时,是否会被其他大组织分流。TfR1 与 αvβ6 路线通常兼具较强骨骼肌摄取能力,这对于治疗DMD等泛肌肉疾病具有明显优势,因为骨骼肌本身就是目标组织;但若用于纯心脏适应症,人体庞大的骨骼肌质量会形成典型的汇池效应,导致有效载荷被大量消耗,需要更高剂量才能达到心肌有效暴露,同时增加成本与全身不良反应风险。
相较之下,Arrowhead的GLP-1R路线展示出更强的去骨骼肌化特征。根据其公开专利数据,心脏组织可实现深度且持久的基因沉默,而骨骼肌组织响应极弱,说明该平台更接近真正的心脏定向递送。这一特性对于TTR心肌淀粉样变、肥厚型心肌病(HCM)、心衰、遗传性心肌病 等以心脏为主要病灶的适应症尤其关键,因为治疗窗口可能显著优于泛肌肉路线。
从产品化角度看,GLP-1R路线具备的优势包括:组织选择性强,有望以更低总剂量获得足够心肌暴露;长效潜力明显,若临床可复制动物数据,季度甚至半年给药具备想象空间。核心瓶颈首先是受体丰度有限:心脏的GLP-1R表达较低,因此需要较高的siRNA potency、配体亲和力及分子工程优化。其次是种属转化风险,动物模型中的受体定位与人类未必完全一致。第三是内源性竞争问题,大量使用Semaglutide等GLP-1药物的代谢患者群体,理论上可能影响受体占位与递送效率。
综上所述,TfR1 / αvβ6 更像是泛肌肉递送平台,GLP-1R则有如心脏精准递送平台。 前者适合肌营养不良等大组织疾病,后者更适合高价值、低剂量、强定向的心脏专科疾病。
三、肾脏靶向递送
3.1 肾脏递送的独特挑战与技术路线
肾脏是维持机体代谢平衡的核心器官,其结构复杂性在所有实质器官中首屈一指。肾单位包含至少26种独特的细胞类型,从肾小球足细胞到近端小管上皮细胞、髓袢升支粗段、远曲小管、集合管等,每一种细胞都可能成为特定肾脏疾病的靶标。遗传性肾脏疾病起源于肾单位的所有部分,这意味着肾脏递送技术必须具备高度的细胞类型选择性。
从解剖学和生理学角度,siRNA药物从血液到达肾脏靶细胞需要经历多重屏障:主要通过血液循环到达肾脏,经过肾小球滤过,受体介导的肾小管上皮细胞的内吞,以及从内涵体逃逸至胞质发挥RNAi效应。这一复杂路径决定了肾脏递送的技术门槛远高于肝脏。
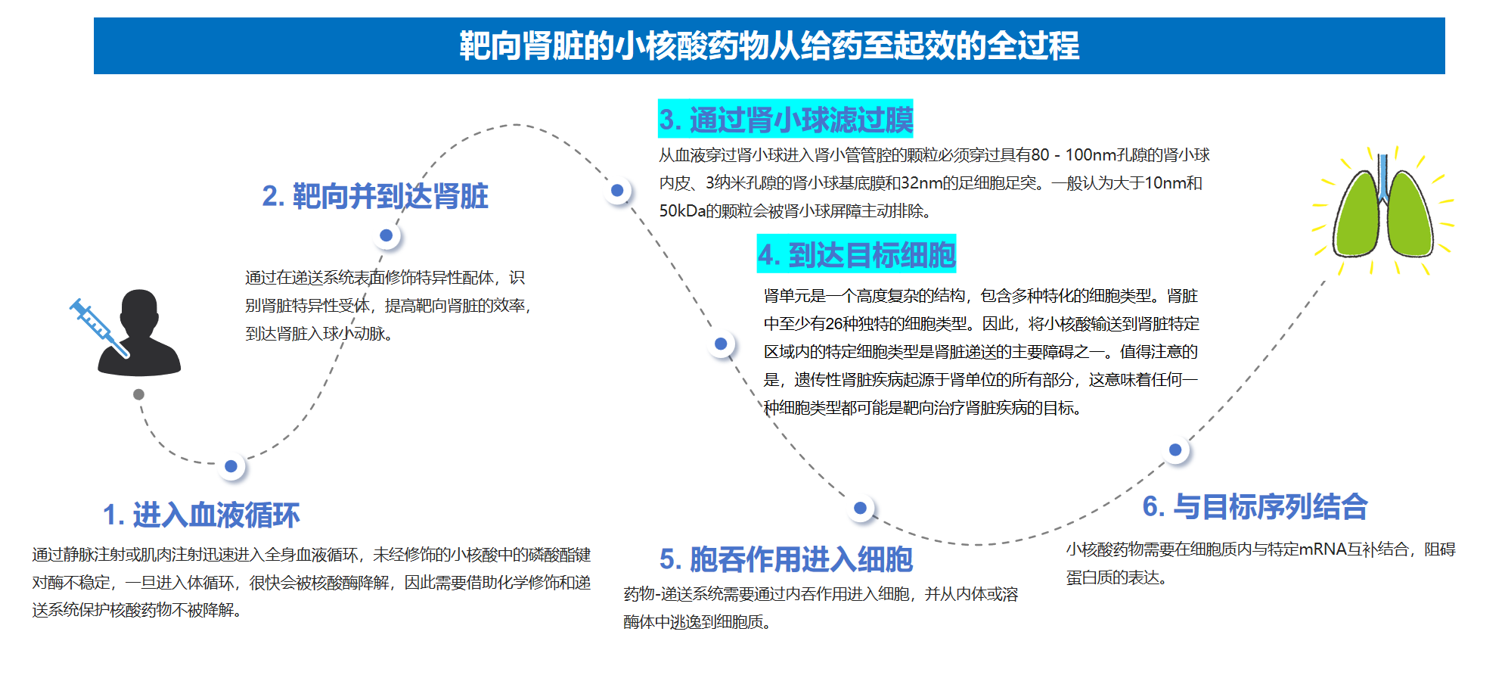
当前肾脏siRNA递送的技术路线主要包括:受体介导的主动靶向递送(以Judo Bio的Megalin路线为代表)、工程化病毒载体(AAV衣壳改造)、纳米载体(脂质/聚合物/外泌体等)以及局部递送(输尿管逆行插管、血管介入等)。其中受体介导的主动靶向路线因靶点多样性最强、临床转化信号最明确而备受关注。

3.2 Judo Bio STRIKE平台:Megalin(LRP2)路线的领跑者
Judo Bio是肾脏siRNA递送领域最引人注目的biotech公司之一。其核心平台STRIKE利用Megalin(又称LRP2,低密度脂蛋白受体相关蛋白2)受体实现siRNA向近端肾小管上皮细胞(PTECs)的高效递送。
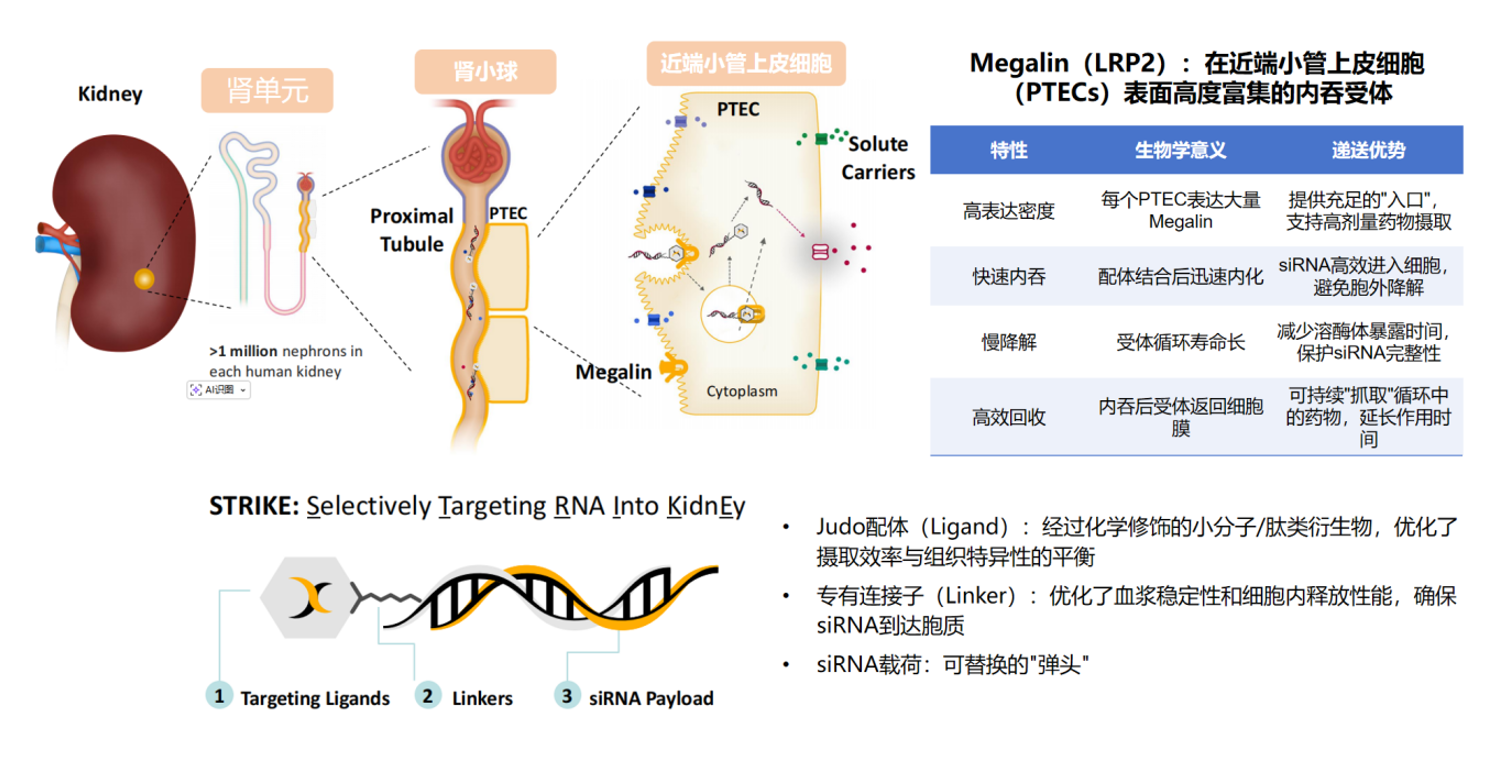
Megalin是一种分子量约600 kDa的大型内吞受体,在PTECs表面高度富集,是正常成人肾脏中表达最丰富的受体之一。其生物学特征使其成为理想的药物递送入口:每个PTEC表达大量Megalin拷贝,提供充足的药物摄取“入口”;配体结合后迅速内化,确保siRNA高效进入细胞;受体循环寿命长且回收效率高,可持续”抓取”循环中的药物分子,延长作用时间。Megalin的生理功能是介导多种配体(维生素结合蛋白、载脂蛋白等)的内吞和溶酶体降解回收,这一高效的分子转运机器恰好可被工程化改造用于药物递送。
Judo的分子设计包含三个模块:Judo配体(经过化学修饰的小分子/肽类衍生物,优化了摄取效率与组织特异性的平衡)、专有连接子(优化了血浆稳定性和细胞内释放性能,确保siRNA到达胞质)以及可替换的siRNA载荷(即“弹头“,可针对不同靶基因进行模块化替换)。

选择性蓄积验证:小鼠接受偶联荧光染料的megalin-STRIKERs给药(5 mg/kg)后4小时,IVIS活体成像和组织切片荧光显微镜分析显示,偶联物被近端小管上皮细胞强效且特异性地摄取,肾脏荧光信号远高于其他器官。更关键的是,在NHP模型中实现了肾脏:肝脏 >10:1的选择性比,甲状腺和睾丸暴露量低,排除了对内分泌系统和生殖系统的潜在脱靶效应。
模块化验证:小鼠接受靶向不同基因的megalin-STRIKERs给药(10 ml/kg)后第7天,所有测试靶点在肾脏中均实现40-70%的mRNA敲低。这些工具基因在近端小管上皮细胞中的相对表达水平呈现稳定的排序规律(Gene 1 > Gene 2 > Gene 3),证明STRIKE平台的模块化特性,单一配体-连接子设计可应用于多种不同siRNA靶点,无需为每个新靶点重新优化递送系统。
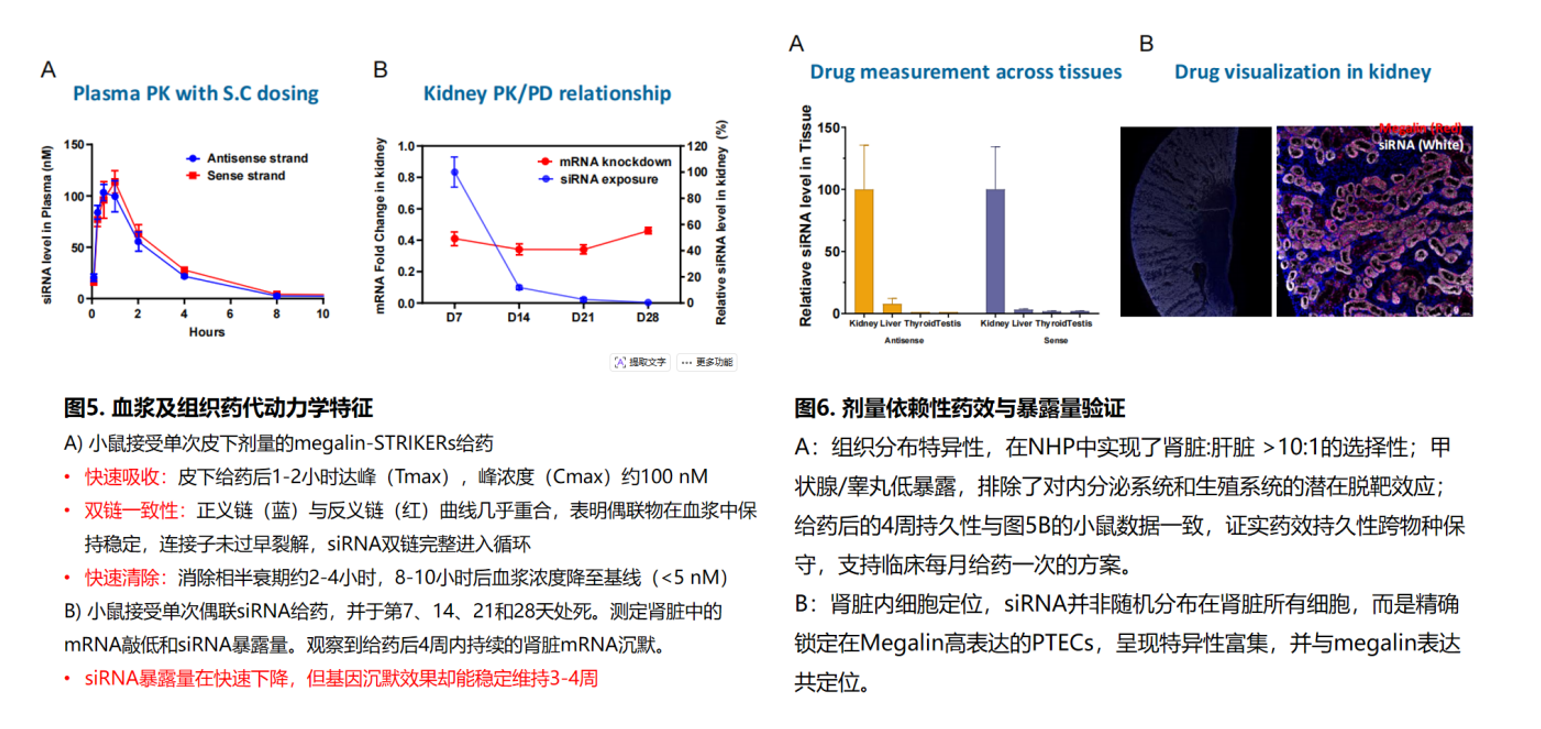
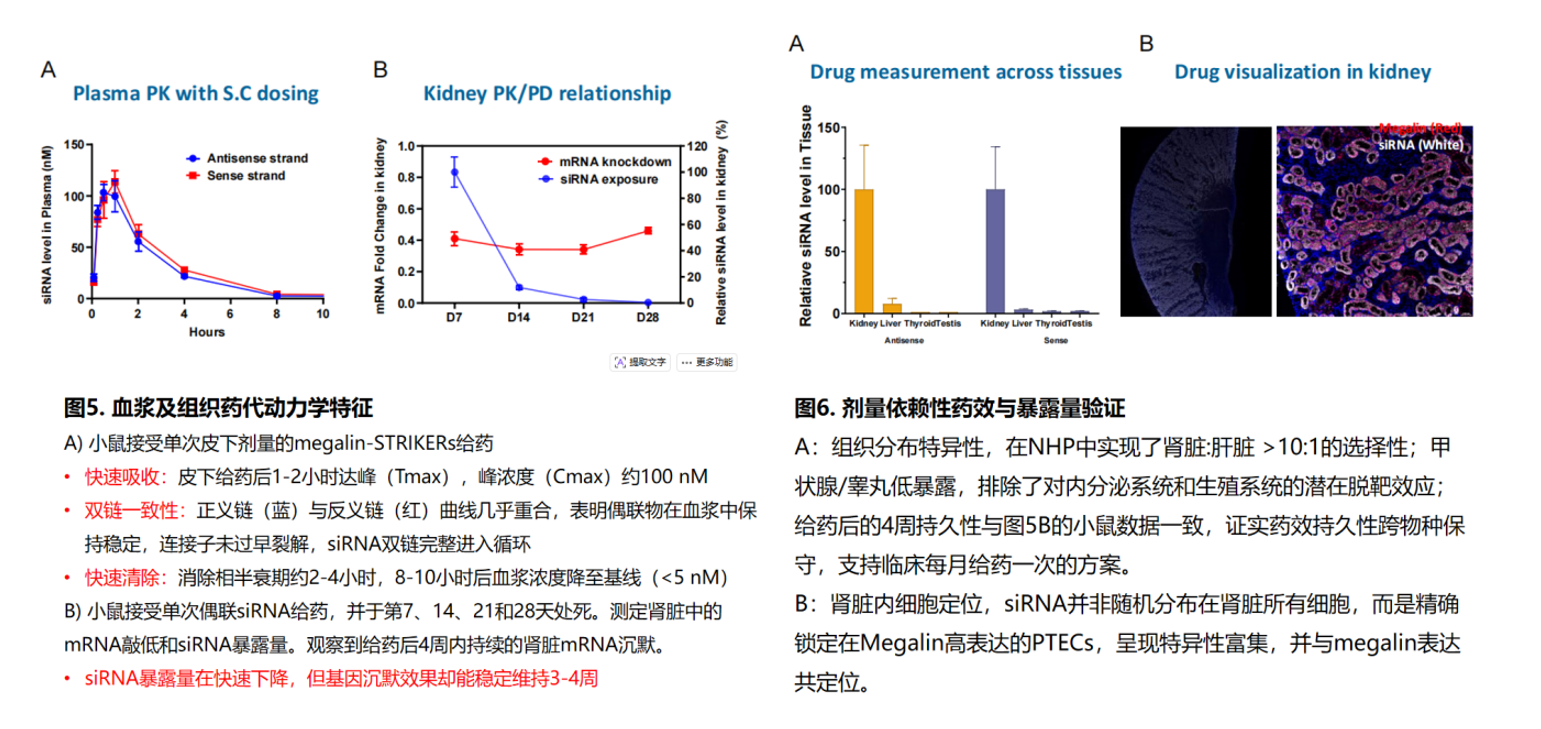
药效持久性:单次皮下给药后,L1a和L1b两种STRIKERs变体均实现了持续的肾脏基因敲低,40天时达到峰值接近70%,且在给药后4周内siRNA暴露量虽快速下降,基因沉默效果却能稳定维持。NHP数据进一步证实药效持久性跨物种保守,支持临床每月给药一次的给药方案。
NHP肾脏靶基因敲低的组织学验证:通过原位杂交(ISH)在给药后9周进行检测,靶基因沉默在组织水平依然可见,且敲低信号严格局限于Megalin阳性区域(PTECs),非靶细胞(如肾小球、间质)不受影响。这一细胞类型特异性是功能性安全的关键保障。
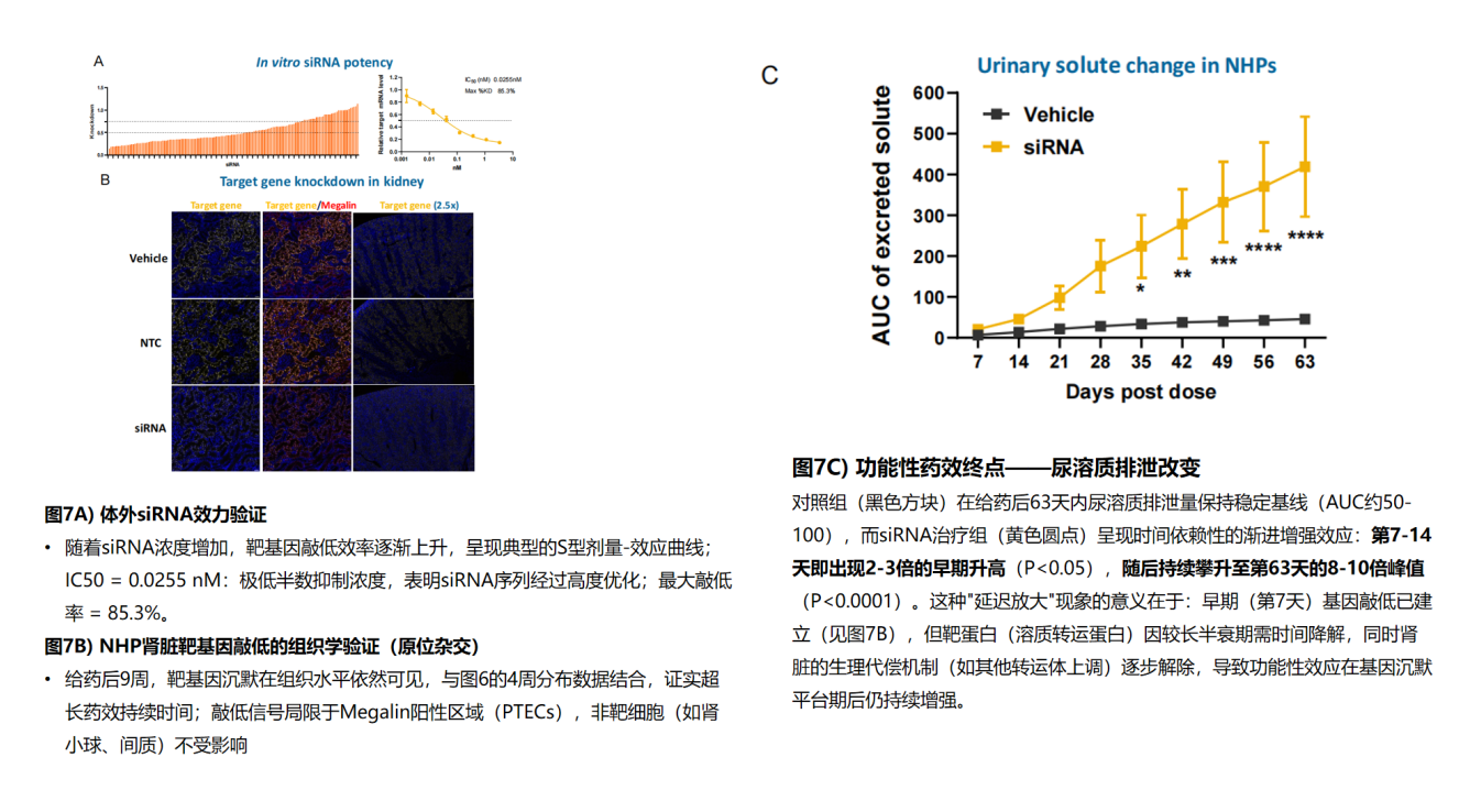
功能性药效终点:siRNA治疗组呈现时间依赖性的渐进增强效应,第7-14天尿溶质排泄量即出现2-3倍的早期升高,随后持续攀升至第63天的8-10倍峰值。这种延迟放大现象具有重要的药理学意义:早期基因敲低已建立,但靶蛋白(溶质转运蛋白)因较长半衰期需要一定时间降解,同时肾脏的生理代偿机制逐步解除,导致功能性效应在基因沉默平台期后仍持续增强。这一机制提示肾脏RNAi药物的功能性疗效评估需要足够长的观察窗口。
3.3 Megalin路线的结构性优势与局限
在当前肾脏特异性递送的技术版图中,LRP2(Megalin)靶点路线正从众多探索路径中浮出水面,成为目前验证度最高、产业信号最明确的领先方案。这一判断的核心支撑来自Judo Bio扎实的临床前数据,在NHP模型中实现了寡核苷酸向近端肾小管的高效递送与功能沉默,初步验证了该受体介导路径的可成药性和治疗窗口。更重要的是,这条路线已经引发了明确的产业跟随效应:炫景生物、必贝特等小核酸Biotech也正在跟进。然而,在肯定其领先优势和产业确定性的同时,也须认知该路线固有的结构性局限。
病理依赖性是最需要关注的策略性风险。Megalin在肾小管上皮的高表达高度依赖细胞的健康状态,在早期糖尿病肾病(正常白蛋白尿期),氧化应激可诱导其代偿性上调;但随着慢性肾病(CKD)进展至中晚期,Megalin表达水平下调(机制可能包括肾小管损伤与Megalin脱落、TMAO介导的下调、蛋白尿超载和EMT与肾小管萎缩等)。这意味着Megalin路线的治疗窗口可能局限于CKD的中早期阶段,对于晚期肾病(ESRD)患者可能无效。适应症选择必须精准定位Megalin高表达的黄金窗口期。
细胞类型的单一性限制了适应症范围。Megalin介导的递送几乎排他性地指向PTECs,对足细胞、系膜细胞或肾小球内皮细胞无能为力。这意味着其在局灶节段性肾小球硬化(FSGS)、膜性肾病等以足细胞病变为核心的疾病中无效。
溶酶体陷阱是工程化层面必须突破的技术壁垒。Megalin的生理功能是将配体内吞后定向输送至溶酶体降解,而siRNA要发挥RNAi效应必须逃逸至胞质结合RISC。连接子的设计必须在溶酶体环境中实现可控释放,确保siRNA在降解前完成内涵体逃逸。
内源性配体竞争可能导致“配体陷阱”。生理状态下尿液中高丰度的维生素结合蛋白、载脂蛋白等内源性Megalin配体,可能与药物偶联物竞争结合位点,迫使治疗剂量升高,增加脱靶风险。
在适应症策略上,一个极具前瞻性的思路是:不局限于治疗肾脏本身的疾病,而是把肾脏当作全身代谢的调节枢纽,通过沉默近端小管高表达的溶质载体(SLC,最大的跨膜转运蛋白家族)来调控全身代谢平衡。肾脏高表达的SLC家族靶点包括URAT1(痛风)、SGLT2(糖尿病)、SLC7A9(肾结石)、SGLT1(糖尿病)、NCC(高血压)、NaPi-IIa(慢性肾病矿物质骨病)、NaPi-IIc(佝偻病/低磷血症)等。通过沉默这些转运蛋白,RNAi药物有望实现以肾脏为靶点的全身代谢疾病治疗,极大扩展了肾脏递送技术的临床价值。
3.4 肾脏递送的其他转运靶点
除了Megalin,多个研究团队正在探索肾脏其他细胞类型表面的受体作为递送入口:
NPR-C(利钠肽清除受体)位于足细胞和系膜细胞表面,结合ANP/BNP/CNP后内化降解。利用足细胞位于肾小球基底膜外侧的解剖优势,可绕过肾小球滤过屏障,通过受体介导的内吞将siRNA直接送入足细胞,为肾小球疾病的治疗提供了全新思路。
Cubilin同样位于PTECs刷状缘,辅助Megalin重吸收维生素-结合蛋白。Cubilin常与Megalin共同靶向,但单独不具备内吞能力,需依赖Megalin介导的内吞。Judo Bio等平台可能已在利用这一协同机制。
GGT(γ-谷氨酰转移酶)位于PTECs刷状缘,催化谷胱甘肽代谢并识别γ-谷氨酰基团。利用GGT识别GSH(谷胱甘肽)修饰的siRNA可实现肾小管靶向,这一化学修饰策略在技术上相对简便。
KIM-1(肾损伤分子-1)在受损肾小管上皮细胞中高表达,是一种磷脂酰丝氨酸受体,介导凋亡细胞清除。利用KIM-1可实现急性肾损伤(AKI)的精准靶向——药物仅在损伤区域富集,正常肾组织不受影响。这种疾病状态激活的递送策略具有极高的安全性优势。
CD36在缺氧条件下的近端小管上皮细胞中上调,针对AKI时的缺氧小管上皮具有靶向价值。
CD320介导钴胺素-转钴胺素复合物的内吞。利用钴胺素-siRNA-转钴胺素三元复合物,可通过CD320或LRP2双重介导进入肾脏细胞,为配体设计提供了更多化学空间。
这些靶点的探索表明,肾脏递送技术正在从单一Megalin依赖走向多靶点矩阵,未来可能根据不同肾脏疾病的细胞类型特异性选择最优递送入口。
下期预告:
在肝外siRNA递送的下篇中,文章聚焦于脂肪、肺、皮肤及脑组织等新兴拓展器官的技术突破与临床转化,将系统梳理肝外递送的产业拐点、未来图景。
关于濠麦科技
濠麦科技专注于生物医药领域,致力于通过大数据挖掘与分析、生物化学信息深度建模,结合人工智能工具,为药物发现提供深度技术服务。公司已建立靶点价值评估、资产价值评估关联、专利核心化合物预测等多个研发模型,至今服务超过30家医药上市企业及近100家生物医药企业,助力客户把握创新药发展机遇。团队成员中博士占比超过70%,学术背景覆盖药物化学、药理学、生物信息学及分子生物学等关键领域。
依托技术积累与创新团队,濠麦科技发展出三大业务方向:
濠麦咨询:聚焦创新药管线规划、靶点挖掘与立项评估。通过大数据分析与专家战略洞察,为企业提供立项筛选、研发策略优化及风险评估,发现差异化机会,规避专利与投资风险。
濠麦孵化:依托大数据预测与全球BD资源,挖掘与评估早期生物医药资产及技术平台,提供从立项到研发策略的全方位孵化服务,助力成果转化与价值落地,精准对接潜在合作方。
濠麦会员:依托自研技术矩阵及专家网络,提供跨国药企及肿瘤、自免、代谢等核心领域的深度立项与交易研究报告,助力会员低成本获取高价值的立项与投资洞见。
欢迎交流探讨
蔡鸿 技术挖掘与研判部负责人
电话:18578675942
邮箱:alex@hq-haomai.com
编辑 | 毛冬蕾
mao.donglei@PharmaDJ.com
访问研发客网站,深度报道和每日新闻抢鲜看