• Arrowhead 的 TRiM Adipose 平台通过双脂质偶联设计,成功将 siRNA 重定向至脂肪组织,核心项目 ARO-ALK7 在临床前及早期临床中表现出色;
• Arrowhead 的 TRiM Pulmonary 平台利用 αvβ6 整合素配体,实现siRNA 的肺上皮靶向递送;
• 针对皮肤递送,利用物理或纳米载体突破角质层是核心策略,新加坡国家皮肤中心的 siRNA 微针贴片在Ⅰ期临床试验中显示,60 天内瘢痕体积缩小效果优于传统硅凝胶贴;
• Arrowhead 的 TRiM-BBB 平台采用单价 TfR(转铁蛋白受体)结合的 Fab 片段与 siRNA 共价偶联,避免了二价交联导致的降解问题;
• 不同器官的递送壁垒差异极大,谁能率先在一个器官中建立标准化、可复制的递送范式,谁就更可能成为该器官赛道的定义者;
• 下一轮竞争的关键是工程化+产业化能力,专利布局的纵深、适应症选择的精准度、剂量-敲低-安全性的三角优化同样决定成败。
撰文|濠麦科技技术挖掘与研判部
四、脂肪组织:siRNA 肝外递送的重要靶器官
4.1 脂肪组织递送的独特挑战与技术路线
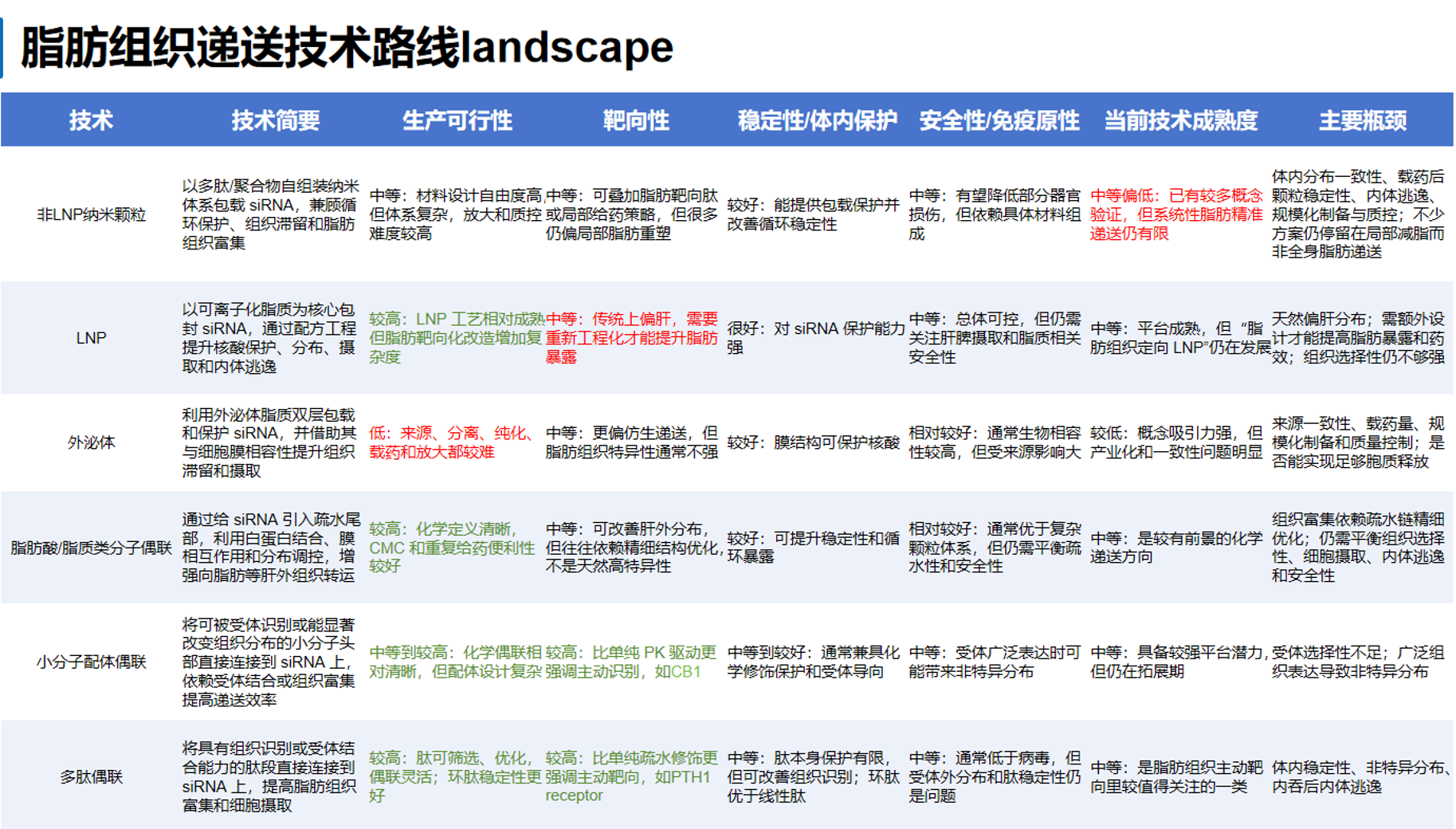
脂肪组织作为 siRNA 肝外递送的重要靶器官,具有不同于肝脏递送的独特障碍。首先,脂肪组织血管分布不均,不同脂肪库之间灌注水平、毛细血管密度和内皮通透性存在明显差异,导致系统给药后,药物进入脂肪组织的机会本身就受限。其次,成熟脂肪细胞体积大、胞内被巨大脂滴占据,细胞质空间相对有限,内吞活性和核酸摄取效率通常不如增殖活跃的细胞,因而 siRNA 即使到达脂肪组织,也未必能高效进入脂肪细胞并释放到胞质中。再次,脂肪组织不仅包含脂肪细胞,还富含前脂肪细胞、内皮细胞、成纤维细胞和免疫细胞,组织异质性较强,因此尽管容易进入脂肪组织,但未必进入目标脂肪细胞。此外,siRNA 在体内仍面临血浆蛋白结合、网状内皮系统清除、内体滞留以及肝脏优先摄取等普遍难题,而这些问题在脂肪组织递送场景下往往更加突出,因此脂肪组织递送的核心并不是单纯提高暴露量,而是同时解决组织到达、细胞摄取和胞质释放三个层面的效率瓶颈。
当前脂肪siRNA递送的技术路线主要包括:脂肪酸/脂质类分子偶联、小分子配体偶联、多肽偶联、工程化的外泌体、LNP和具有多样性的非LNP纳米颗粒。脂肪酸/脂质类分子偶联是目前技术成熟度较高的路线,因临床转化信号最明确而备受关注。
4.2 Arrowhead双脂质偶联平台(TRiM Adipose platform)
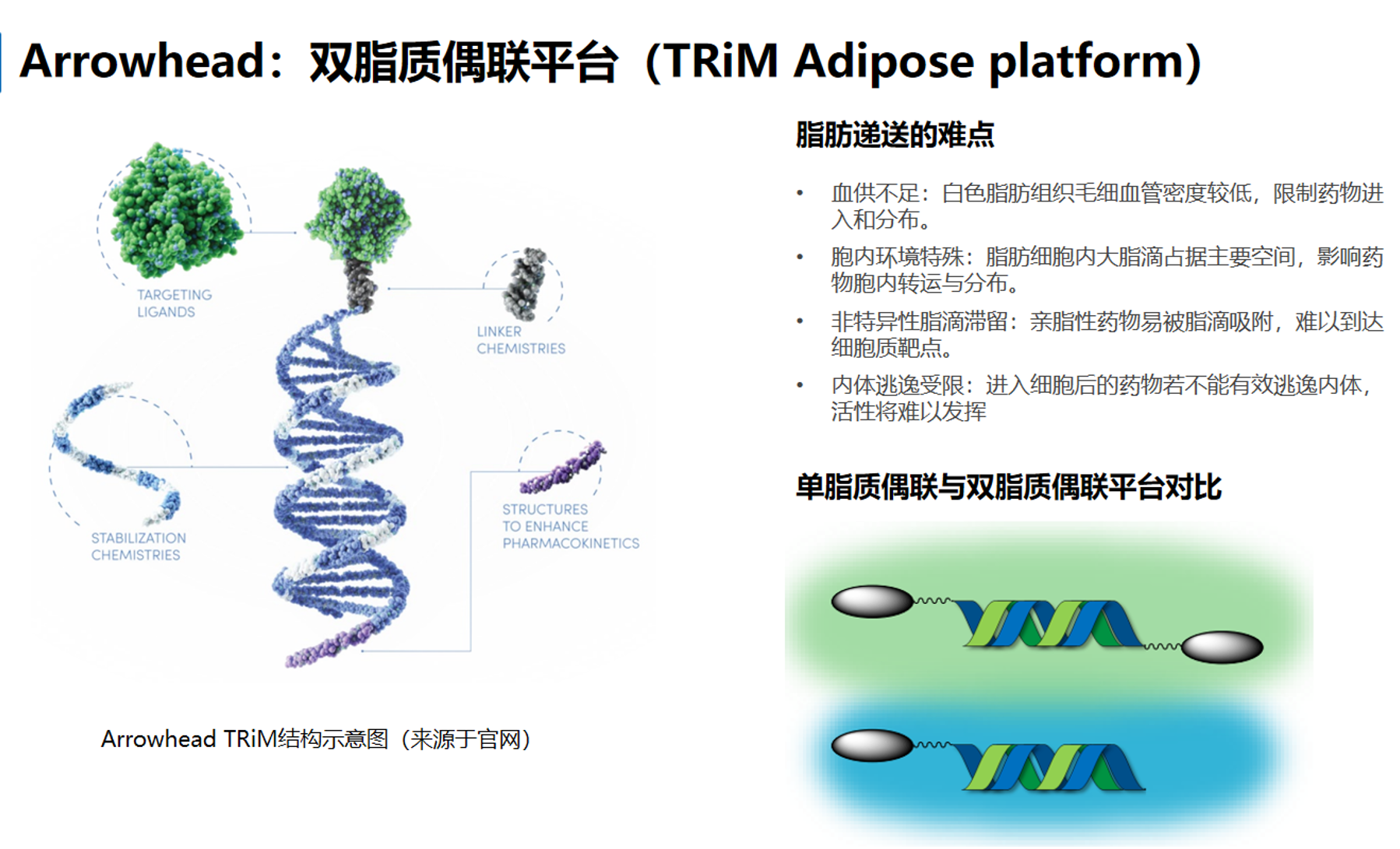
Arrowhead 的 TRiM Adipose platform,本质上是其 TRiM(Targeted RNAi Molecule)体系在脂肪组织递送上的一个分支,核心目标是把化学修饰的 siRNA 通过脂质偶联方式,尽可能从“容易进肝”重定向到“更容易进入脂肪组织/脂肪细胞”。从官方披露看,ARO-ALK7 是其代表性项目,也是 Arrowhead 明确用来证明该平台可实现脂肪细胞基因沉默的核心案例。Arrowhead 在 2025~2026 年的公开材料中反复将 ARO-ALK7 描述为首个进入临床、并在临床中显示脂肪细胞表达基因敲低的 RNAi 药物。
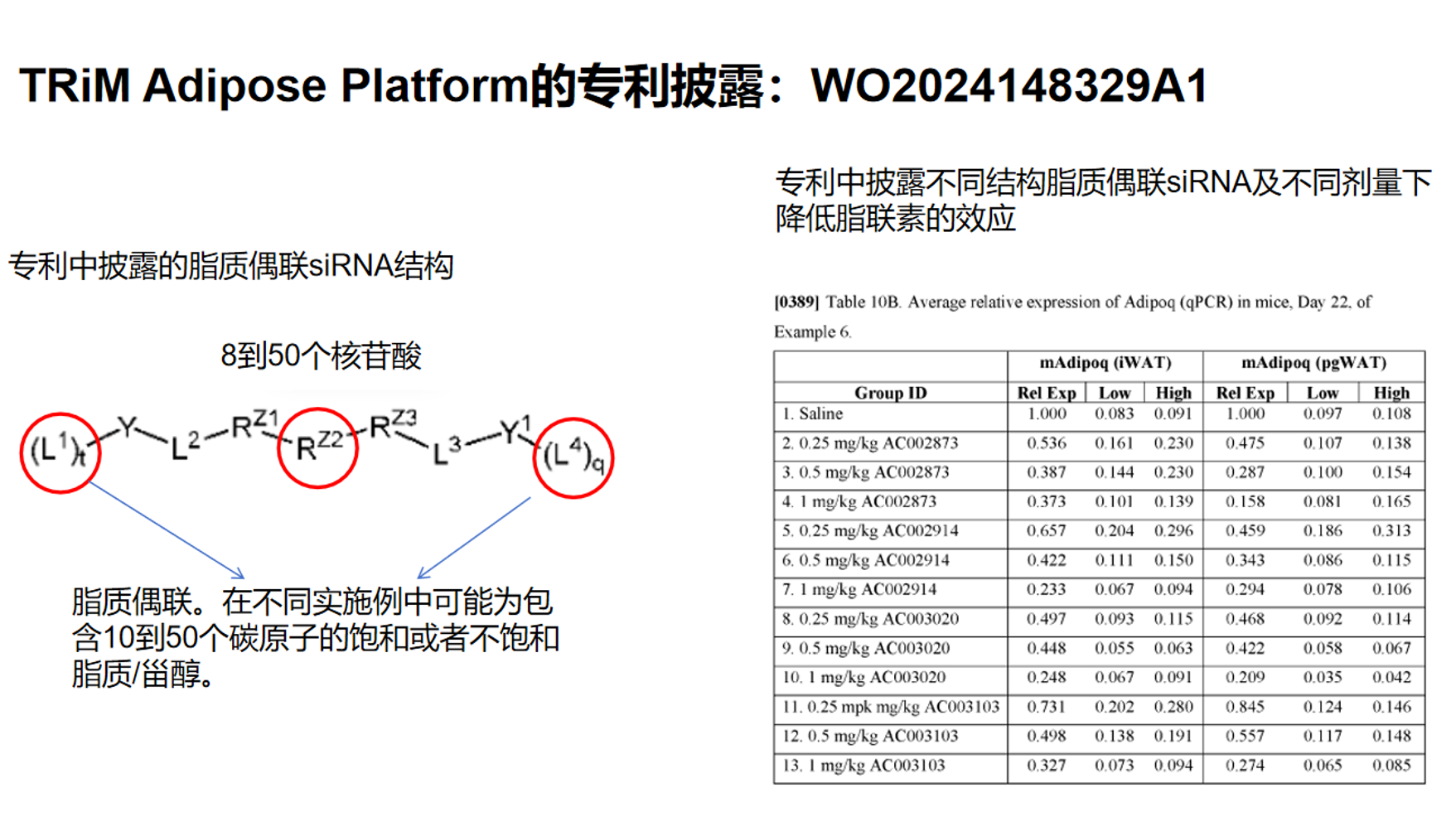
从结构思路上看,TRiM Adipose是定义明确的偶联型siRNA。专利 WO2024148329A1披露了相关的结构设计,其重点在于把 RNAi agent 与一个或多个脂质样 PK/PD 调节基团连接,通过改变体内分布、血浆结合、组织暴露和细胞摄取行为,提升脂肪组织递送效率。通过在siRNA上引入两个脂质端基或两个脂质相关模块,双脂质偶联进一步增强与体内疏水转运环境的相互作用,借此改善脂肪组织暴露和药效。
4.3 双脂质偶联平台的临床前研究
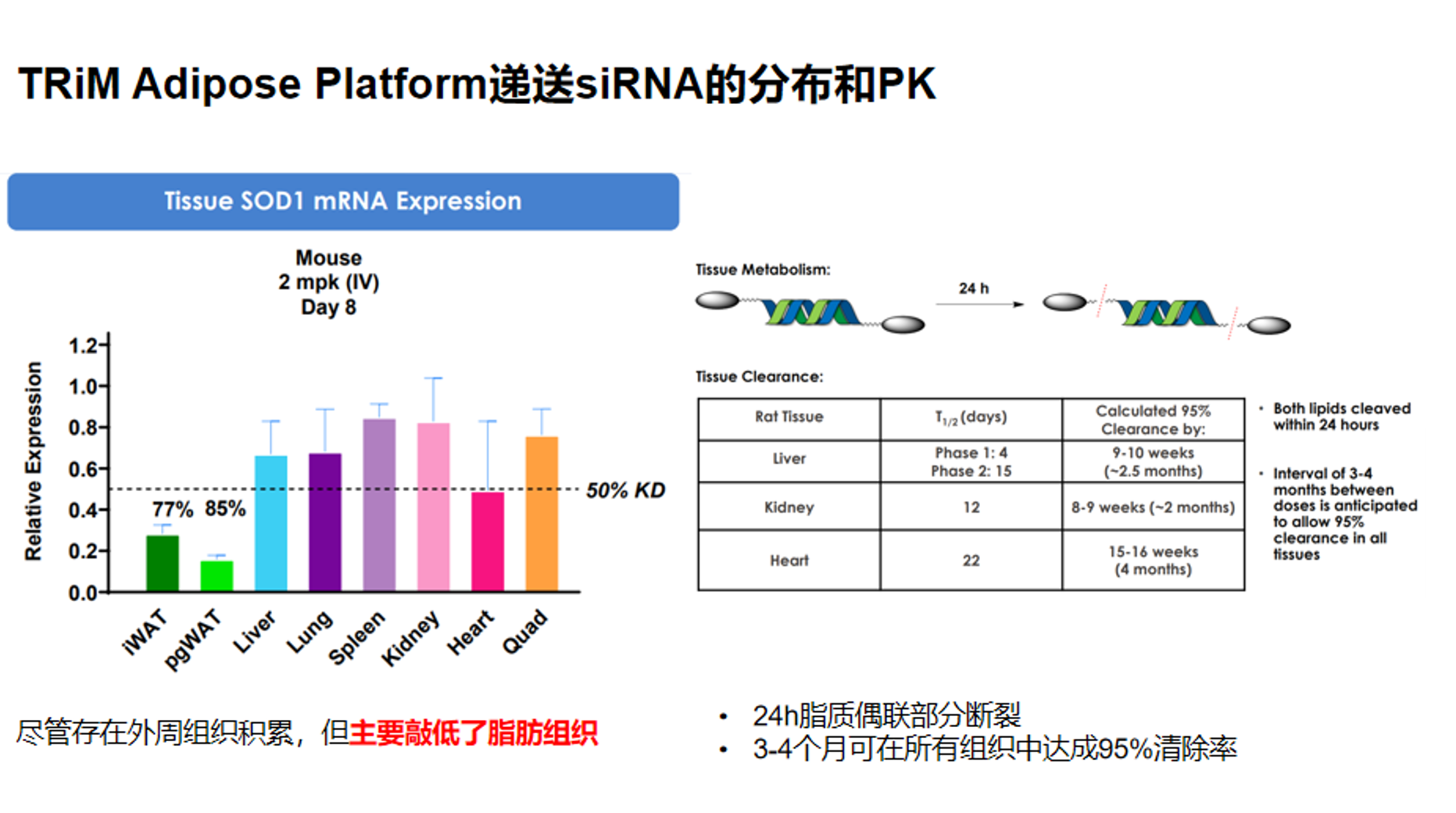
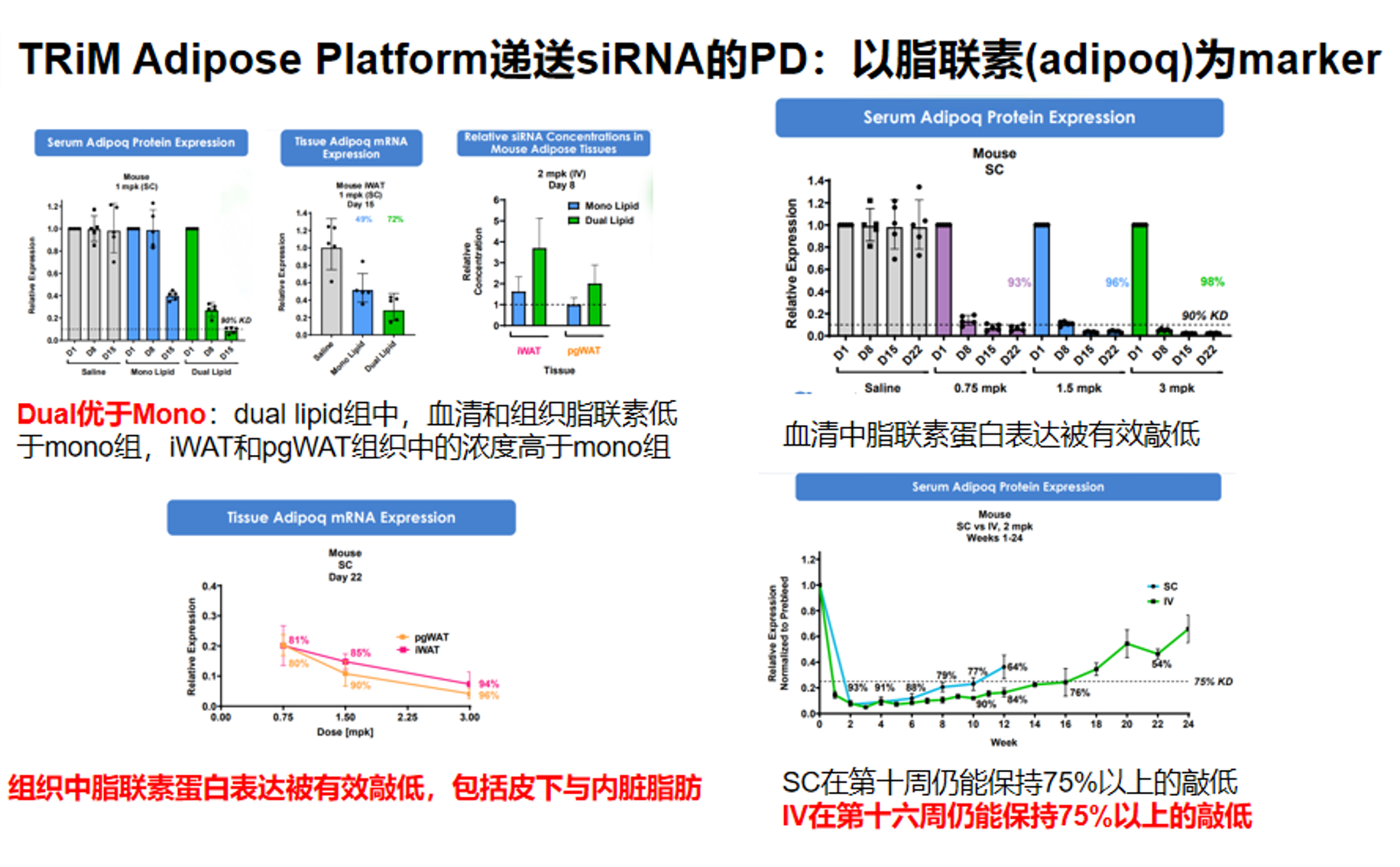
濠麦科技的数据库显示,双脂质偶联平台的临床前研究这一平台有优秀的脂肪组织递送表现,在以SOD1为工具基因的结果中,腹股沟脂肪(iWAT)和附睾周脂肪(pgWAT)敲低率达到77%和85%,远优于其他组织,说明了其优异的脂肪组织靶向作用。
从药效动力学看,该平台不仅能在皮下脂肪、还能在内脏脂肪中形成明显的靶基因抑制。图中可见,随着给药剂量的增加,血清脂联素蛋白表达可被有效降低,且脂肪组织中的 Adipoq mRNA 下降具有剂量依赖趋势。在给药持续性方面,皮下注射后第十周仍可观察到约75% 以上的敲低,而静脉给药在第16周仍维持约75%以上的敲低,提示该平台具有较好的长效特征。这说明 TRiM Adipose platform 不只是短暂的提高脂肪组织暴露,而是有能力在脂肪组织中建立持续性的 RNAi 药效。
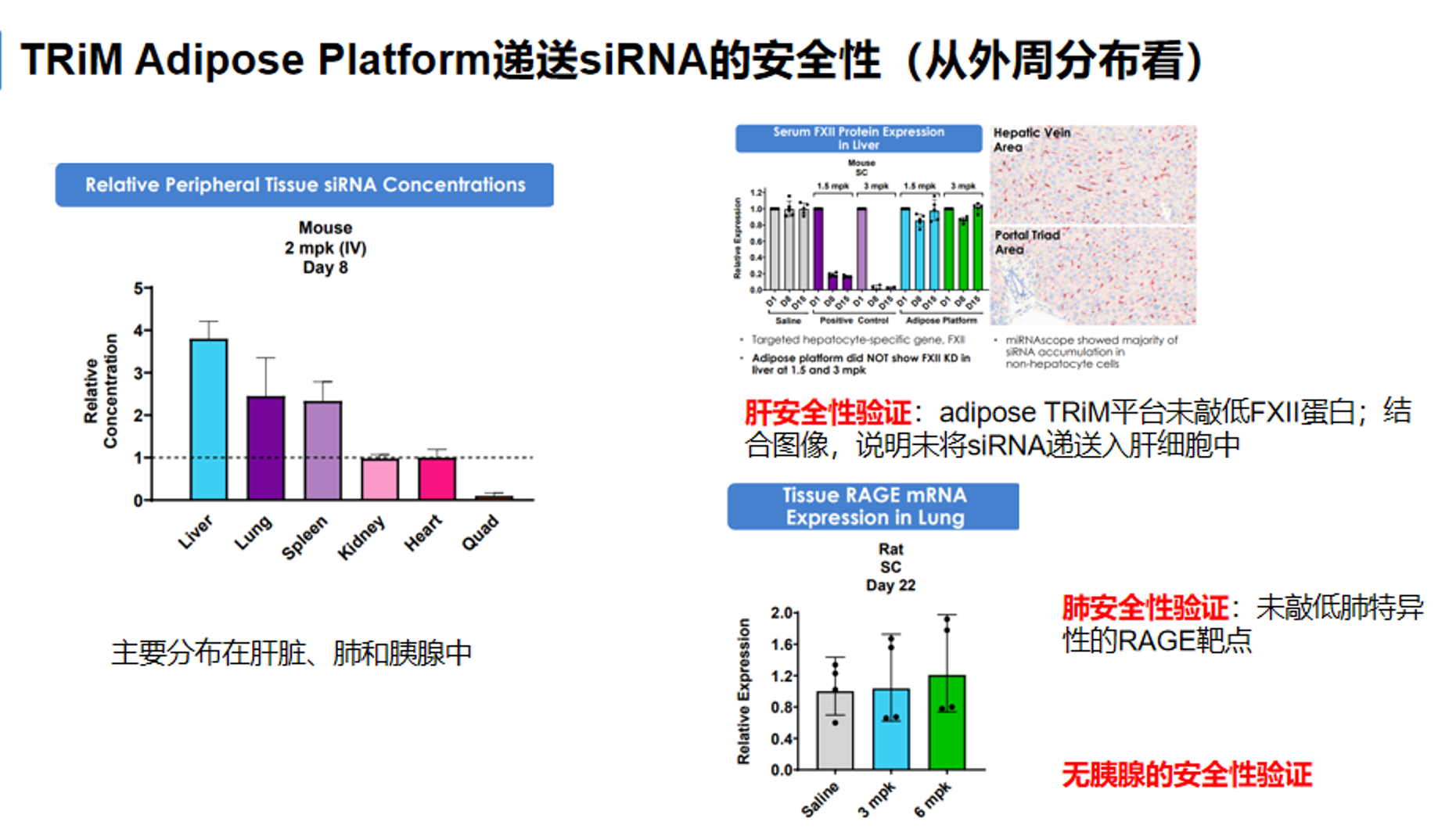
从外周分布与安全性验证来看,该平台虽然在肝、肺和脾等器官中仍可检测到一定的药物分布,但其主要目标仍是脂肪组织递送,尽管在肝中也有大量分布,但数据显示,其并未造成明确的不良反应。在以 FXI 作为肝脏安全性验证指标的实验中,结果显示在该平台条件下并未造成显著的肝脏 FXI 下调,提示其未表现出明显的肝脏偏向性药效;同时以 RAGE 作为肺部安全性验证指标,也未观察到肺组织中持续性的 RAGE 低表达。整体而言,这组数据支持 TRiM Adipose platform 具备较好的脂肪组织选择性、较强且持久的药效,以及相对可接受的肝肺外周安全窗口。
4.4 双脂质偶联平台的NHP研究
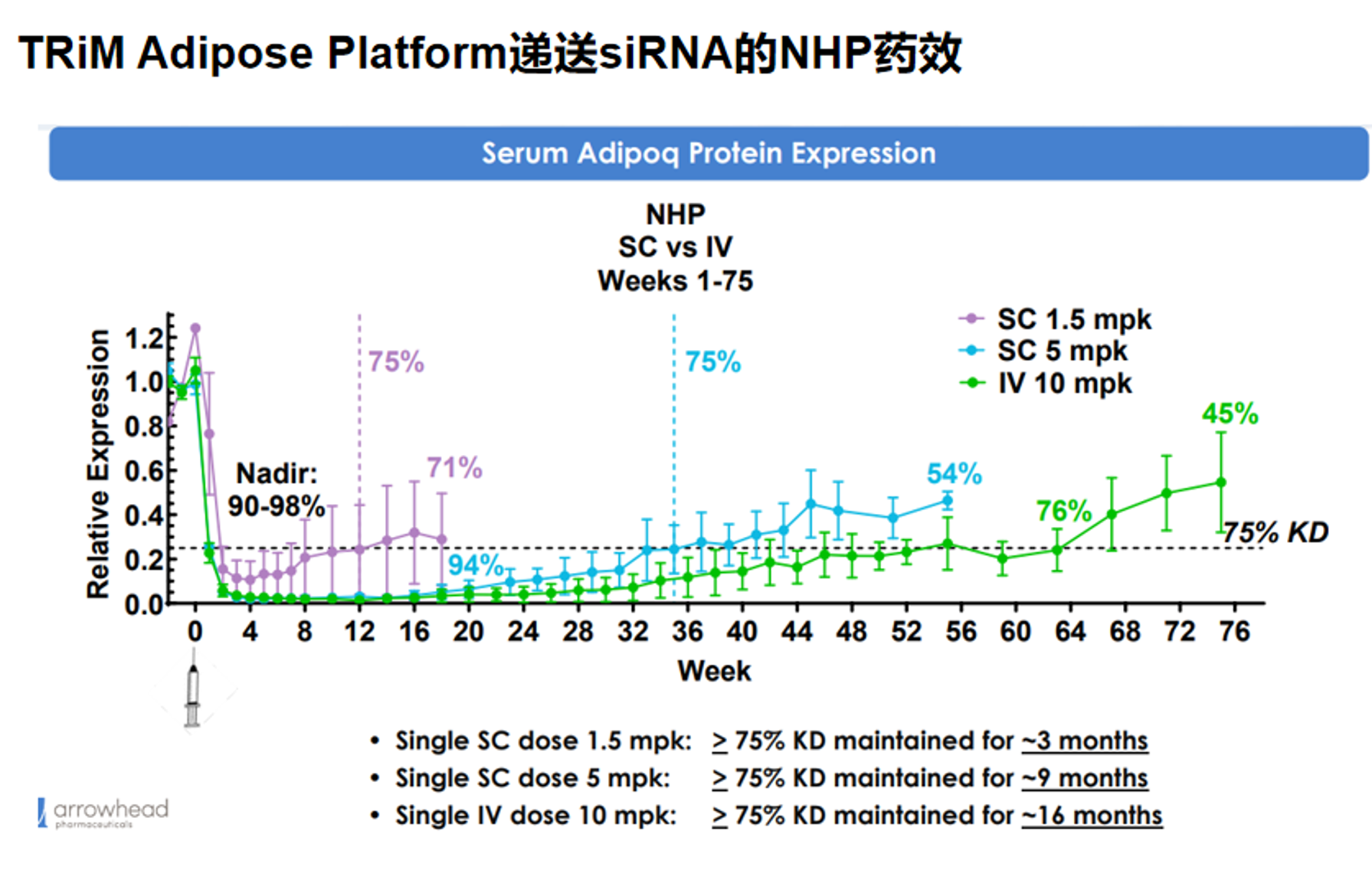
在非人灵长类动物研究中,该平台表现出较深且非常持久的脂肪组织药效。以血清 Adipoq 蛋白作为药效读出,单次皮下注射1.5mpk 后,最低点可达到约 90%~98%的敲除,且 75% 以上的敲低可维持约 3 个月;单次皮下注射 5mpk 时,药效更持久,75%以上敲低可维持约9 个月,并在较长时间内保持较低的蛋白表达水平;单次静脉注射10mpk 时,持续时间进一步延长,75%以上敲低可维持约16个月。整体看,下图说明该平台不仅能在NHP中实现高幅度基因沉默,而且具有非常突出的长效特征,并且药效持续时间随剂量和给药方式增强而延长,提示其在脂肪组织RNAi治疗中具备较强的转化潜力。
4.5 应用双脂质偶联平台的临床前研究:ARO-ALK7
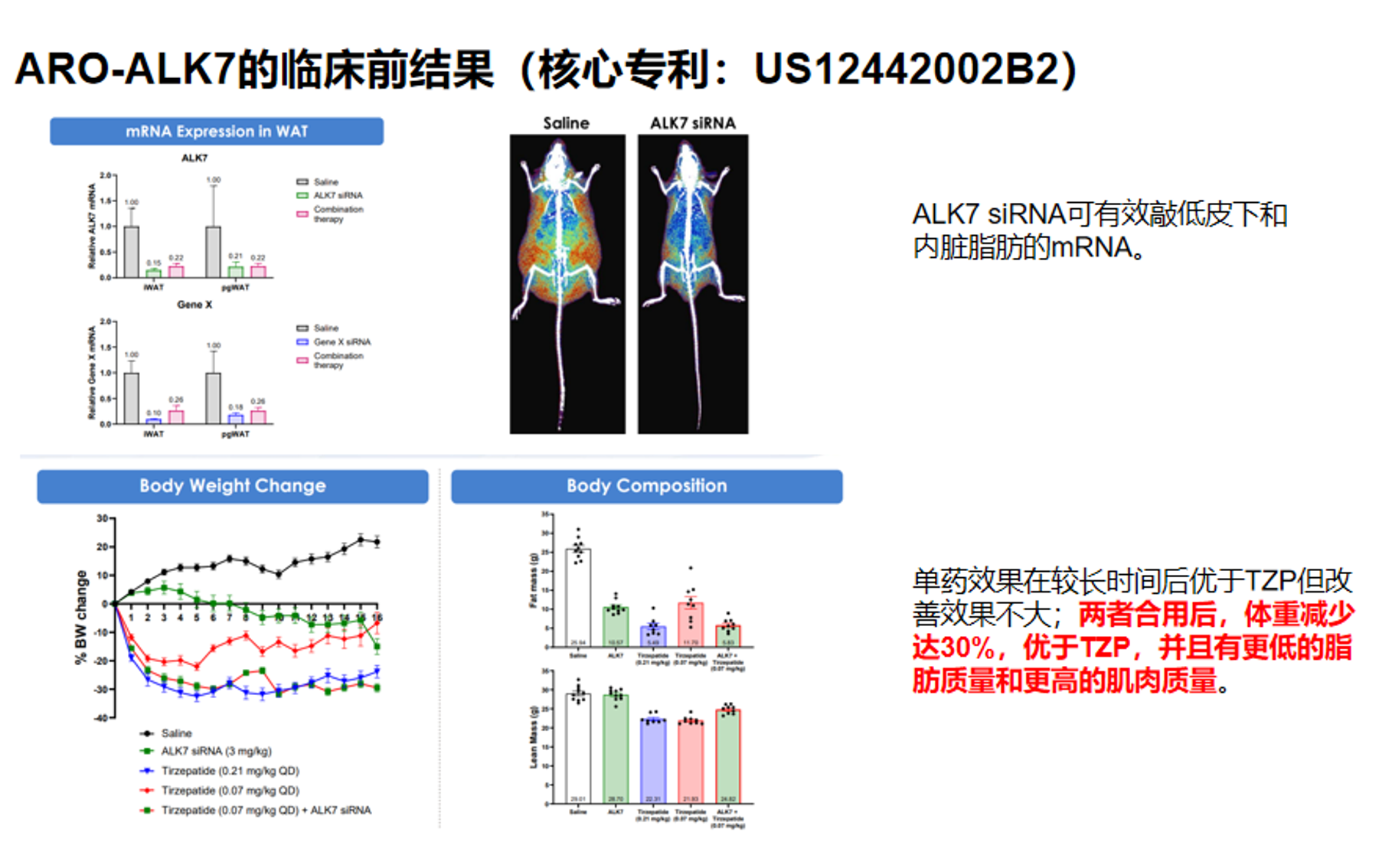
ARO-ALK7 的临床前结果显示,其具有明确的脂肪组织药效,并在减重和改善体组成方面优于对照处理。从下图中左上角的 mRNA 表达结果看,ALK7 siRNA 可明显降低脂肪组织中 ALK7 mRNA 水平,且在皮下脂肪和内脏脂肪中均可见下调,说明该药确实进入了目标组织并实现了靶点沉默。小鼠成像图也直观提示,ALK7 siRNA 处理后整体脂肪负担低于对照组。左下角体重变化曲线显示,ALK7 siRNA 组体重下降幅度劣于替尔泊肽(TZP),但与TZP共用后显著提升了TZP的减重效果至30%,达到了更低的脂肪质量及更高的肌肉质量。
4.6 应用双脂质偶联平台的临床研究:ARO-ALK7
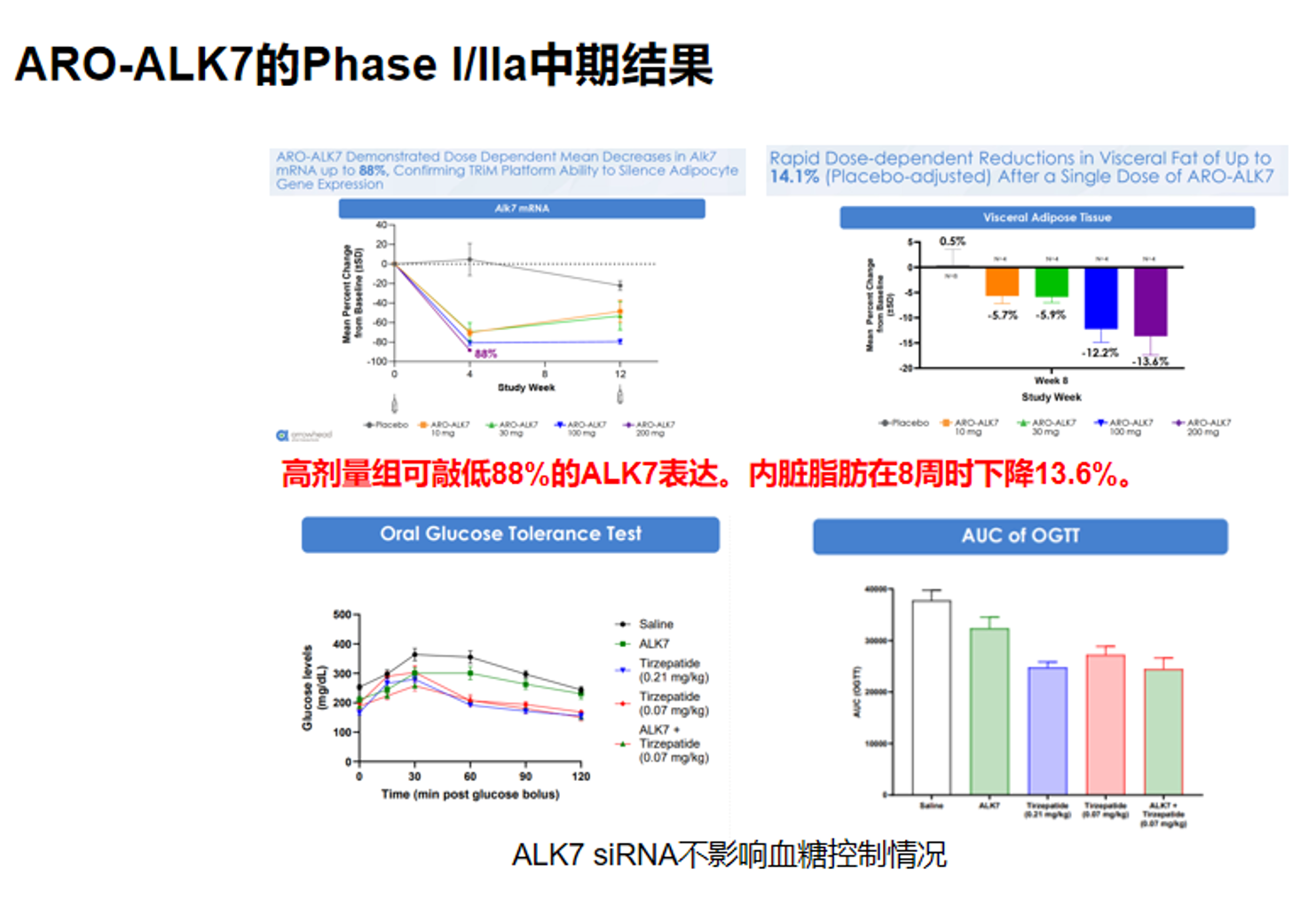
ARO-ALK7 的Ⅰ/Ⅱa 中期结果已给出了较明确的人体药效信号。下图显示,该药在腹部脂肪组织中可产生剂量依赖性的 ALK7 mRNA 下调,其中高剂量组可见约 88% 的 ALK7 表达降低,说明其在人群中不仅能到达脂肪组织,而且能够有效实现靶点沉默。右上图进一步显示,ARO-ALK7 对内脏脂肪也有较快且剂量相关的改善作用,在第 8 周时内脏脂肪可下降约 13.6%。与此同时,下方OGTT 曲线和 AUC 结果显示,ALK7 siRNA处理后血糖控制并未恶化,整体葡萄糖耐量表现与对照相近,说明在当前图示条件下,减少脂肪组织中 ALK7 并没有带来明显的不利的糖代谢影响。
五、肺部递送
5.1 肺部递送的独特挑战与技术路线
肺部siRNA递送的独特挑战,主要在于给药路径特殊、组织结构复杂、清除机制强、细胞类型高度异质。与肝脏相比,肺部更像一个同时存在多重屏障和多重非靶细胞竞争摄取的器官,递送难点通常可分为以下几个层面。
首先是解剖与沉积分布问题。如果采用吸入给药,药物是否能真正到达目标区域,首先取决于气溶胶粒径、流速、呼吸模式及气道几何结构。颗粒可能沉积在上气道、大气道,也可能到达小气道或肺泡,但不同疾病状态下气道狭窄、黏液增多、通气不均,又会进一步导致肺内分布不均。
第二个关键障碍是黏液与肺表面液屏障。呼吸道表面覆盖有黏液层或肺表面液,能捕获外来颗粒和核酸药物。对于siRNA来说,这意味着药物在接触到上皮细胞之前,就可能先被黏液黏住、稀释、聚集,或者随着纤毛清除系统被带出气道。尤其在哮喘、COPD、囊性纤维化、感染等状态下,黏液分泌增加且性质改变,这一屏障会更加明显。
第三是肺部强大的清除与防御系统。肺是直接暴露于外界环境的器官,因此,天然具有非常活跃的防御机制。吸入或进入肺部的颗粒可能被肺泡巨噬细胞快速吞噬,也可能被黏液-纤毛系统清除,还可能被局部蛋白、表面活性物质吸附后改变行为。其结果为,药物虽然进入了肺部,但很大一部分并不会进入目标细胞,而是先被“防御系统”处理掉。
第四是靶细胞类型复杂且异质性高。肺并不是一个由单一细胞组成的器官,而是包含气道上皮细胞、肺泡I/II型上皮细胞、内皮细胞、成纤维细胞、平滑肌细胞、巨噬细胞以及多种免疫细胞。不同疾病对应的真正治疗靶细胞并不相同。
第五是细胞摄取与内体逃逸仍然是决定性瓶颈。即便 siRNA 成功沉积到肺部并被某些细胞摄取,它仍需从内体中释放到胞质,才能进入 RISC 发挥沉默作用。很多肺部体系的问题并不只是组织到达不足,而是到达之后仍被困在内体中,导致实际药效弱于组织分布数据所显示的水平。
当前肺部siRNA递送的技术路线主要包括:αvβ6整合素配体偶联、AOC、亲脂性缀合、亲水/疏水缀合、病毒、LNP以及外泌体。αvβ6整合素配体偶联是目前技术最成熟,并且具有高度靶向性的技术。Arrowhead是这一领域的绝对先行者。

5.2 Arrowhead的肺部管线布局
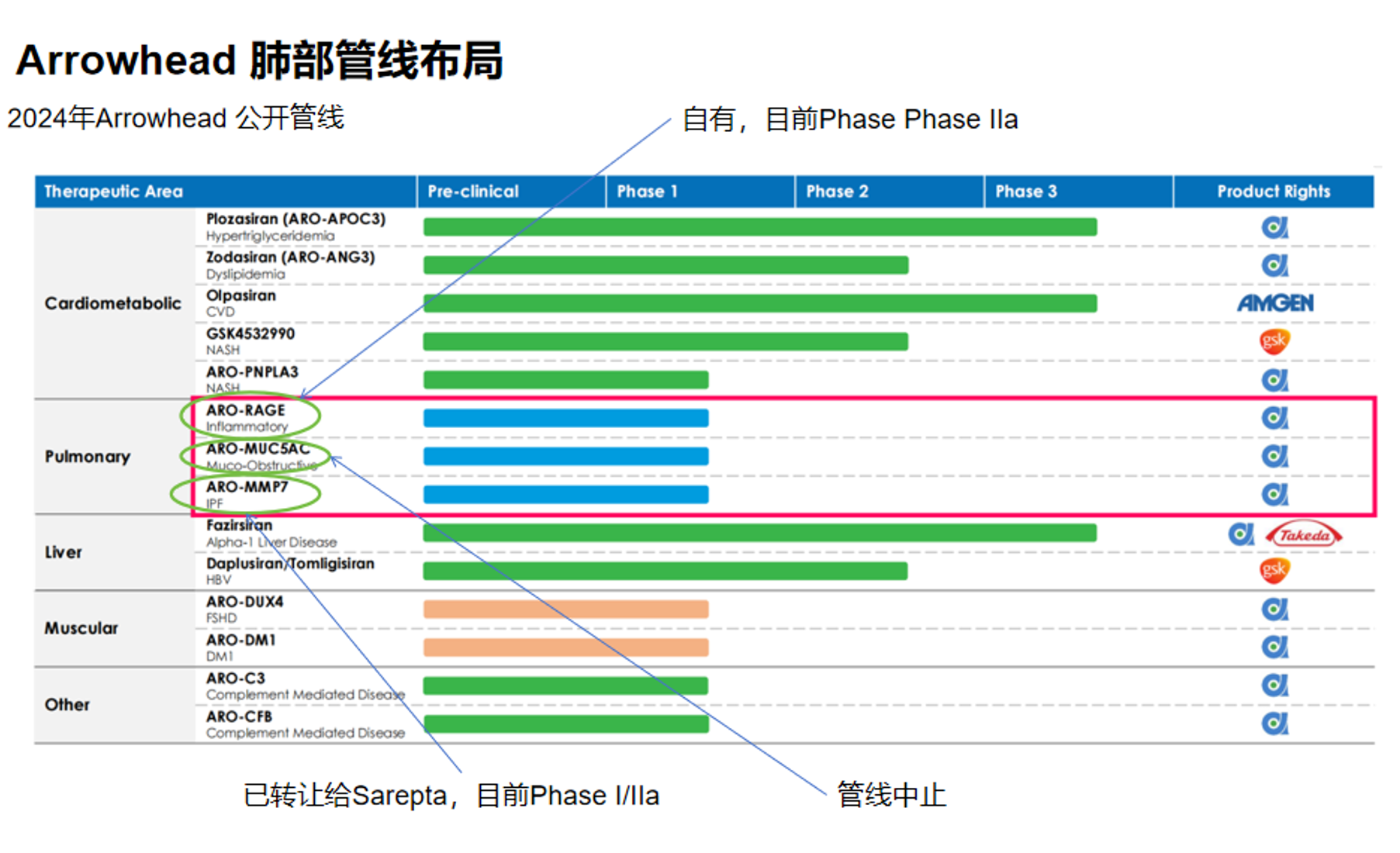
Arrowhead作为小核酸肝外递送的先驱探索者,在肺部递送领域也早早布局,并且在管线方面做出了重大的改变。对比2024年与2026年的公司官方肺部管线布局,可以看到重大差异。下图展示了2024年Arrowhead的公开管线和不同管线的当前状态。其中,ARO-RAGE为Arrowhead的自有管线,是目前Arrowhead自身推动的唯一管线;ARO-MMP7则转让给Sarepta来推进后续的临床试验;而ARO-MUC5AC则已经被终止。这三条管线在肺部递送方面都使用了相同的靶点,即αvβ6整合素。
5.3 Arrowhead的αvβ6整合素配体设计
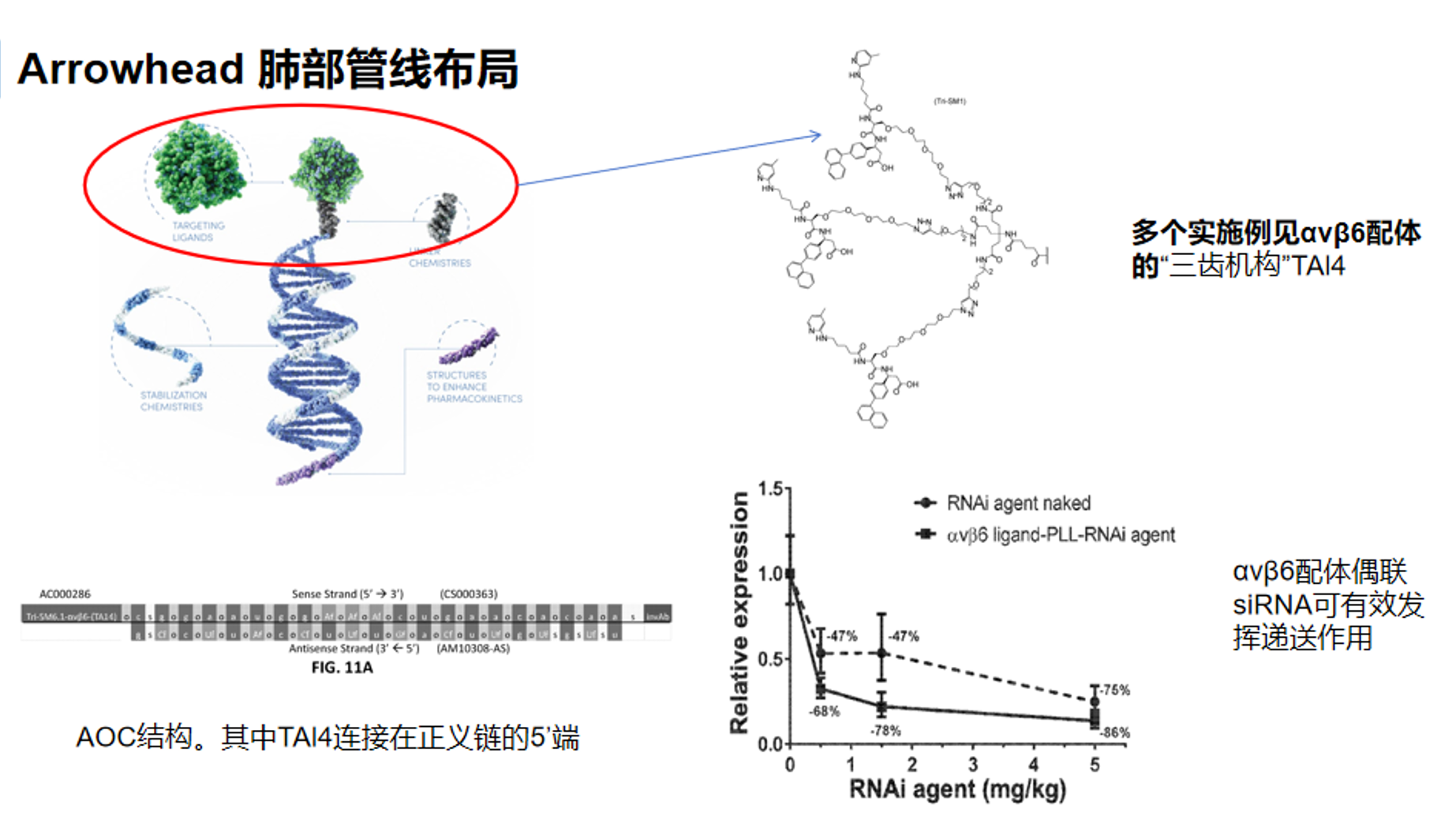
Arrowhead的αvβ6配体,本质上是其肺部RNAi递送体系中的上皮细胞靶向配体。它不是治疗靶点本身,而是接在siRNA分子上的“递送头部”,目的是识别 αvβ6 integrin,从而促进 RNAi trigger 被肺上皮细胞摄取。Arrowhead 早期ARO-ENaC的资料显示,αvβ6 配体可促进上皮细胞对偶联 RNAi 分子的内吞和功能性递送,并在吸入给药后带来更深、更一致的肺部基因敲低。目前披露较多的是一种三齿/三价αvβ6 配体,该配体被用于连接在siRNA的正义链 5' 端。
5.4 TRiM Pulmonary platform可递送入肺深处,到达RAGE广泛表达的区域
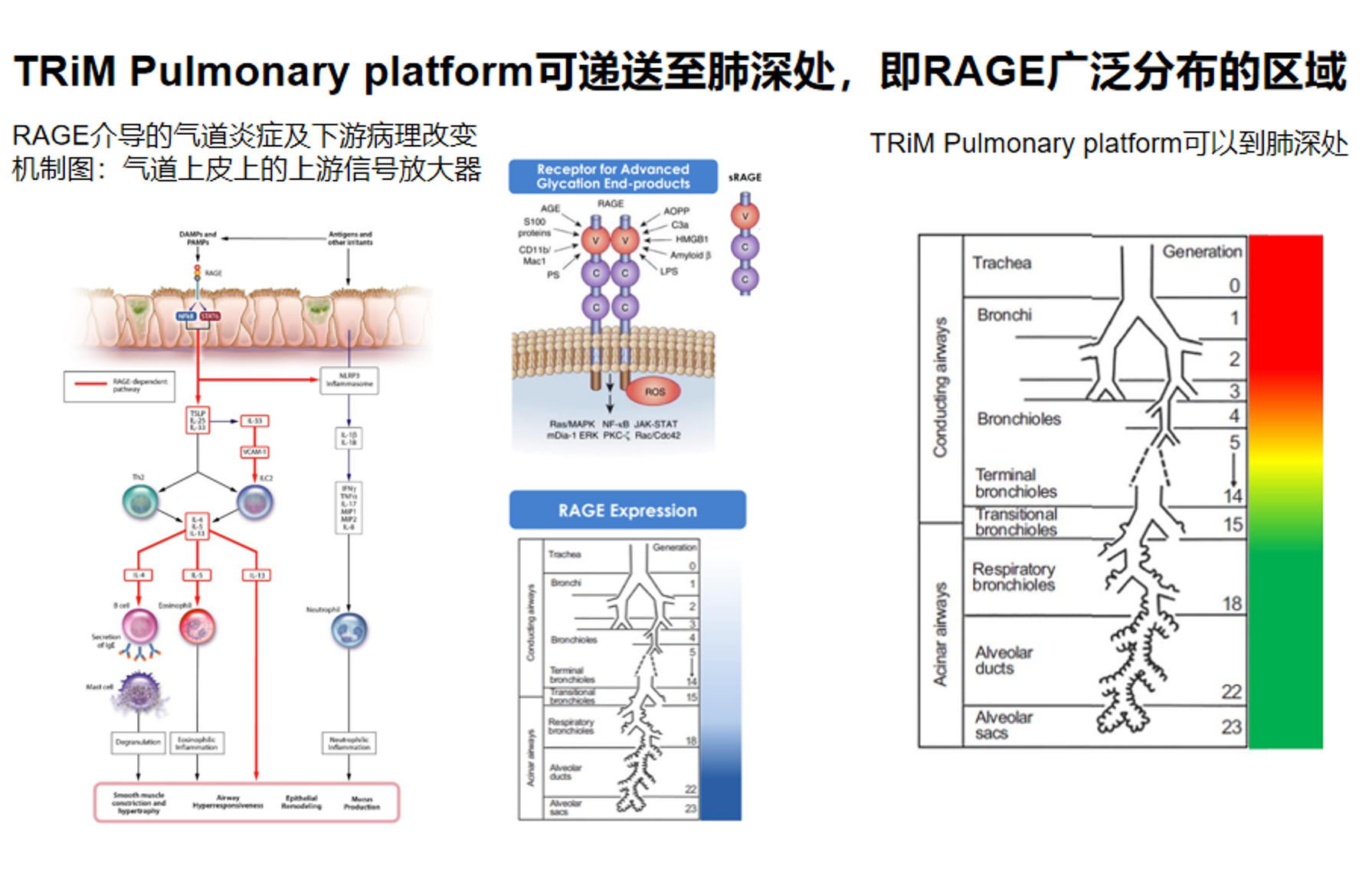
公开资料支持,Arrowhead 的 TRiM Pulmonary platform 并非只停留在近端气道,而是能够把 RNAi 药物有效递送至肺上皮,并覆盖更深部的肺部区域。 其临床数据显示,药效不仅体现在血清,还体现在 BALF(支气管肺泡灌洗液) 中出现剂量依赖性的 sRAGE 下降;BALF 读出本身就提示药物已经到达并作用于更靠近远端气道/肺泡相关区域,而不只是停留在大气道表面。Arrowhead 也据此将其描述为能够在肺内实现“深度和持久的基因沉默”。结合 RAGE 在肺深部,尤其肺泡上皮相关区域的广泛表达背景,这些结果整体支持 TRiM Pulmonary platform 具备进入肺深处并在相应上皮区域产生功能性药效的能力。
5.5 ARO-RAGE的临床前结果
ARO-RAGE 的临床前结果主要说明,其不仅能在肺部实现较深且持久的 RAGE 沉默,还能在多种炎症/损伤模型中降低肺部炎症反应,尤其对中性粒细胞相关炎症轴有明显抑制作用。
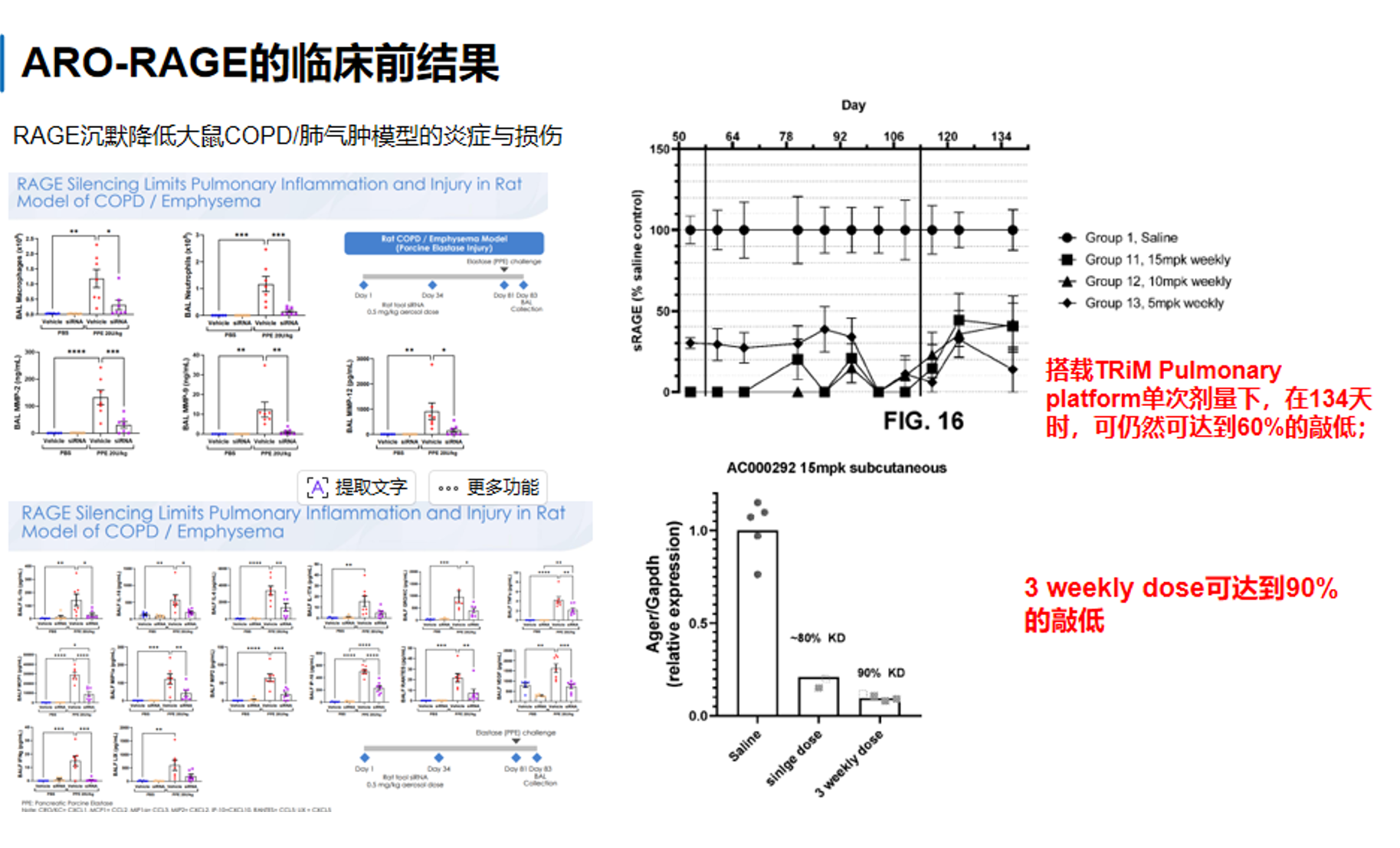
下方第一张图显示,在COPD/肺气肿相关模型中,RAGE沉默能够减轻肺部炎症和组织损伤。左侧多组柱状图整体提示,给药后多个炎症或损伤相关指标较对照组下降,说明RAGE作为上游炎症放大节点被抑制后,肺部病理反应被削弱。右上角时间曲线进一步提示,采用TRiM Pulmonary platform递送后,在110天左右时仍然能维持sRAGE近90%的敲低;右下角则显示,经过 3 次每周给药后,Ager表达可出现接近90%的敲低。整体上,这张图支持 ARO-RAGE 在肺部具有较强、较深且较持久的靶点沉默能力,并且这种沉默可转化为对 COPD/肺气肿样炎症和损伤的改善。
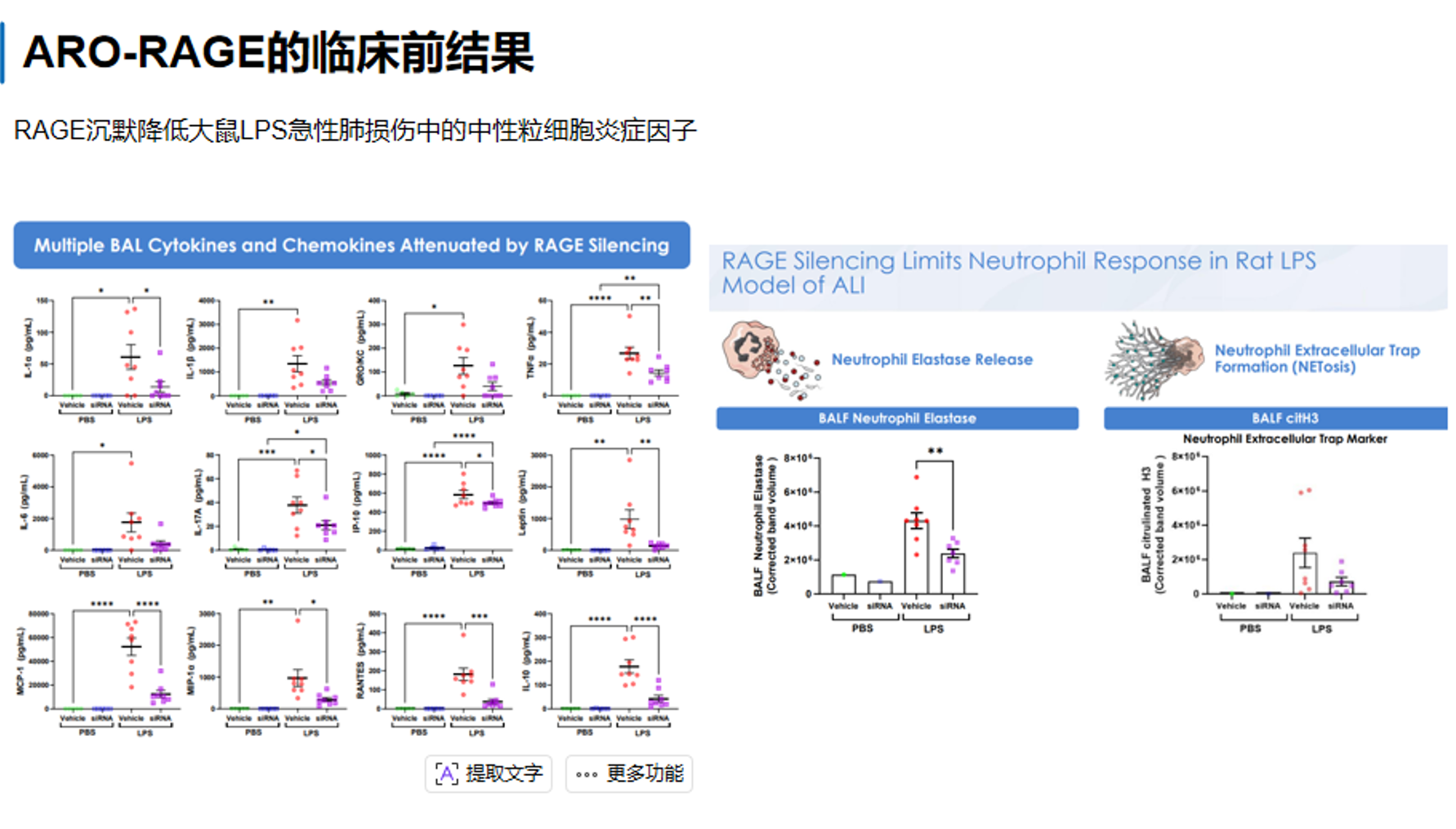
第二张图进一步把重点放在 LPS 急性肺损伤(ALI)模型下的炎症抑制效果。左侧一系列图显示,在BAL液中,多种细胞因子和趋化因子在RAGE沉默后整体下降,说明药物对炎症网络具有较广泛的抑制作用,而不是只影响单一分子。右侧两张图则更聚焦于中性粒细胞反应:一方面,BAL中的中性粒细胞弹性蛋白酶水平下降;另一方面,代表中性粒细胞胞外陷阱形成的NETosis标志物也下降。这说明 ARO-RAGE 不仅降低一般性炎症因子释放,还可能抑制中性粒细胞募集、活化及其介导的继发性组织损伤。
综合这两张图,ARO-RAGE的临床前结果说明该药物能够在肺部实现高效而持久的RAGE敲低,并在COPD/肺气肿及急性肺损伤模型中降低多种炎症介质和中性粒细胞相关损伤信号,从而显示出较强的抗炎和肺保护潜力。
5.6 ARO-RAGE的Ⅰ期临床结果
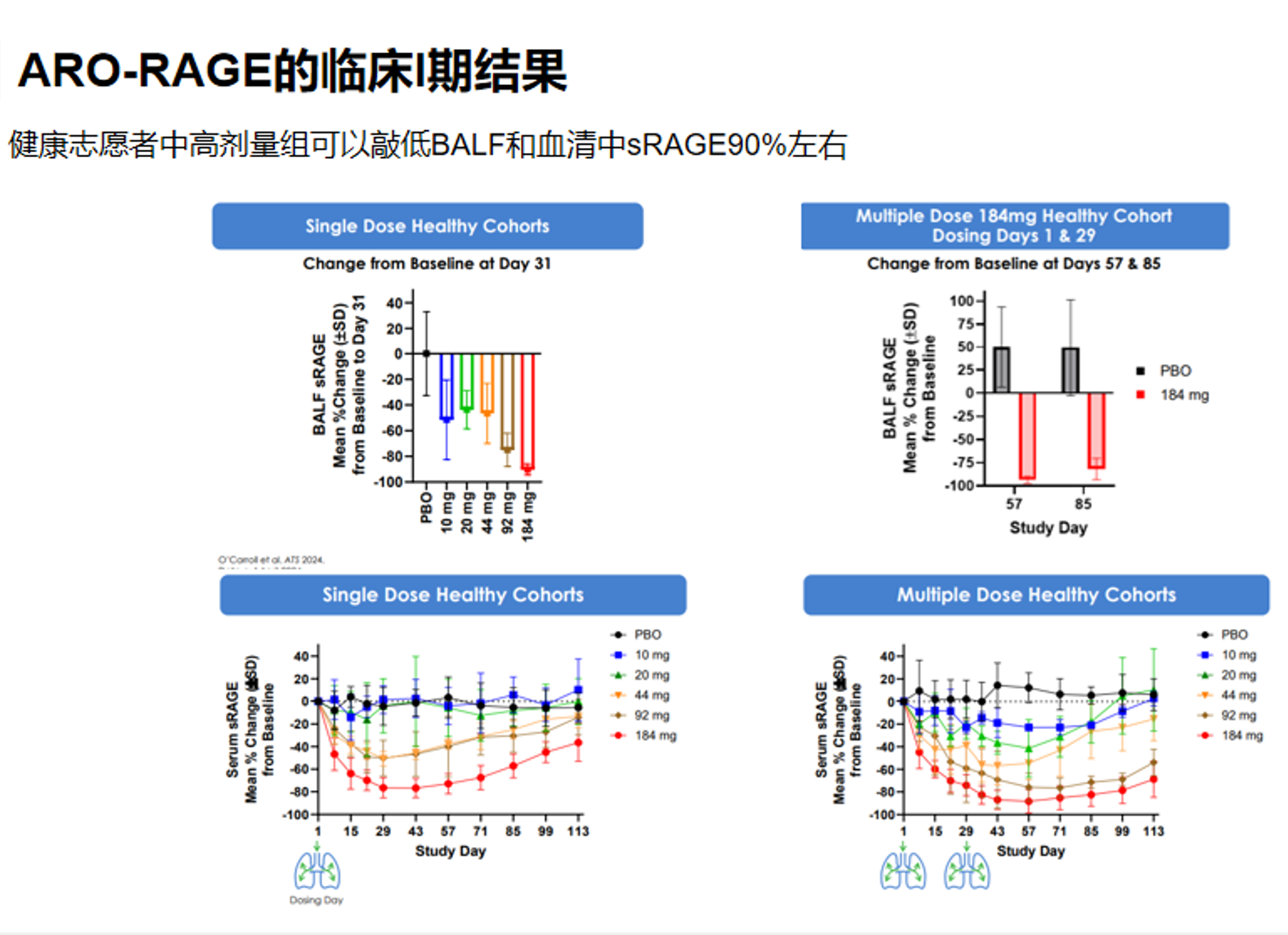
ARO-RAGE 已经显示出较明确的人体靶点敲低证据,而且这种药效同时出现在肺部局部和外周可检测层面。在健康志愿者中,单次或多次吸入给药后,血清 sRAGE 呈现清晰的剂量依赖性下降;高剂量组的降幅可接近 90%,并能维持较长时间。与此同时,单次吸入 184 mg 后,BALF 中 sRAGE 的平均降幅约 90%,最大可达 95%,这说明药物不仅在血液中有信号,更重要的是已经进入肺部并在局部产生了较深的靶点抑制。
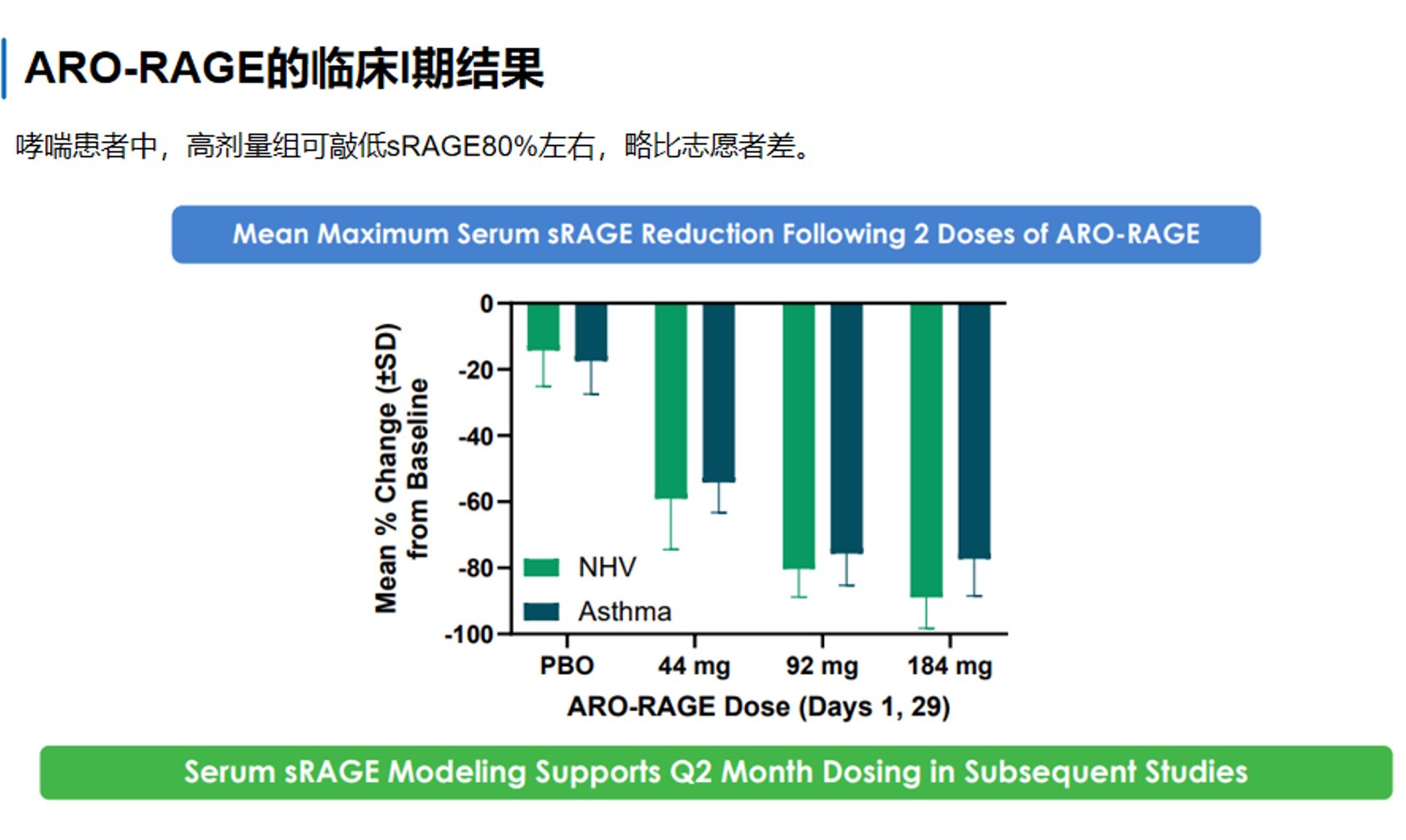
在哮喘患者中,ARO-RAGE 也显示出与健康志愿者相近的趋势。如以下第二张图所示,两次给药后,血清sRAGE在较高剂量下可下降约80%左右;Arrowhead 2024 年更新的数据则进一步披露,在轻中度哮喘患者中,两次给药后 serum sRAGE 最大降幅可达88%,平均最大降幅最高约77%。在相同剂量水平下,健康志愿者与哮喘患者的 sRAGE 降低幅度总体相似。这意味着该药的肺部靶向和靶点engagement 并未因为哮喘相关气道炎症环境而明显失效,支持其向真实患者人群推进。
5.7 MMP7管线中,TRiM平台同样可有效深入MMP7广泛表达的部位
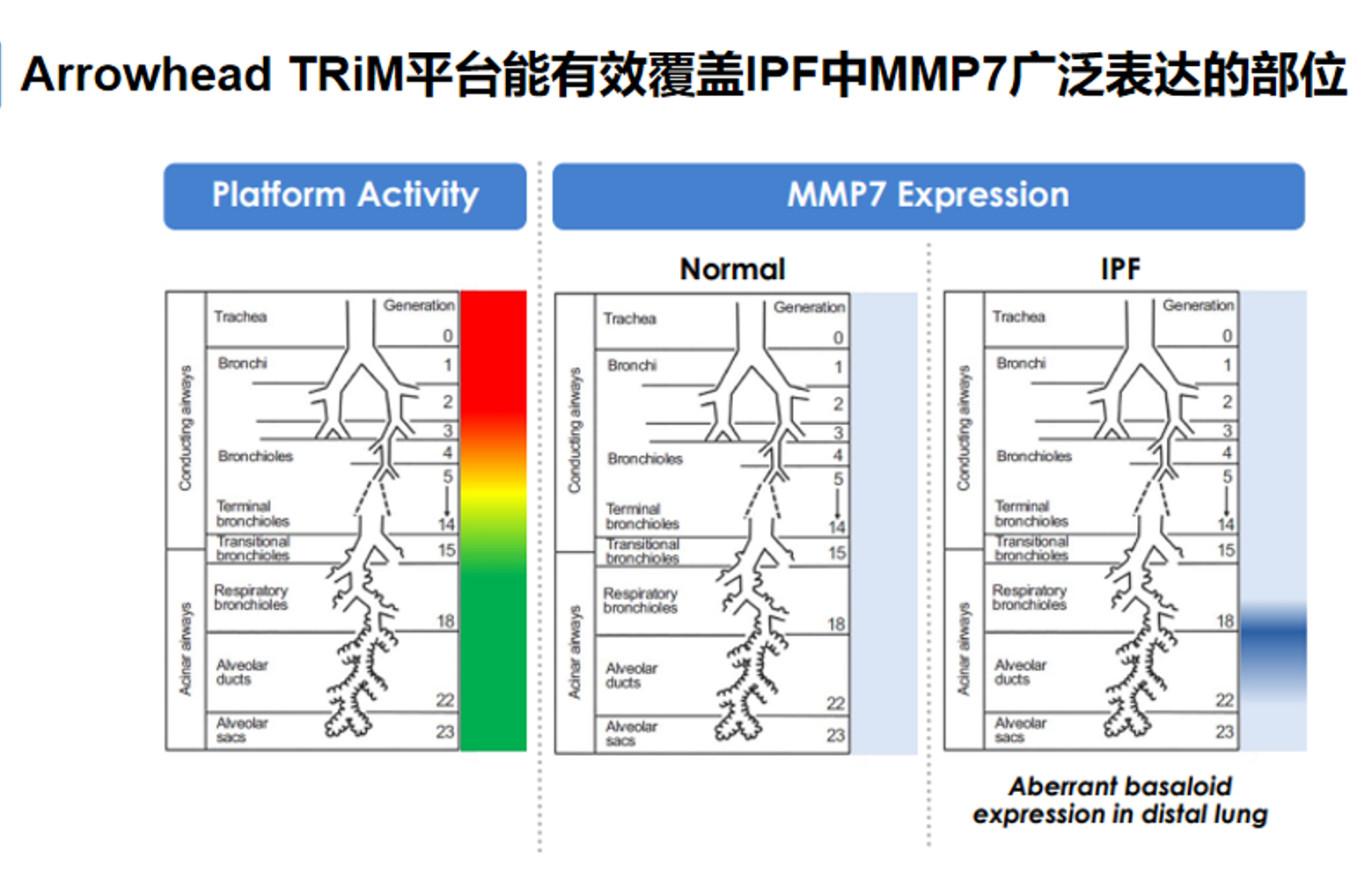
Arrowhead 的 TRiM pulmonary 平台具备到达肺深部的能力,而 MMP7 在 IPF 中又恰好在这些远端肺区存在异常表达,因此两者在空间上是匹配的。 左侧 Platform Activity图显示,该平台的活性并不局限于近端气道,而是能够覆盖从支气管、细支气管一直到呼吸性细支气管、肺泡管和肺泡囊等更深部区域。中间的MMP7 Expression正常肺图提示,MMP7在正常状态下表达有限;而右侧IPF图则显示,MMP7 在特发性肺纤维化中于远端肺部(distal lung)出现异常基底样表达。三图说明该递送平台可有效覆盖IPF中MMP7的病理性表达空间。
5.8 ARO-MMP7的临床前结果
ARO-MMP7 的临床前结果说明:该药能在肺部有效敲低MMP7,并在纤维化模型中同时改善分子标志物、肺功能和生存结局,且这种药效已在NHP中获得一定跨物种支持。
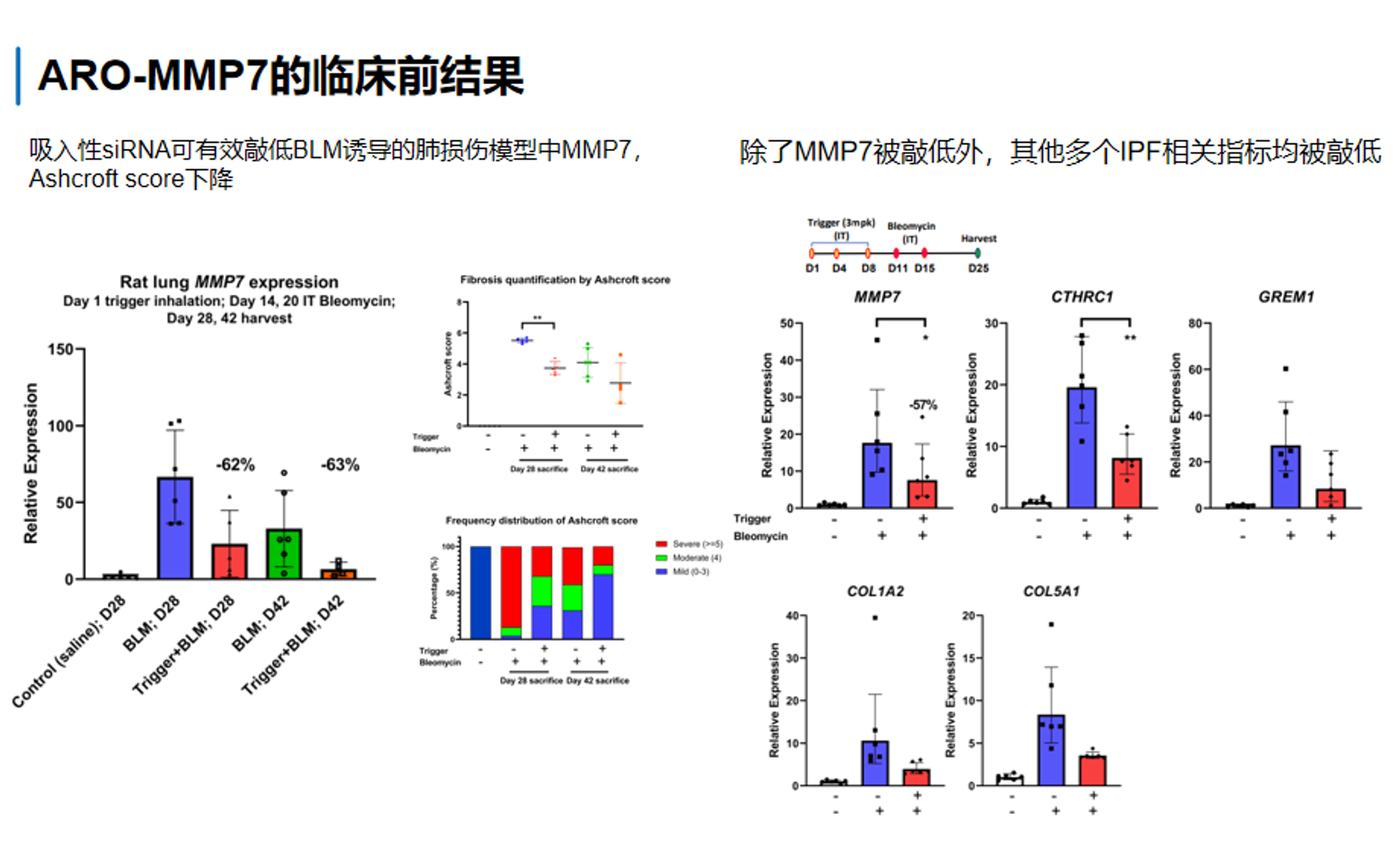
首先,从靶点敲低和疾病相关分子readout来看,ARO-MMP7在博来霉素(BLM)诱导的肺纤维化模型中表现出明确活性。第一张图左侧显示,吸入给药的MMP7 siRNA可显著降低大鼠肺内MMP7 mRNA水平,在不同实验条件下大约可见 60%左右的下降。右侧进一步显示,除MMP7本身被敲低外,多个与IPF相关的下游纤维化标志物也同步下降,包括Cthrc1、Grem1、Col1a2、Col5a1等,这说明ARO-MMP7的作用并不只是停留在单一靶点层面,而是已向纤维化相关分子网络传导,提示其可能对疾病进程产生更系统的抑制作用。
其次,从组织病理和纤维化严重程度看,ARO-MMP7对博来霉素肺损伤后的纤维化表型具有改善趋势。第一张图中部的Ashcroft score结果提示,治疗组的纤维化评分低于BLM对照组,说明肺组织纤维化程度有所缓解。图中频数分布也支持类似趋势,即高纤维化严重度的组织区域减少、较轻病变区域增加。虽然从图面来看这些差异未必在所有指标上都极端显著,但整体方向是一致的,即 MMP7 沉默伴随着纤维化组织学改善。
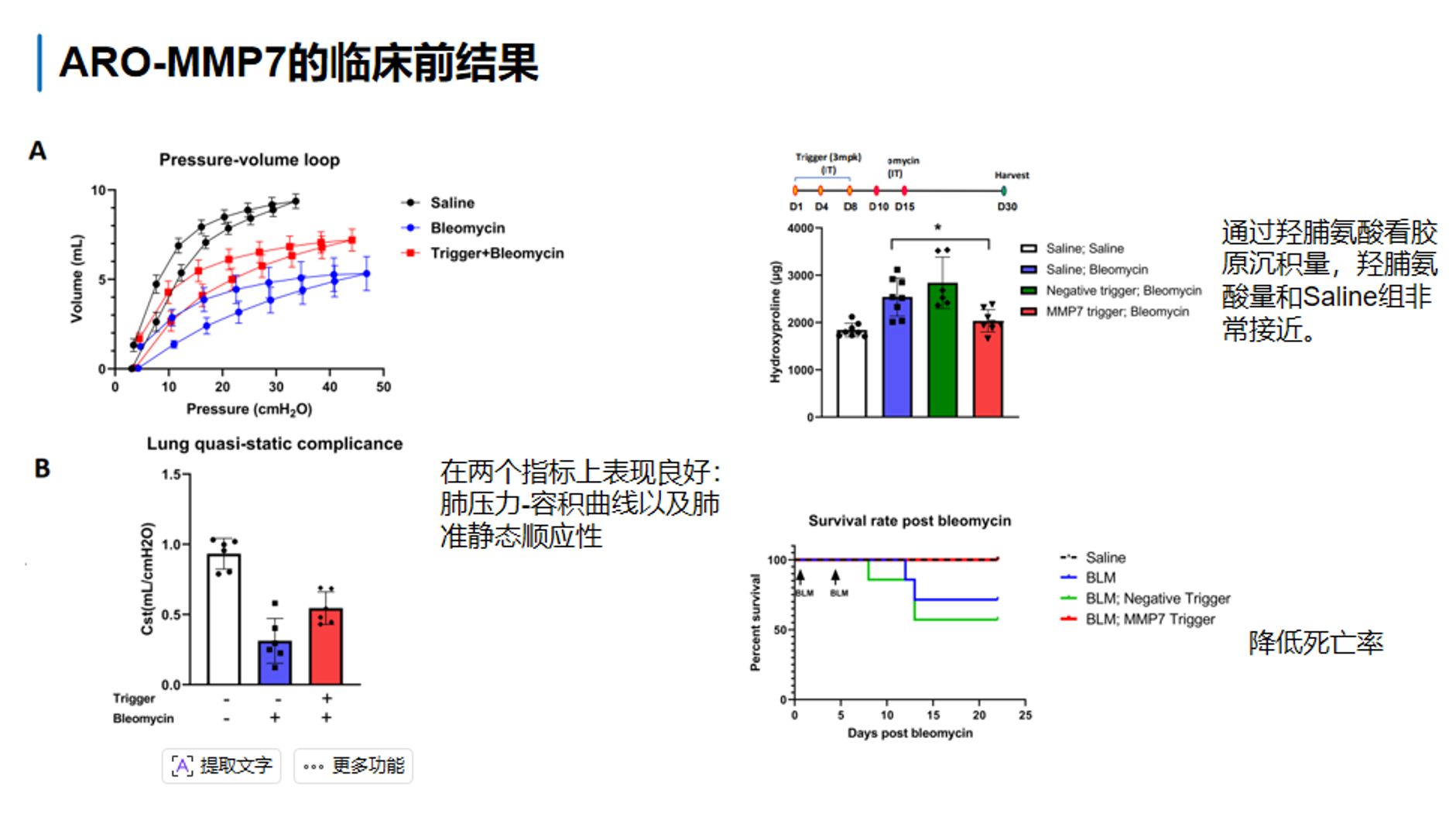
第三,从功能终点看,第二张图提示 ARO-MMP7 不仅改善分子和组织学指标,也改善肺力学表现。压力-容积曲线显示,MMP7 trigger组整体向saline组靠近,而与单纯BLM组相比明显改善,说明肺顺应性和肺扩张能力得到一定恢复。左下角的lung quasi-static compliance也体现出同样方向:BLM使肺顺应性下降,而MMP7 siRNA可部分逆转这一变化。右上角的羟脯氨酸结果则提示胶原沉积水平下降,说明抗纤维化效应具有一定生化基础。右下角生存曲线进一步表明,治疗组在博来霉素损伤后死亡率下降、存活趋势改善,这使得ARO-MMP7 的药效不只是看起来有分子变化,而是对疾病严重结局也可能产生积极影响。
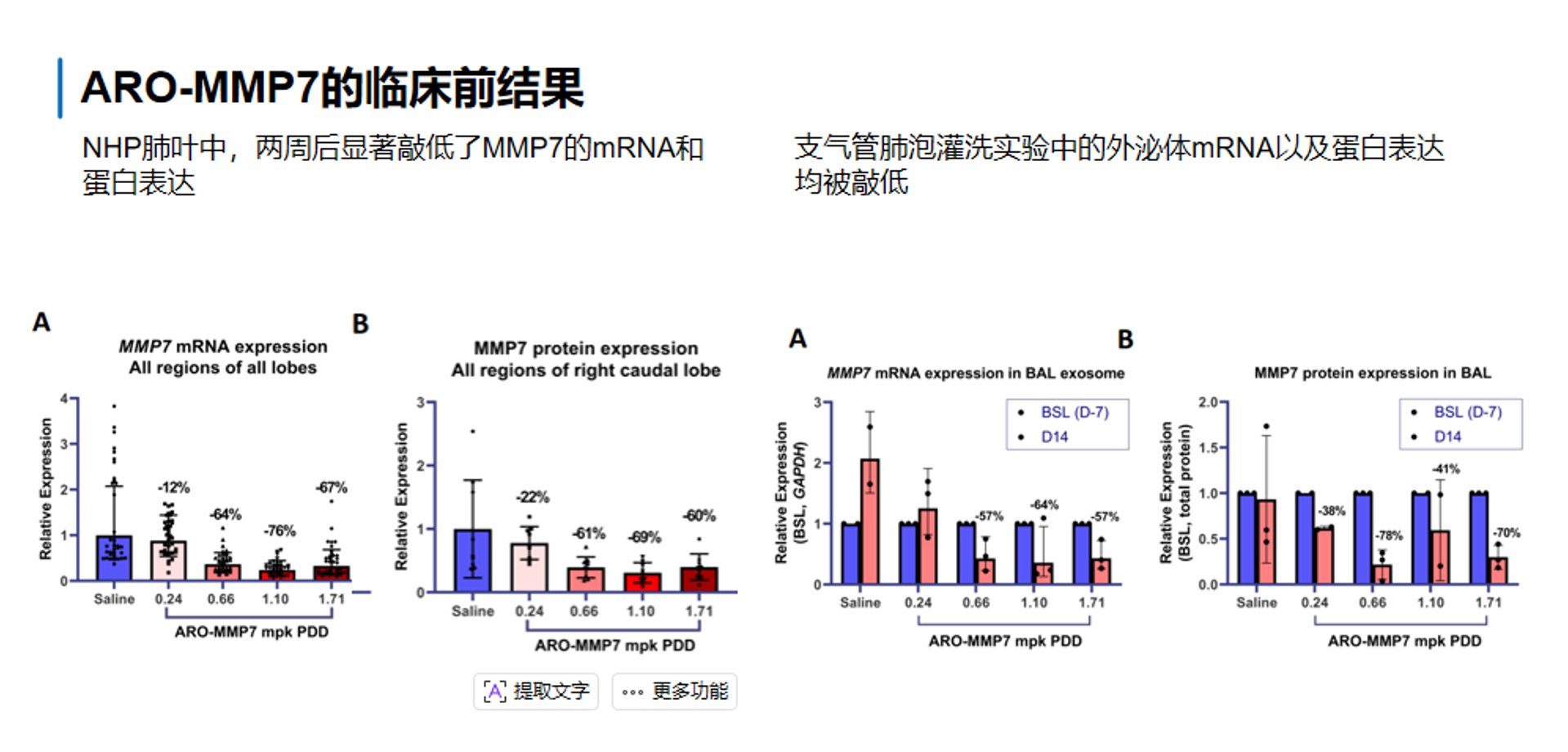
第四,第三张图提供了NHP肺部递送和药效验证。在NHP肺部内,给药两周后,所有肺叶中的MMP7 mRNA和蛋白表达均出现下降。与此同时,在BAL中,无论是分泌性的 MMP7 mRNA 还是 MMP7 蛋白,也均显示下降趋势,说明药物不仅进入肺组织,而且在肺局部可检测环境中也形成了功能性药效信号。
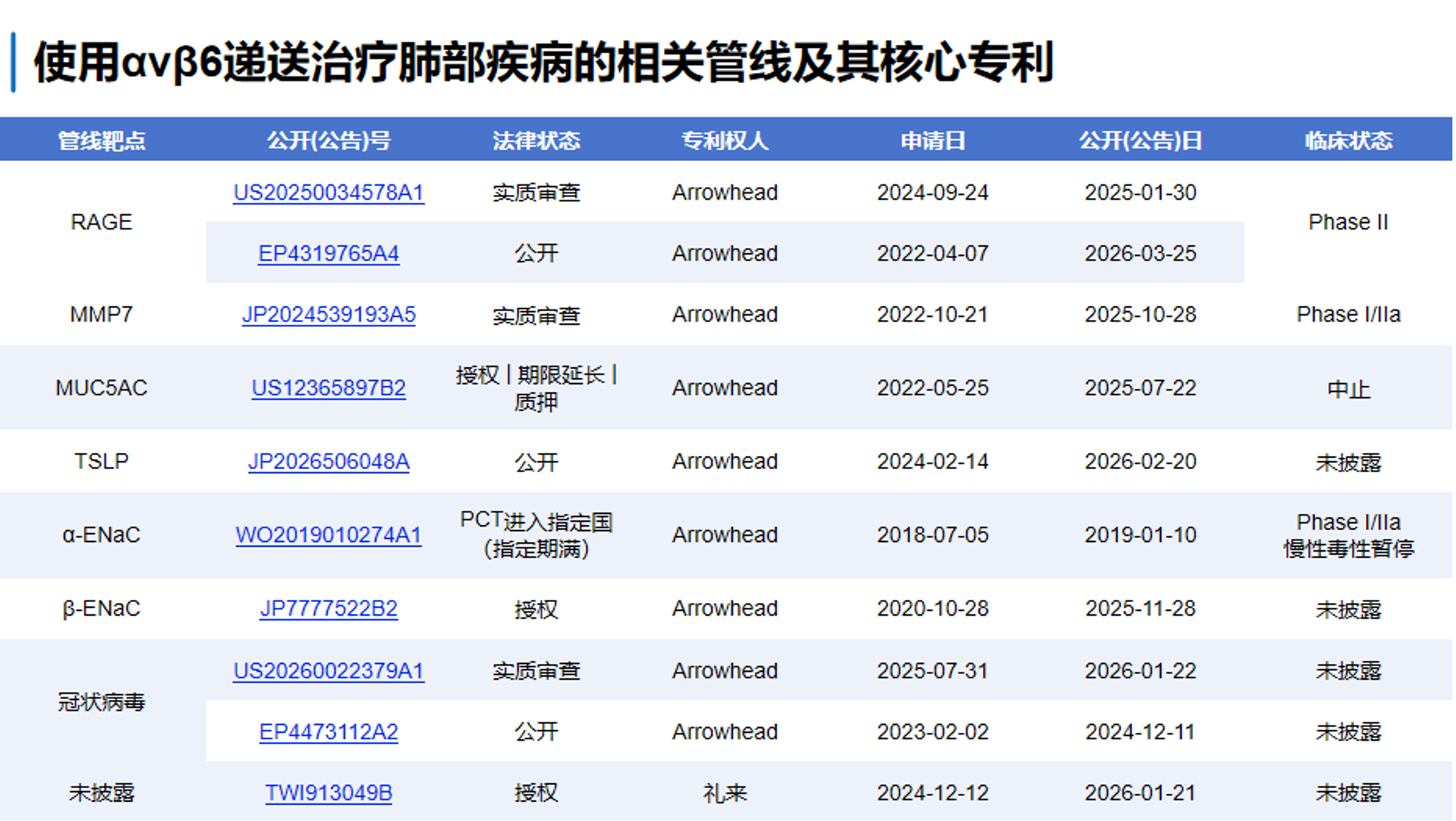
5.9 目前靶向αvβ6整合素治疗肺部疾病的相关管线和核心专利
鉴于Arrowhead在αvβ6整合素治疗肺部疾病的系统性布局,濠麦科技总结了αvβ6整合素治疗肺部疾病的相关专利。Arrowhead在这方面走了相当长的一段路:2018年开始α-ENac,2020年的β-ENaC,两个ENaC相关管线后续均未继续推进;2022年前后开始做RAGE、MMP7以及MUC5AC,其中RAGE和MMP7得以继续推进;近些年,TSLP和针对冠状病毒的专利相继公开,说明Arrowhead在肺部递送的坚实信心。目前,Arrowhead在肺部递送siRNA领域处于绝对的全面领先,在前期失败的基础上,现在已广泛铺开管线开展临床前与临床研究。值得注意的是,礼来也在2026年初公布了基于αvβ6整合素的相关专利,这也说明了这一靶点在肺部递送领域的地位。
六、皮肤递送:实现高靶向分子治疗
6.1 皮肤递送的独特挑战与技术路线
siRNA在皮肤领域具有较广的应用潜力,适应症可涉及纤维化与瘢痕、色素异常、局部感染、皮肤肿瘤以及与毛囊相关的疾病等,例如银屑病、特应性皮炎、瘢痕疙瘩、病理性色沉、皮肤鳞状细胞癌及脱发等,核心逻辑是利用 RNA 干扰在局部组织中沉默致病基因,从而实现较高靶向性的分子治疗。与其他器官相比,皮肤递送需要特别关注几类连续屏障:首先是角质层这一最强的外部物理屏障,决定了siRNA很难通过普通外用方式自由进入;其次是表皮和真皮内的致密组织结构与细胞外基质,限制其在组织中的进一步扩散;再次是皮肤局部复杂的细胞组成,使“进入皮肤”不等于“进入正确靶细胞”;此外,siRNA还面临局部核酸酶降解、细胞膜摄取不足以及进入细胞后内体逃逸效率低等共性难题,同时还必须控制局部刺激性和炎症反应,以保证耐受性。
当前皮肤siRNA递送通常通过几条路径来解决:一类是使用脂质体、聚合物纳米颗粒、凝胶、微乳、外泌体等载体,对siRNA进行包载和保护,并增强局部滞留与细胞摄取;一类是通过脂肪酸、胆固醇、细胞穿透肽或受体靶向配体等化学偶联,提高其与皮肤细胞膜或特定细胞的相互作用。
目前,新加坡National Skin Centre的SPARC相关管线治疗术后瘢痕和韩国公司Lemonex的CTGF相关管线治疗增生性瘢痕已披露临床Ⅰ期结果,接下来将针对这两个案例进行分析。

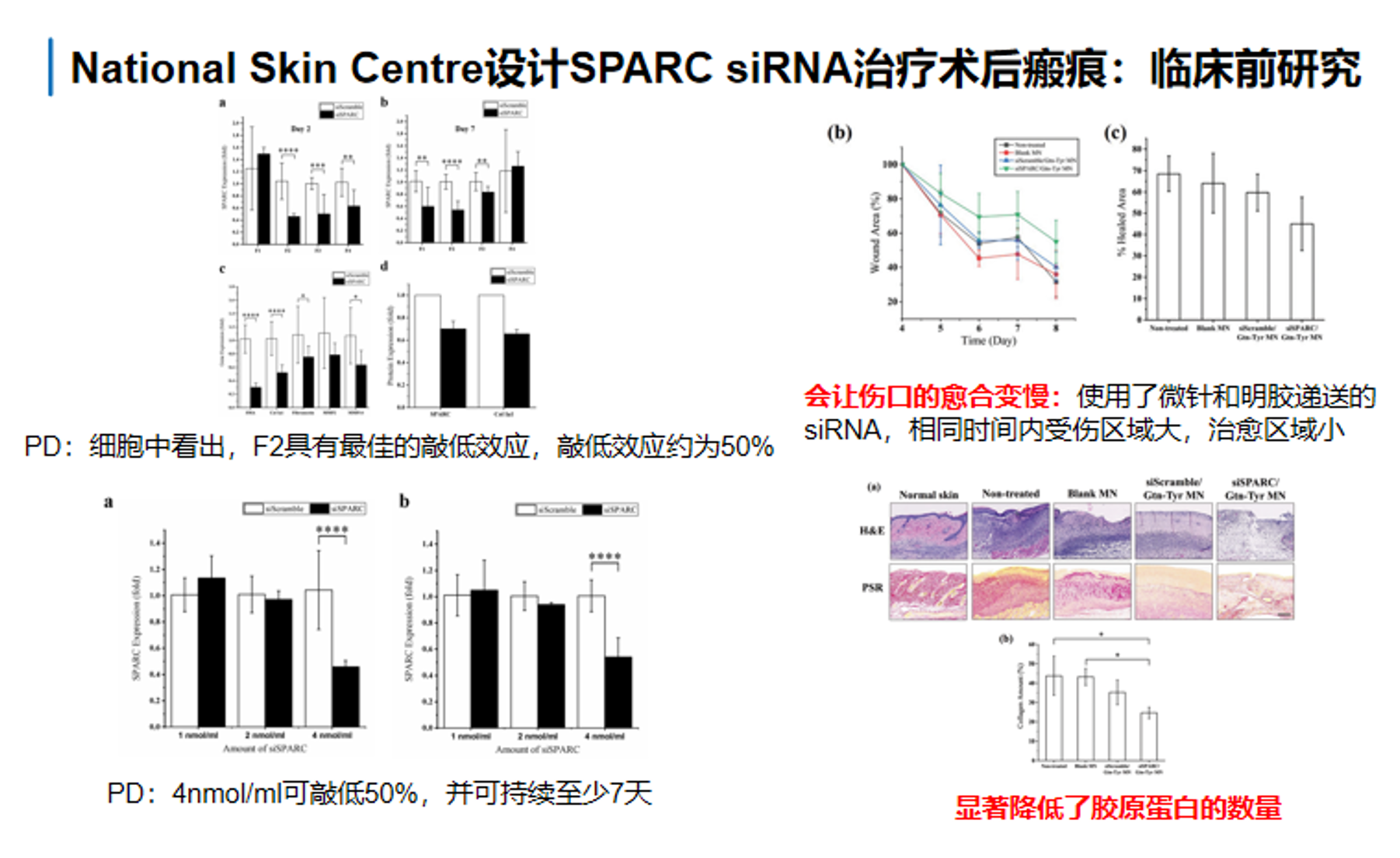
6.2 National Skin Centre特有的纳米复合物设计
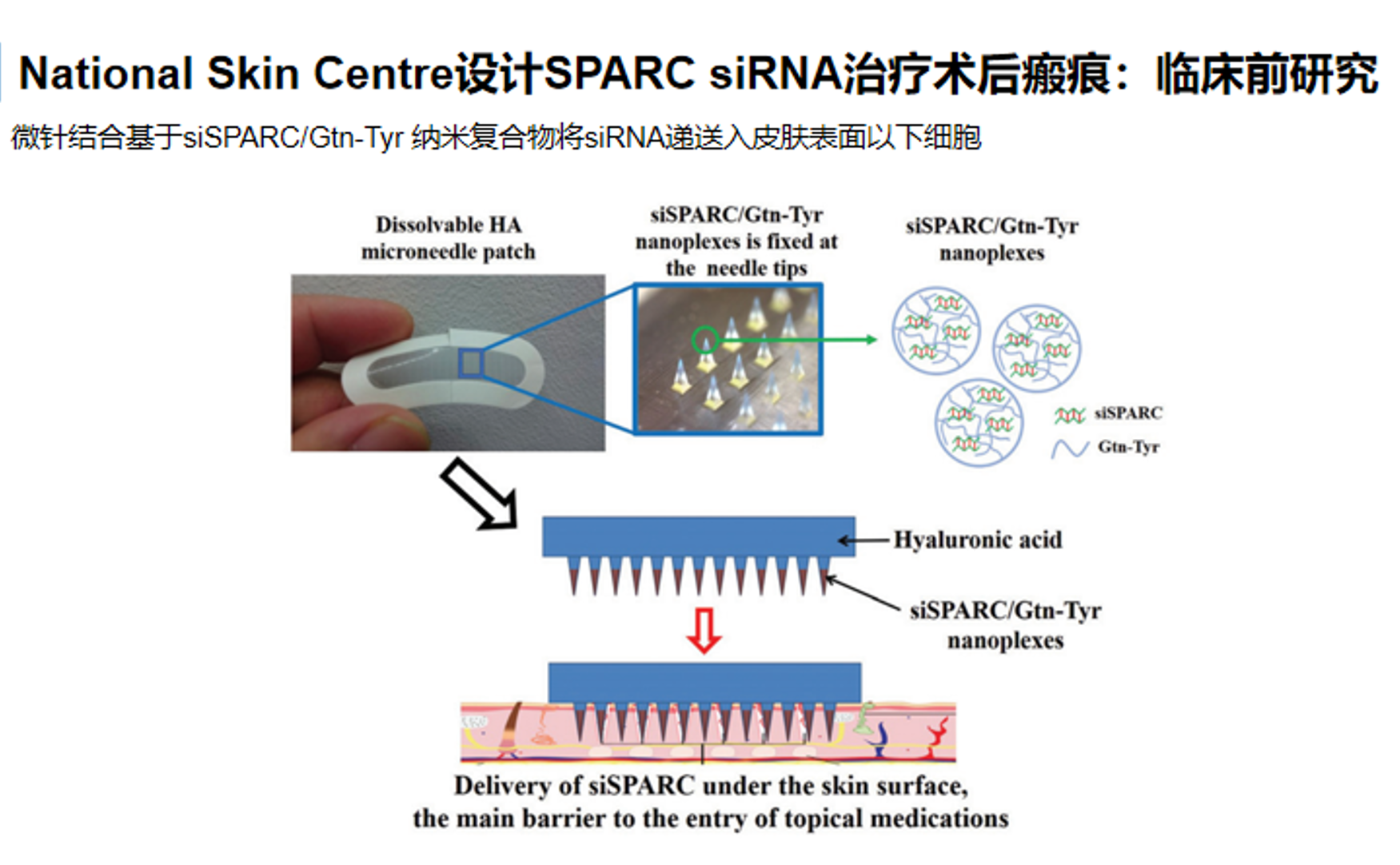
这套纳米复合物设计的核心思路是把siSPARC(靶向SPARC的siRNA)装载进gelatin-tyramine(Gtn-Tyr)纳米复合物中,再进一步整合到可溶性透明质酸微针贴片中,经皮将siRNA直接送过角质层,释放到皮下浅层和局部成纤维细胞富集区域。你给的第一张图体现的是它的整体给药逻辑:可溶解性的透明质酸微针先机械性跨越皮肤表面最强的角质层屏障,针尖中的siSPARC/Gtn-Tyr nanoplex随后在皮内释放,从而把siRNA送到传统外用药难以有效到达的部位。
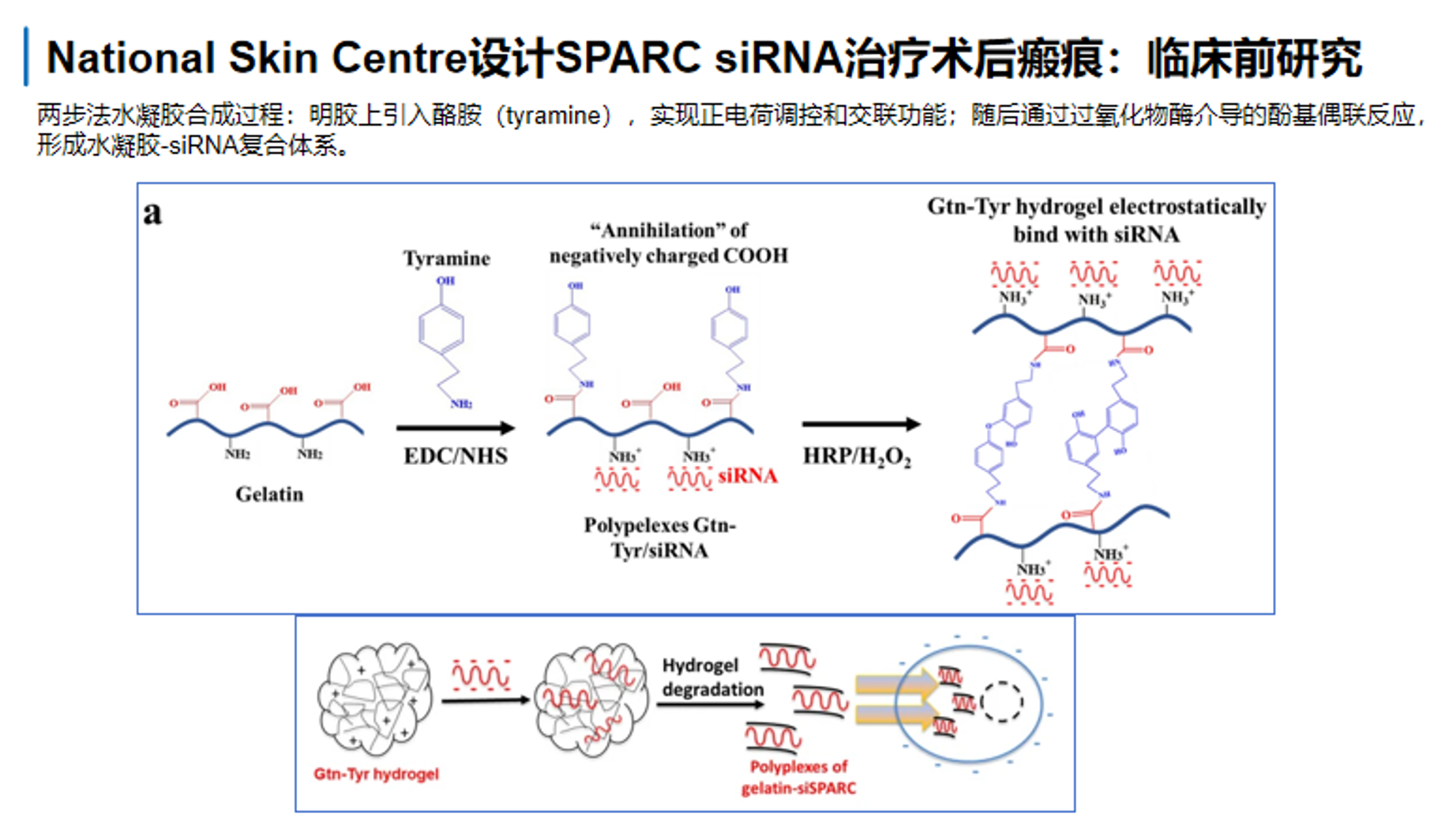
从分子设计上看,这个体系不是简单把siRNA直接装进微针,而是先构建一个带正电、可进一步交联固化的纳米复合物。如下图所示,研究者先通过EDC/NHS 把 tyramine 接到明胶上,形成Gtn-Tyr;这样一方面引入了更多正电/可复合位点,使其能够与带负电的siRNA形成静电复合物,另一方面也提供了后续通过 HRP/H₂O₂催化 tyramine基团氧化偶联、形成水凝胶网络的可能。论文摘要和图示都表明,这样做的目的是把siRNA先稳定包进Gtn-Tyr nanoplex,再借助可降解水凝胶/微针体系实现局部缓释和保护,减少 siRNA 在皮肤局部被快速失活的风险。
6.3 National Skin Centre靶向SPARC的临床前研究结果
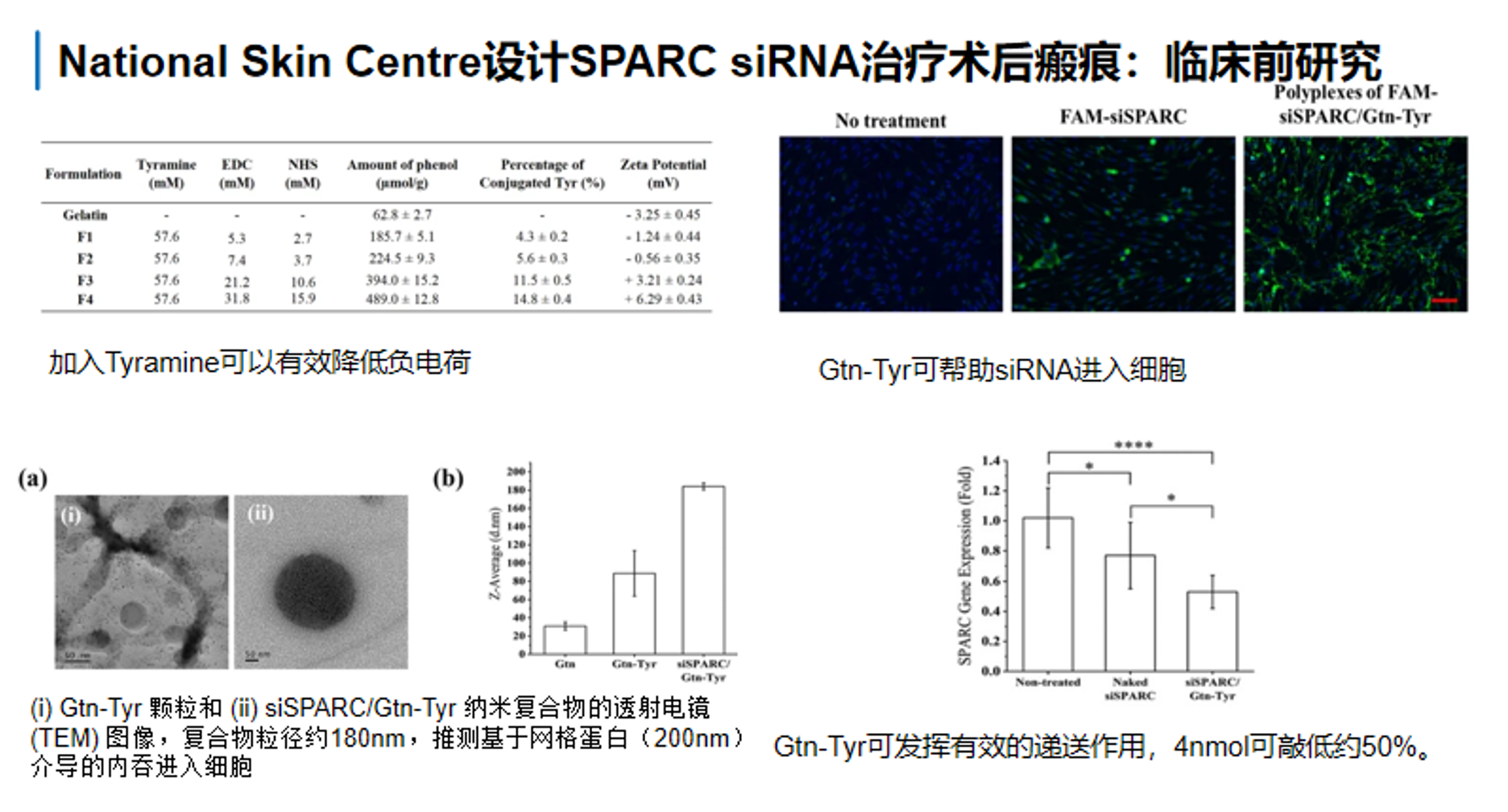
siSPARC/Gtn-Tyr微针体系,目前不仅在材料层面解决了siRNA带负电、难入细胞、难穿皮肤屏障的问题,而且已经在细胞和动物层面证明了其抗瘢痕活性。 其中,加入tyramine后的明胶(Gtn-Tyr)能够提高体系正电性,更容易与带负电的siSPARC形成稳定纳米复合物,并促进细胞摄取;图中绿色荧光结果和SPARC表达下降结果,说明Gtn-Tyr既起到载体保护作用,也起到递送促进作用。
SPARC本身是与纤维化和胶原生成密切相关的基质细胞蛋白,因此在术后瘢痕和病理性瘢痕预防中具有明确靶点意义。这个体系在细胞实验中4 nmol剂量下也能获得50%左右敲低。第二张图显示,在小鼠伤口模型中,siSPARC/Gtn-Tyr-loaded 可溶解性透明质酸微针贴片能够在伤口愈合过程中降低胶原生成,而且未触发明显免疫反应。从组织学上看,图中的H&E、PSR以及胶原相关定量都继续支撑瘢痕组织中的胶原沉积被明显压低这一结论。
6.4 National Skin Centre靶向SPARC的临床结果
Ⅰ期临床试验结果表明,siRNA微针贴片在术后瘢痕控制方面优于传统硅凝胶贴。从三维体积测量看,治疗60天后,siRNA微针侧的瘢痕体积降至8.88,低于硅凝胶贴侧的12.77,提示其在缩小瘢痕体积方面更有效;虽然第30天时差异尚未达到显著性,但到第60天已显示出更明确的优势。与此同时,从瘢痕体积减少百分比来看,siRNA微针组在0~30天和0~60天两个时间段内均优于硅凝胶贴组,其中60天时体积减少比例分别为83.78%和74.11%,且差异具有统计学意义。整体而言,这说明siRNA微针贴片不仅能够加快术后瘢痕缩小,而且其减疤效果在两个月内已明显优于现有常用的硅凝胶贴。

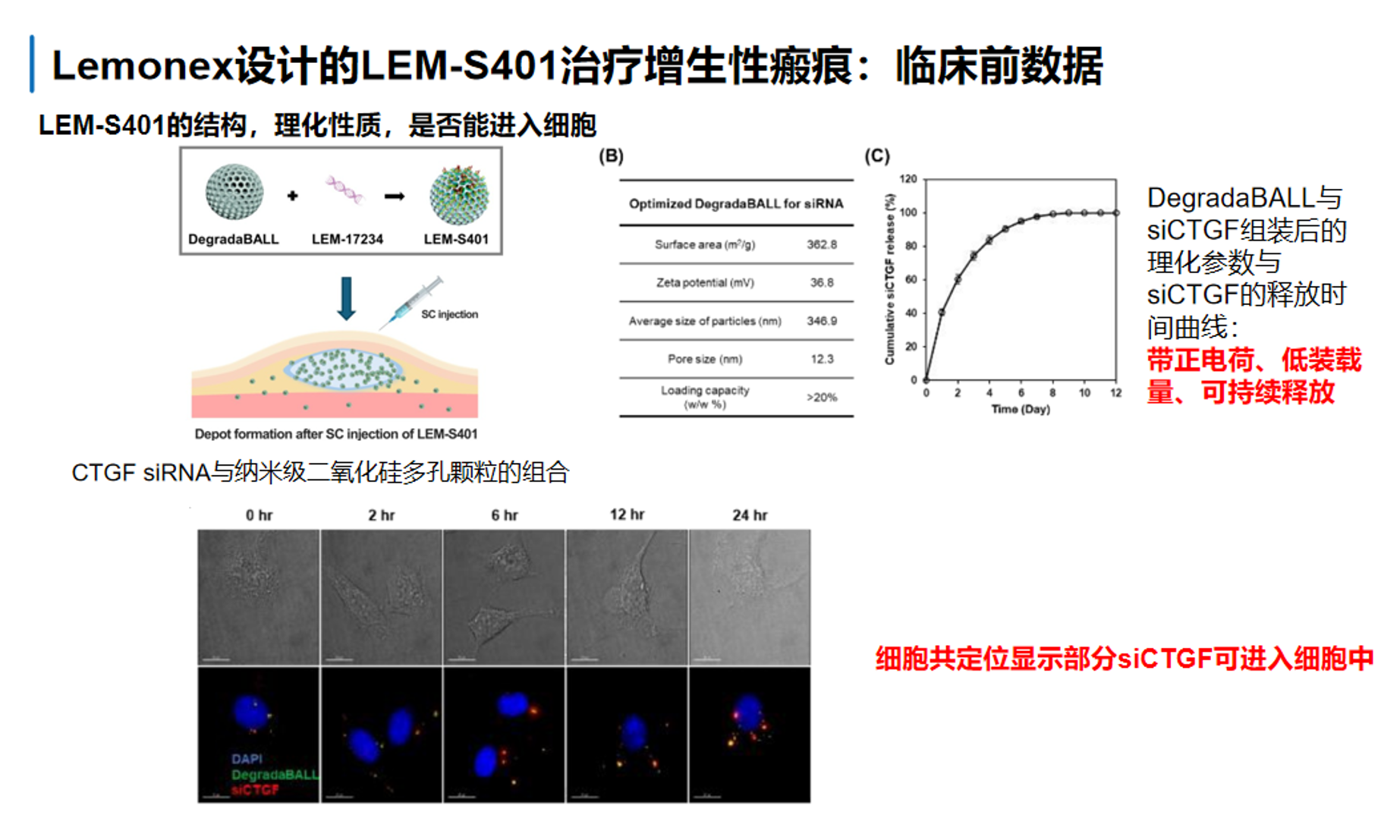
6.5 Lemonex设计的LEM-S401结构信息
LEM-S401是Lemonex开发的一款用于增生性瘢痕/瘢痕疙瘩的局部 RNAi 药物,其核心是把靶向CTGF的siRNA装载到自研的DegradaBALL 多孔纳米载体中,形成可皮下注射的siRNA-纳米复合物。CTGF是瘢痕纤维化中的关键促纤维化因子,参与成纤维细胞活化以及I型、III型胶原等细胞外基质的过度沉积,因此用siRNA下调CTGF,逻辑上是直接切断异常瘢痕形成的重要上游通路。
LEM-S401的设计特点主要体现在三个方面。第一,DegradaBALL负责保护和缓释siCTGF:这类多孔颗粒具有一定表面电荷、可装载 siRNA,并在体外呈现逐步释放曲线,在局部形成一个储库持续释放,从而提高局部暴露时间。第二,它具有一定的细胞进入能力:下方细胞荧光图提示,部分siCTGF可随载体逐步进入细胞内。第三,它适合局部皮下注射到瘢痕/创缘附近,从而避开皮肤角质层屏障,直接把siRNA送到真皮成纤维细胞相关区域。
6.6 LEM-S401的临床前数据
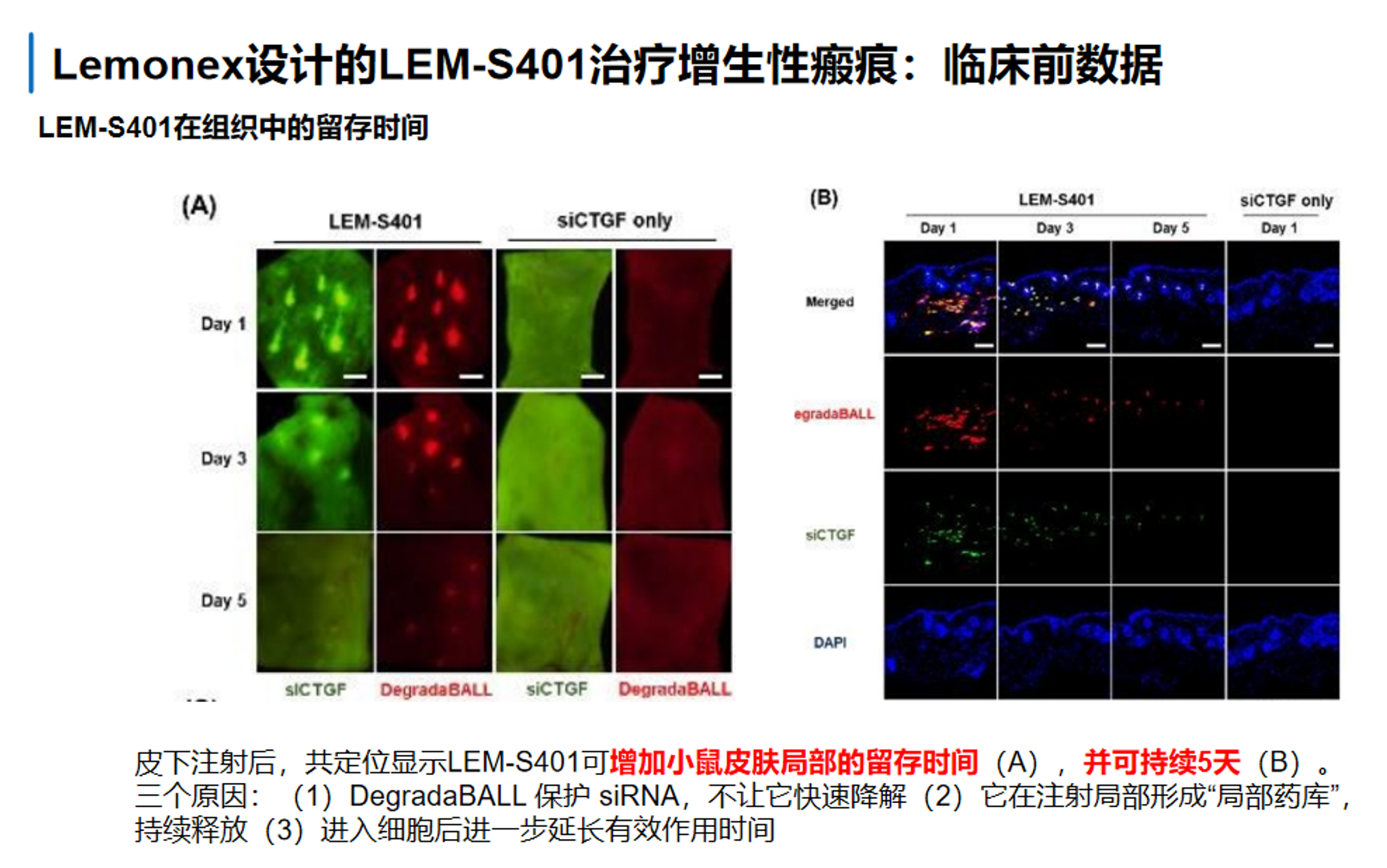
第一组图说明LEM-S401能把siCTGF更久地留在皮肤局部。图中与单独siCTGF 相比,LEM-S401组在注射后第一、三、五天仍能在皮肤组织中看到更明显的信号,说明DegradaBALL载体并不是简单包裹siRNA,而是确实延长了其在局部组织中的停留时间。这个结果很关键,因为局部抗瘢痕治疗如果药物停留太短,往往来不及持续压制纤维化通路;而LEM-S401通过形成局部储库、对siRNA的保护以及进入细胞后继续缓释,提升了局部有效暴露时间。
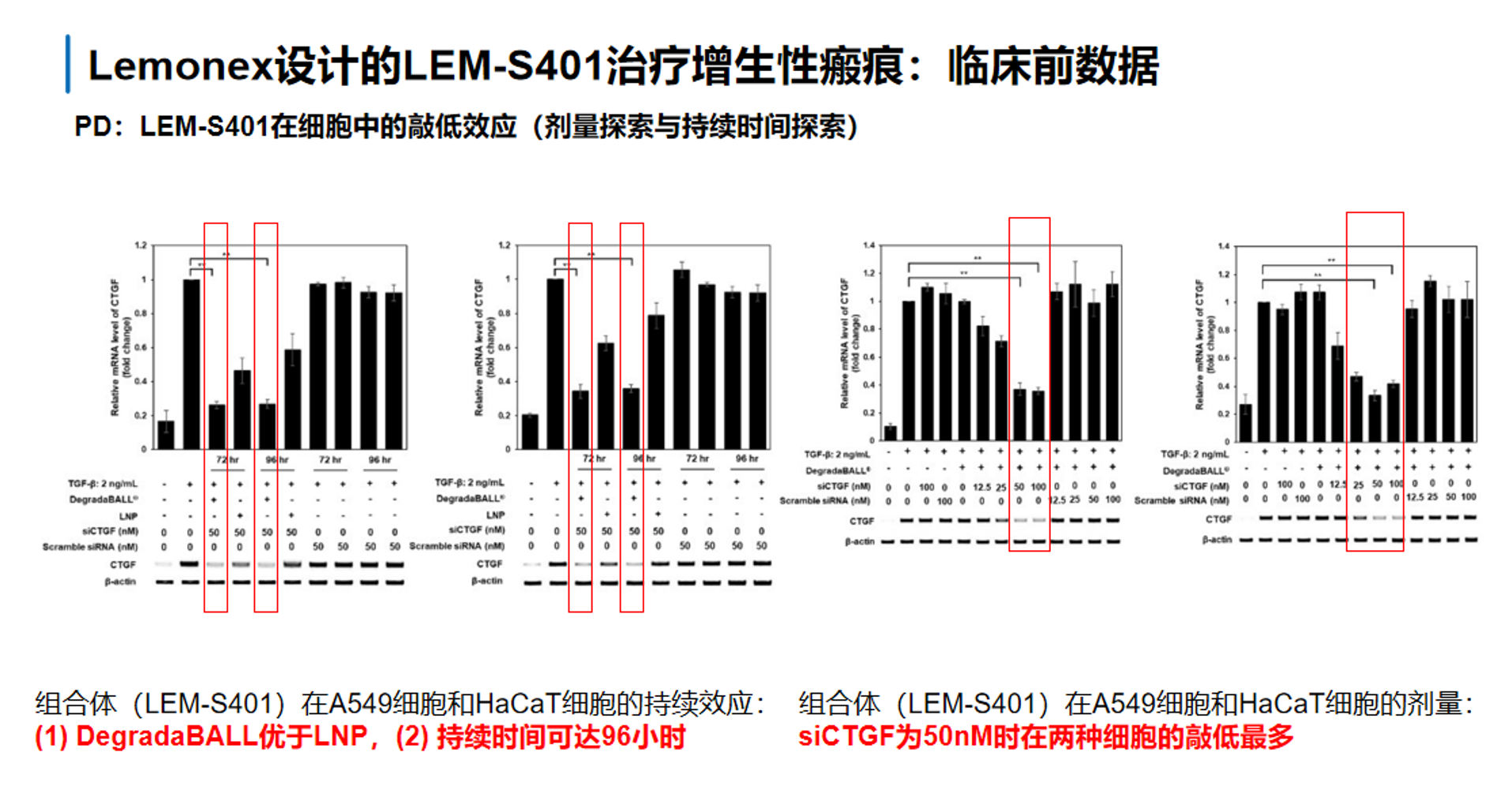
第二组图说明LEM-S401在细胞层面具有更好的敲低效率和持续性。在A549和HaCaT细胞中,LEM-S401相比裸siCTGF或其他对照条件,整体表现出更深、更持久的 CTGF 抑制,图中也强调其持续时间可达96小时。同时,剂量探索结果提示,在这些细胞模型里50 nM siCTGF条件下敲低最明显。
第三组图把这种分子层药效进一步推进到了小鼠皮肤损伤/瘢痕模型。从组织学和qPCR/分子指标看,LEM-S401不仅能降低CTGF mRNA,还连带压低了Collagen I和Collagen III的表达,降幅大约可达80%左右,同时还能降低皮肤厚度,说明它影响的不是单一靶点,而是整个促纤维化输出通路。图中把LEM-S401与siCTGF only做对比也很重要:同样是siCTGF,装入DegradaBALL后效果明显更强,说明真正起作用的关键不只是选对正确靶点,也是这个局部递送体系把药效放大了。
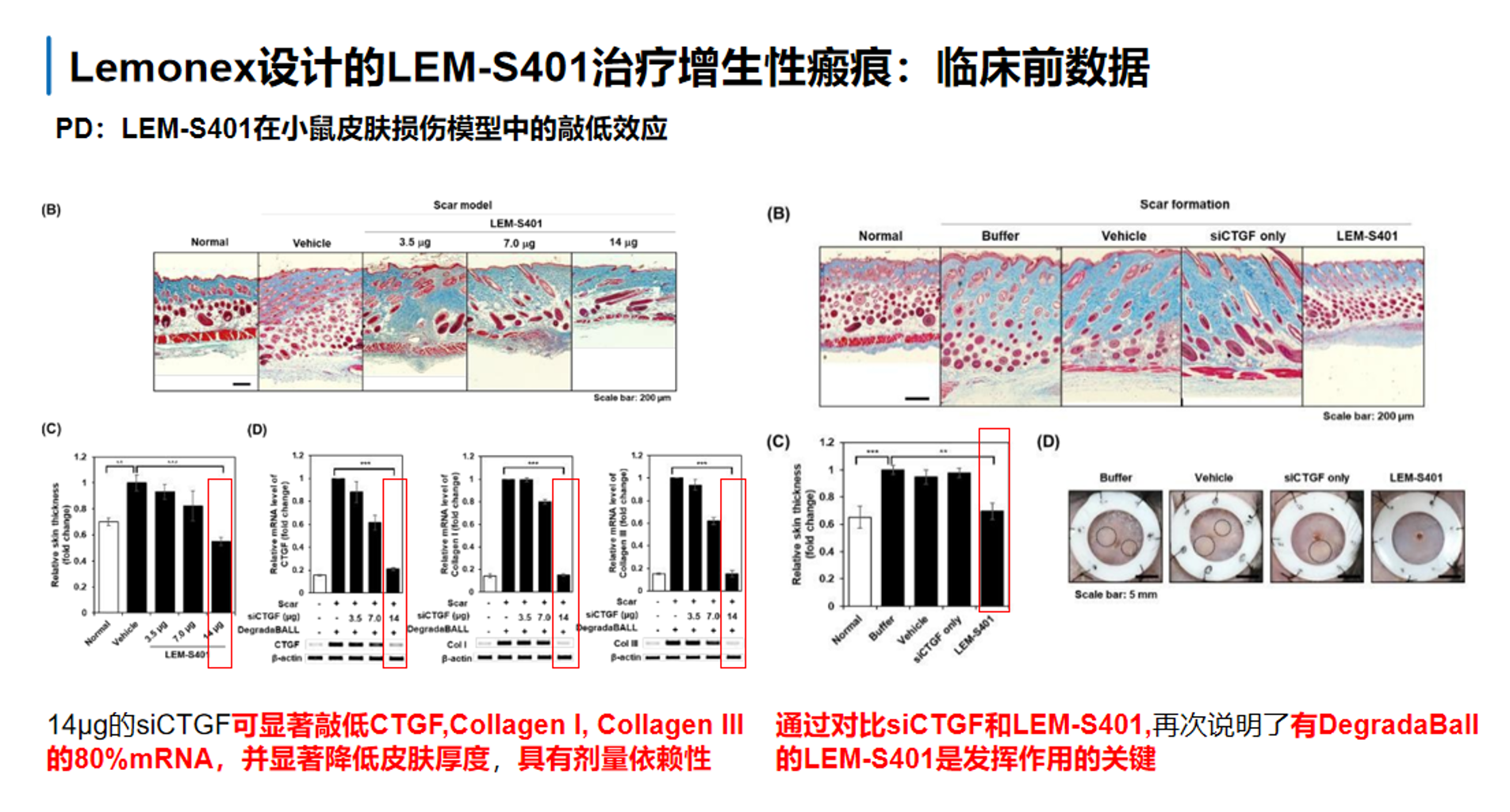
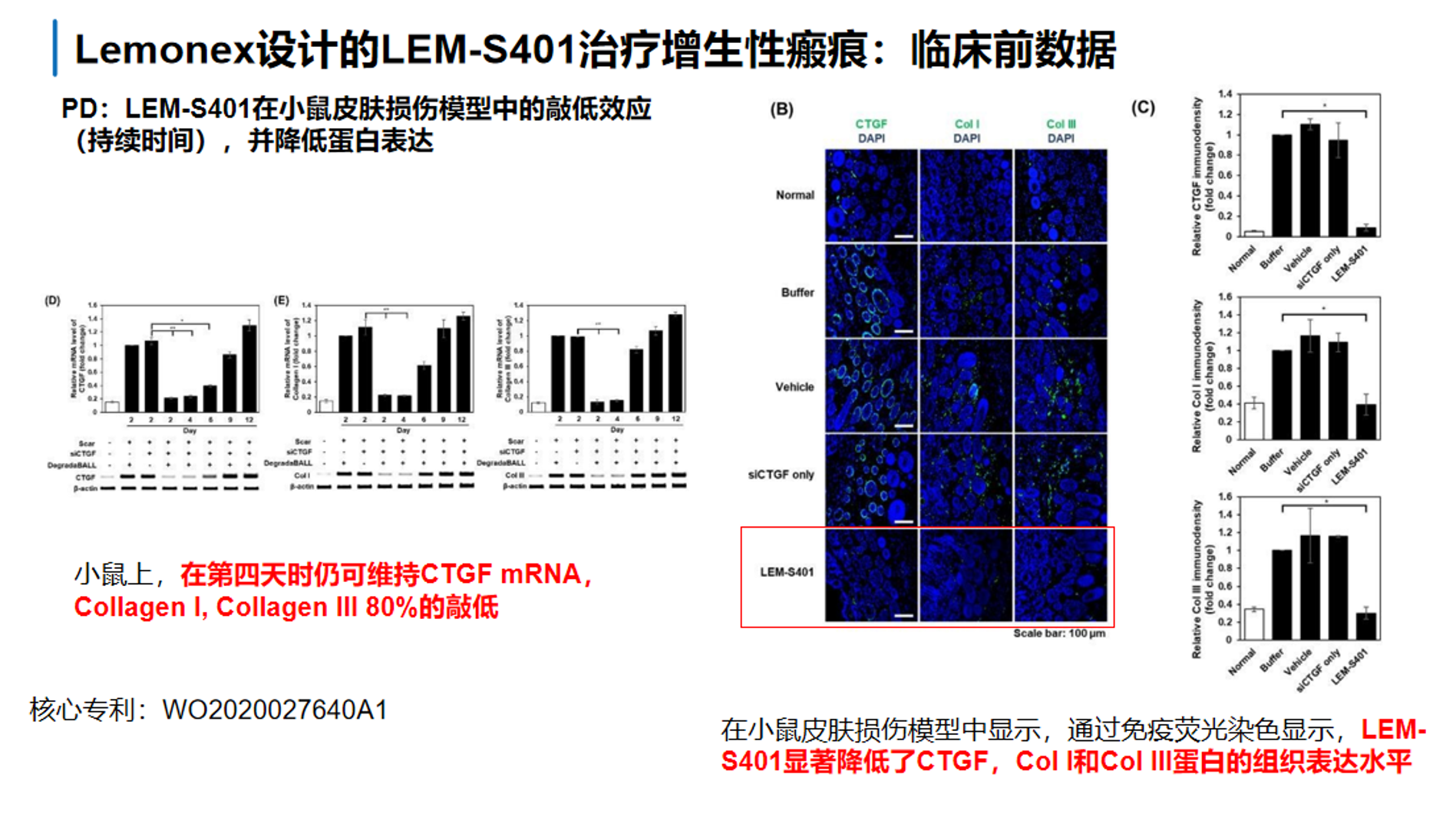
第四组图进一步说明LEM-S401的药效具有持续性,而且能在蛋白/组织层面被验证。在小鼠上第4天仍可见CTGF、Collagen I、Collagen III mRNA 明显下降,提示不是短暂抑制。右侧免疫荧光/免疫染色结果则表明,LEM-S401还能显著降低组织中的CTGF、Col I 和 Col III蛋白表达。也就是说,这个体系形成了完整链条:先在局部延长停留,再在细胞内持续释放,最终把 mRNA 层面的敲低转化成胶原相关蛋白下降和抗瘢痕组织学改善。
6.7 LEM-S401的临床数据
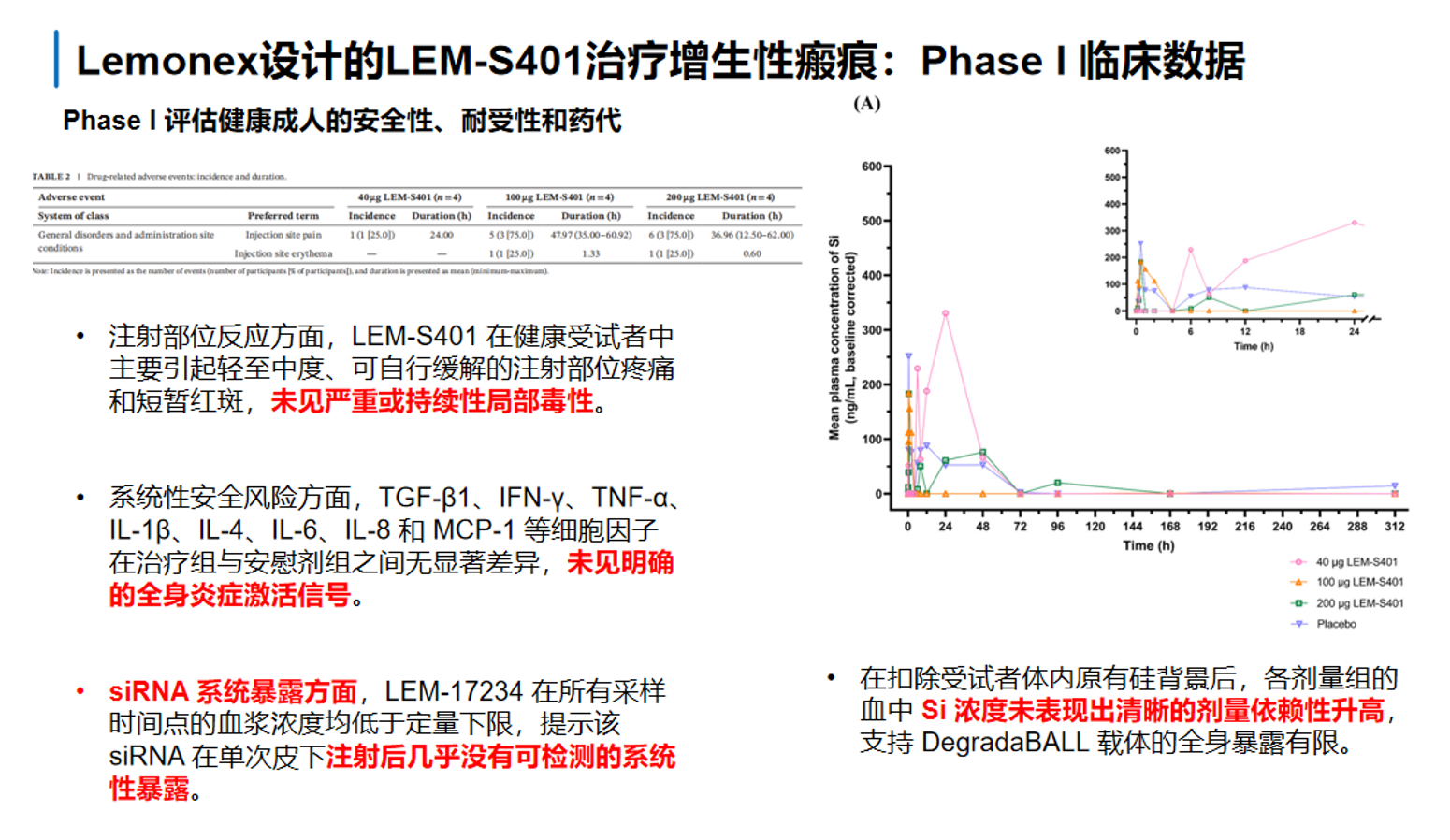
Ⅰ期临床结果总体表明,LEM-S401在健康成人中的局部给药具有较好的初步安全性和系统暴露受限的特点。从安全性看,主要不良反应集中在注射部位局部反应,包括短暂红斑、瘙痒或轻微疼痛,整体以轻中度为主,未见图中提示的严重全身性毒性信号。系统炎症方面,TGF-β1、IFN-γ、TNF-α、IL-1β、IL-4、IL-6、IL-8和MCP-1等细胞因子在给药前后未显示出明确异常升高,提示未观察到明显的全身炎症激活。药代方面,图中指出siRNA在多数样本中血浆浓度低于定量下限或仅短暂可测,说明系统性暴露非常有限;与此同时,右侧动力学图显示,与DegradaBALL载体相关的血中硅元素浓度仅在给药早期出现短暂、低水平升高,随后快速下降,也支持其全身暴露有限、主要以局部作用为主。整体而言,这组Phase I数据支持LEM-S401作为局部抗瘢痕siRNA制剂,具有较好的早期耐受性,并未显示出明显的系统性安全风险。
七、脑组织递送:多层级高门槛系统
7.1 脑组织递送的独特挑战与技术路线
脑组织siRNA递送的特别之处在于它面对的不是单一组织屏障,而是一个由血脑屏障、脑内细胞选择性和胞内释放共同构成的多层级高门槛系统。
首先,siRNA 分子量较大、带强负电、亲水性高,几乎不能依靠被动扩散穿过血脑屏障,因此系统给药后往往难以像肝脏那样自然进入靶组织;其次,即使药物进入脑血管侧,也还要跨越脑内皮细胞、避免被内体-溶酶体通路降解,并真正释放到脑实质中,而不是只停留在血管或血管周围区域。进一步而言,脑组织内部也并非均一环境,神经元、星形胶质细胞、少突胶质细胞、小胶质细胞等细胞类型差异很大,不同疾病对应的真正靶细胞并不相同,因此“进入脑”并不等于“进入正确脑细胞并起效”。
此外,中枢神经系统对炎症、免疫激活和局部毒性高度敏感,递送系统不仅要追求效率,还必须严格控制安全性和可转化性。也正因为如此,脑组织 siRNA 递送通常不能仅靠常规纳米颗粒思路,而更依赖于受体介导跨胞转运、鞘内/脑室内给药、细胞特异性配体偶联或高度工程化载体等策略,其核心难点不是单纯提高暴露,而是在保证安全的前提下,实现“跨 BBB-入脑实质-进靶细胞-出内体”这一整条链路的有效打通。
破解血脑屏障(BBB)是神经系统siRNA药物开发的首要难题。尽管后续还面临入胞、内体逃逸等多重障碍,但当前所有努力的焦点,都集中在如何实现高效的跨BBB脑实质递送。
当前siRNA跨BBB的技术路线主要包括:脑靶向肽、非肽的配体偶联、脂质/亲脂性缀合、病毒、外泌体、LNP等技术。其中,以TfR为靶点的AOC技术发展最为成熟,这主要源自TfR在其他modality,比如双抗等方面的快速发展对TfR的验证。接下来仍是以Arrowhead的TRiM BBB皮下给药平台以及相关的管线ARO-MAPT的相关信息。

7.2 TRiM-BBB的核心工程设计临床前结果
根据专利披露,TRiM™-BBB的核心工程设计为:通过单价 TfR(Transferrin Receptor)结合的 Fab 片段,将化学稳定的 siRNA 以不可逆共价方式偶联,构建具备系统给药能力的 BBB 转运 RNAi 分子。TRiM™-BBB 采用 单价 TfR binder(Fab)作为递送配体,其设计目标并非最大化受体结合强度,而是精确控制结合-解离动力学,以避免TfR二价交联引发的内吞-溶酶体降解通路。Fab与siRNA 之间通过化学稳定、不可逆的链接子连接,在保证血液循环稳定性的同时,避免体内siRNA的非特异性释放。这一设计在工程逻辑上与当前主流的单价 TfR 抗体穿梭策略保持一致,但其载荷由大分子抗体转变为siRNA,从而在机制上直接作用于神经元和胶质细胞内的mRNA 靶点。

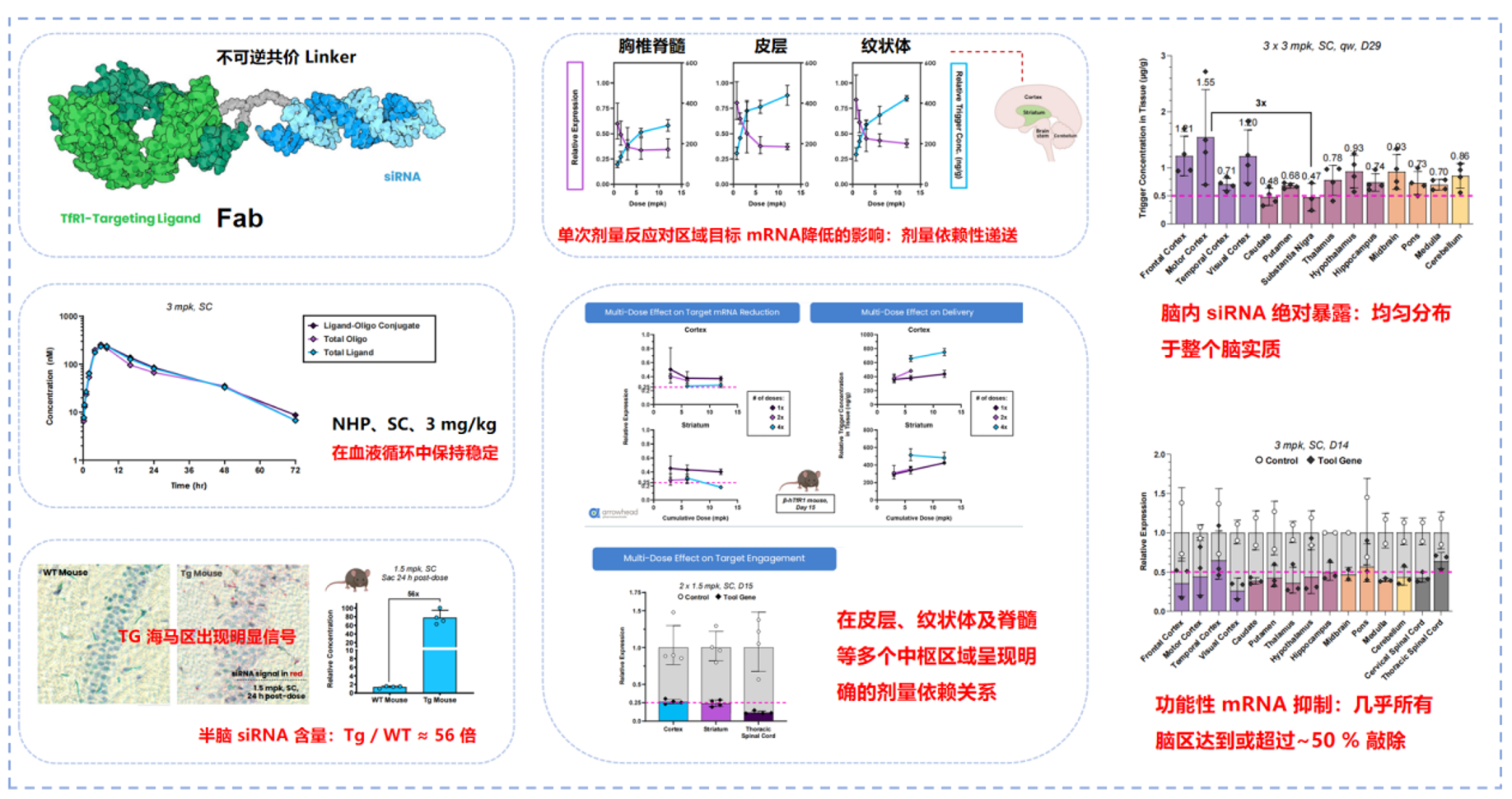
图14
Arrowhead 在非人灵长类动物中系统评估了 TRiM™-BBB 的脑内递送效率与功能性结果。数据显示,在皮下给药后,siRNA 能够在皮层、纹状体、丘脑、海马以及脊髓等多个 CNS 区域实现广泛且均一的分布。在单次给药条件下,不同 CNS 区域的目标 mRNA 敲低程度呈现明确的剂量依赖关系,多次给药实验进一步显示,TRiM™-BBB 在累积剂量增加的情况下,能够持续增强脑内暴露并加深 mRNA 抑制水平,且不同脑区之间的响应趋势高度一致(~50%)。
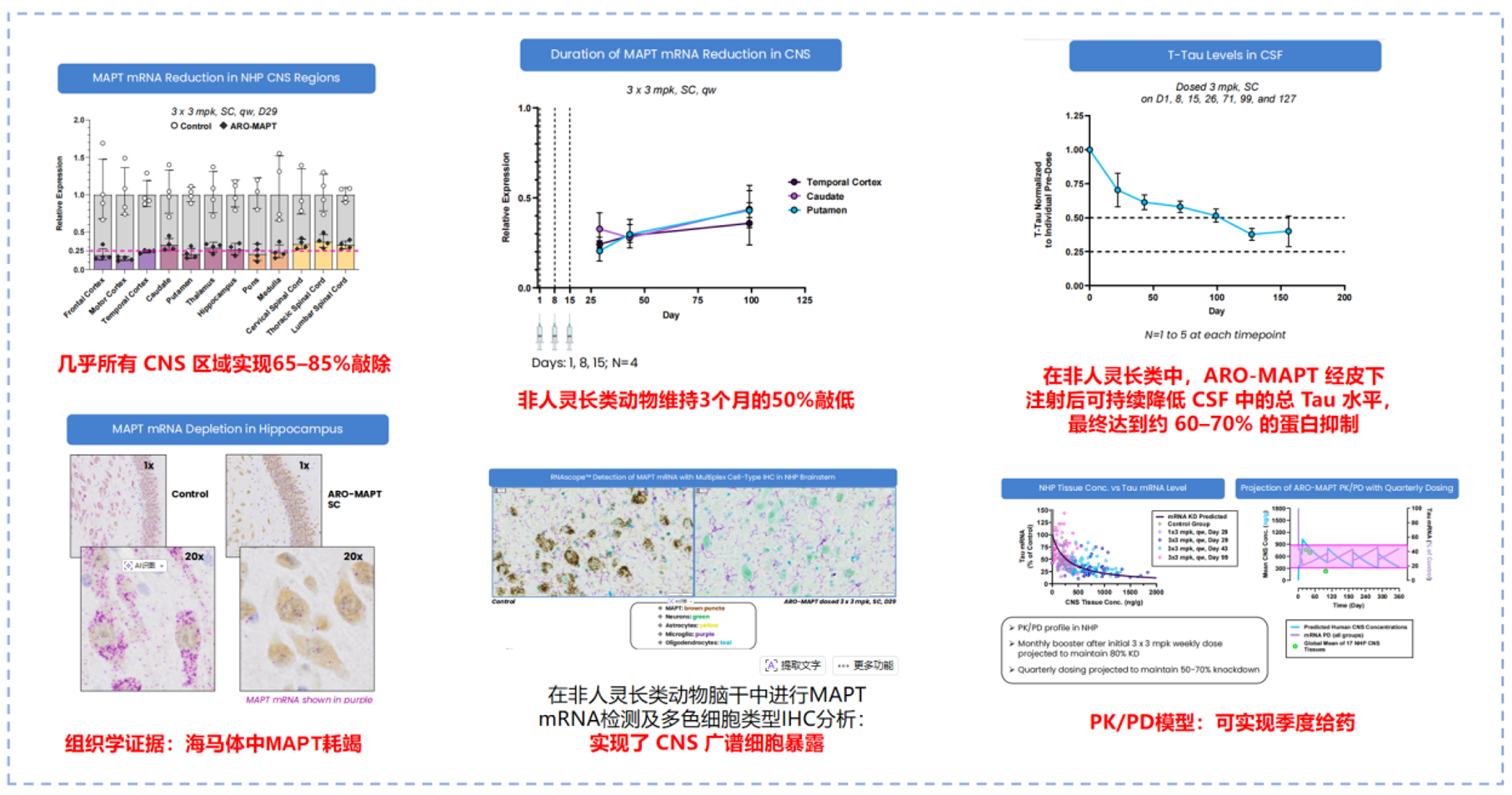
基于 TRiM™-BBB 平台,Arrowhead 开发了针对 MAPT(Tau)靶点的候选药物 ARO-MAPT,并将其作为 CNS 递送能力的功能性验证模型。在非人灵长类动物中,ARO-MAPT 经皮下给药后,不仅在几乎所有检测的 CNS 区域实现 65–85% 的 MAPT mRNA 敲低,而且该效应可持续 至少 3 个月。在脑脊液(CSF)层面,ARO-MAPT实现了总Tau 蛋白约 60–70% 的持续下降,证明 mRNA 层面的抑制能够有效转化为可测量的蛋白终点。组织学与原位检测结果显示,MAPT mRNA 的降低覆盖神经元及多种胶质细胞类型,支持 TRiM™-BBB 并非局限于单一细胞亚群,而是具备广谱细胞暴露能力。基于 NHP 数据构建的 PK/PD 模型显示,TRiM™-BBB 分子在外周血液循环中保持可控暴露的同时,其脑内 siRNA 浓度与 mRNA 抑制程度之间呈现良好的相关性。
模型推演表明,在完成初始加载剂量后,通过季度给药有望维持 CNS 内 50%~70% 的持续 mRNA 抑制水平,这一给药频率在慢性神经退行性疾病中具备显著的临床可行性优势。
八、总结与展望:肝外递送的产业拐点与未来图景
1.不同器官将逐步形成各自独立的专用递送范式,而非统一的万能平台
不同肝外器官之间的递送壁垒差异极大。骨骼肌递送因受体广泛表达且组织质量庞大,导致剂量-药效难以平衡;心脏因持续收缩与舒张,药物滞留效果较差;肾脏递送需要克服肾小球滤过屏障,同时还面临细胞类型多样的问题;肺部更强调深部沉积、上皮细胞靶向及局部持留;脑组织的核心障碍始终是跨血脑屏障;脂肪组织则同时受限于组织灌注差、细胞异质性强以及脂肪细胞自身摄取效率低下;皮肤则需先解决角质层屏障与局部组织扩散问题。
因此,未来技术发展大概率不会收敛为单一平台,而是形成“器官专属入口 + 工程化修饰”的格局。受体或配体介导的主动靶向仍将是主线,但不同器官会对应不同的受体、配体、连接方式及PK/PD调节策略。谁能率先在某一个器官中建立标准化、可复制的递送范式,谁就更可能成为该器官赛道的定义者。
2. 肝外siRNA的未来潜力,不止于补足肝外空白,更在于打开一批此前难以药物化的高价值适应症
从产业角度看,肝外递送的核心吸引力不仅在于技术本身,更在于其对应的疾病空间。肌肉和心脏方向对遗传性疾病、心肌病及慢性心衰具有明确吸引力;肺部方向有望覆盖哮喘、COPD、肺纤维化甚至感染性疾病;脑部方向指向神经退行性疾病等高壁垒领域;脂肪组织递送将减重、代谢综合征及脂肪相关慢病纳入RNAi的新战场;皮肤及局部组织递送则展现出小范围局部高效沉默的差异化价值。
换句话说,肝外递送一旦成熟,siRNA将不再只是肝脏药物的延伸,而可能成为一个覆盖慢病、遗传病、炎症性疾病及局部组织疾病的多器官治疗平台。这正是其产业拐点的真正含义。
3. 真正决定下一轮胜负的因素,将是工程化能力与产业化能力,而非单点药效数据
未来几年,真正能拉开差距的,往往是以下几个更硬核的问题:
种属转化的一致性:能否在NHP乃至人体中保持可预测的递送趋势,降低从小鼠到灵长类、从动物到人的种属差异失真。
化学制造与质量控制的可放大性:是否具备稳定、可放大的合成与纯化体系,包括偶联效率、杂质谱控制、连接子稳定性、DAR均一性及批间一致性。
药效生物标志物的桥接能力:能否建立可靠的生物标志物体系,将组织内靶点敲低水平与可检测的生物标志物可靠对应,这对无法反复活检的器官尤为关键。
长效性与安全性的动态平衡:能否在追求深度、持久敲低的同时,保持良好的安全性。
专利布局的纵深与自由度:是否在核心配体结构、连接子化学、偶联位点、适应症组合及给药方案上形成了足够宽阔的护城河,同时规避了领先者的FTO风险?
适应症选择的精准度与扩展性:是否选择了受体高表达、病理机制明确、部分敲低即可获益的“黄金适应症”作为突破口,同时保留了向邻近适应症扩展的模块化能力。
剂量-敲低-安全性的三角优化:能否在最低有效剂量、最大敲低深度与可接受安全窗口之间找到可持续的甜蜜点,而非靠高剂量换取药效。
4. 从产业图景看,肝外递送正处于从概念验证向临床转化过渡的关键拐点
当前,技术价值已获初步确认,但产业格局远未固化,呈现出三个特征:
平台型公司主导技术路线定义,但尚无赢家通吃;临床前数据丰富,但大多数平台仍处于I期或临床前阶段,临床验证依然稀缺;适应症选择呈现“聚焦罕见病、试探慢性病”的双轨策略:短期价值由罕见病管线释放,长期天花板则取决于慢性病市场的打开速度。
因此,对于具备技术能力的后来者而言,结构性机会窗口仍然存在。同时,未来几年极有可能出现更多围绕肝外递送平台的合作、授权与并购,交易逻辑也将从单纯引进管线,逐步转向通过收购争夺平台级Biotech。
欢迎交流|研究与合作对接
如您对肝外siRNA递送的技术路线有进一步研究需求,或希望探讨濠麦科技在专利情报、技术评估及投资研判方面的合作,欢迎随时联系并获取本报告的原始PPT文件。与此同时,我们正依托该框架持续挖掘并更新中国本土肝外siRNA潜力平台公司,筛选早期具备投资与合作开发潜力的机构。
关于濠麦科技
濠麦科技专注于生物医药领域,致力于通过大数据挖掘与分析、生物化学信息深度建模,结合人工智能工具,为药物发现提供深度技术服务。公司已建立靶点价值评估、资产价值评估关联、专利核心化合物预测等多个研发模型,至今服务超过30家医药上市企业及近100家生物医药企业,助力客户把握创新药发展机遇。团队成员中博士占比超过70%,学术背景覆盖药物化学、药理学、生物信息学及分子生物学等关键领域。
依托技术积累与创新团队,濠麦科技发展出三大业务方向:
濠麦咨询:聚焦创新药管线规划、靶点挖掘与立项评估。通过大数据分析与专家战略洞察,为企业提供立项筛选、研发策略优化及风险评估,发现差异化机会,规避专利与投资风险。
濠麦孵化:依托大数据预测与全球BD资源,挖掘与评估早期生物医药资产及技术平台,提供从立项到研发策略的全方位孵化服务,助力成果转化与价值落地,精准对接潜在合作方。
濠麦会员:依托自研技术矩阵及专家网络,提供跨国药企及肿瘤、自免、代谢等核心领域的深度立项与交易研究报告,助力会员低成本获取高价值的立项与投资洞见。
欢迎交流探讨
蔡鸿 技术挖掘与研判部负责人
电话:18578675942
邮箱:alex@hq-haomai.com
编辑 | 毛冬蕾
mao.donglei@PharmaDJ.com
访问研发客网站,深度报道和每日新闻抢鲜看