• 默沙东PD-1/VEGF双抗MK-2010的初步临床数据尚未展示出远超竞品的潜力;
• BioNTech与基因泰克联合开发的治疗性mRNA癌症疫苗公布Ⅰ期临床6年长期随访结果;
• RAS抑制剂和肿瘤疫苗打破胰腺癌多年治疗僵局;
• 多项肺癌耐药新药数据公布,覆盖EGFR、KRAS、ROS1等靶点。
2026 AACR上,肺癌赛道聚焦EGFR、KRAS等耐药靶点继续攻坚;胰腺癌领域则针对“免疫沙漠”微环境、RAS通路等硬核难题,肿瘤疫苗与新型靶向药取得了重要突破。本届AACR展现的新数据,在破解这两大癌种临床困局的进程上又往前了一步。
拓展阅读

默沙东虽迟但到
在PD-1/VEGF赛道起步较晚的默沙东,在本届AACR上首次披露PD-1/VEGF双抗MK-2010(LM-299)的初步临床结果。数据显示,针对非小细胞肺癌(NSCLC),MK-2010与该领域的领先药物相比,具有相似的安全性和有效性。默沙东认为,现有数据可以支持继续探索MK-2010单药及联合用药方案。
一项在中国开展的Ⅰ/Ⅱ期临床试验中,MK-2010在NSCLC扩展队列的初治患者中,20 mg/kg Q3W组的未确认客观缓解率(ORR)为55%,30 mg/kg Q3W组为44%。
MK-2010的ORR水平,与康方/Summit的同类首创双抗依沃西单抗、BioNTech/BMS的pumitamig,以及辉瑞/三生制药的PF-08634404等多款 PD-(L) 1/VEGF双抗在NSCLC一线治疗中的早期数据相近,但MK-2010目前研究数据尚处于早、入组患者样本量有限,且各项试验中鳞癌与非鳞癌、不同PD-L1表达水平患者的占比存在差异,暂无法据此得出切实可靠的有效性对比结论。
拓展阅读
康方/Summit双抗数据发布:PFS显著改善,错过OS,仍有可能获批
安全性方面,MK-2010 的不良反应以VEGF通路抑制剂典型问题为主,包括蛋白尿、高血压和出血。
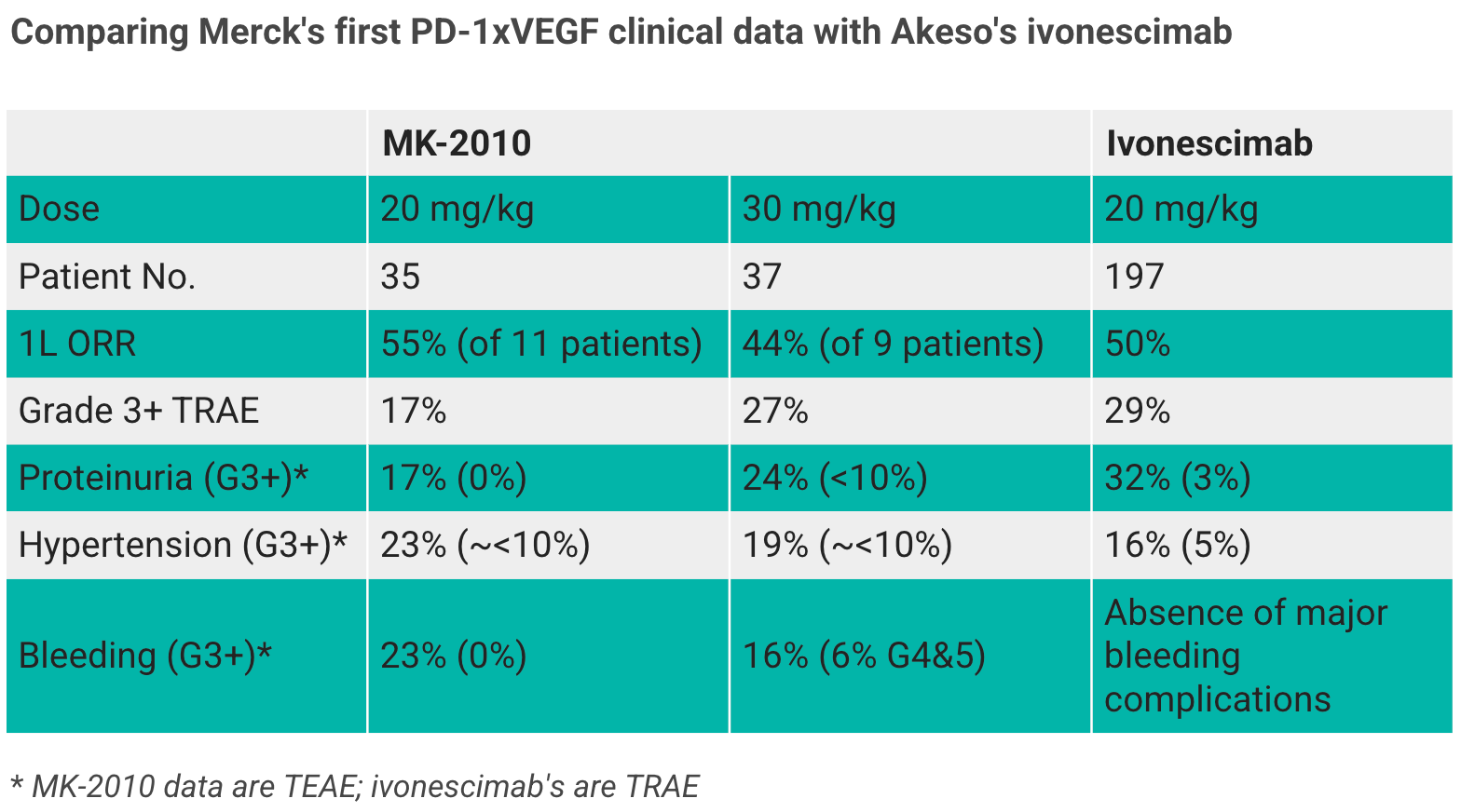
来源|Fierce
2024年,康方生物的依沃西“头对头”击败Keytruda之后,默沙东斥资超32亿美元从礼新医药获得了MK-2010的全球独家权益。目前,默沙东尚未公布该药物的III期计划,而依沃西单抗、pumitamig、PF-08634404等同类竞品已广泛布局多癌种关键III期临床试验,依沃西单抗已向FDA递交了上市申请。
与此同时,默沙东在肺癌领域的研发重心似乎有意放在与科伦药业合作的TROP2 ADC药物,这让外界质疑其在PD-1/VEGF双抗赛道的投入决心。不过有机构分析师认为,凭借强大的肿瘤研发实力,默沙东若有意发力,仍可快速追赶行业竞品。
围剿肺癌耐药
围绕肺癌耐药这一未竟临床难题,德昇济医药、翰森制药、劲方医药、Revolution Medicines、Nuvalent等中外药企披露了一批具有突破性的临床与临床前数据。
翰森制药口头报告第四代EGFR TKI抑制剂HS-10504针对EGFR C797S突变(三代靶向药核心耐药突变)的晚期NSCLC患者首次人体Ⅰ期研究数据。这类患者预后较差且目前尚无靶向治疗选择。结果显示,在推荐的II期剂量(RP2D)400 mg每日一次(QD)口服剂量下,客观缓解率(ORR)为52.9%,中位无进展生存期(mPFS)为9.6个月。
Vernalis的VRN110755同样在多种靶向药耐药肺癌患者(包括C797S突变)中展现比较明确的抗肿瘤活性,同时对脑转移病灶具备治疗潜力。在Ⅰa期REACH-EGFR试验里,8名可评估疗效的患者中有7人肿瘤大幅缩小,且该药对携带最难治的C797S突变患者也有效。
德昇济医药公布了下一代KRAS G12C抑制剂Elisrasib(D3S-001)针对既往接受过免疫治疗和/或化疗的局部晚期或转移性NSCLC的I/II期研究数据,初治患者ORR为 58.8%、mPFS为12.2个月,既往经KRAS G12C抑制剂治疗的耐药组ORR为32.3%,展现出比第一代KRAS G12C抑制剂显著更高的缓解率和更持久的肿瘤响应,且安全性和耐药性良好。
Revolution Medicines披露Zoldonrasib(RMC-9805)针对KRAS G12D 突变晚期实体瘤I期研究数据。结果显示,在27例既往接受过免疫和化疗、但未使用过多西他赛的KRAS G12D突变NSCLC患者中,确认的ORR为52%,疾病控制率高达(DCR)93%,中位无进展生存期(mPFS)为11.1个月,中位总生存期(OS)尚未达到,预计12个月OS为73%,疗效具有优于现有G12C抑制剂的潜力。
劲方医药融合RAS和ADC双路线开发了GFS784。GFS784由分子胶Pan RAS(ON)抑制剂与西妥昔单抗连接构成,临床前研究数据显示其在RAS突变、及DXd敏感或耐药模型中均展现强效活性,且对EGFR突变和TKI耐药模型亦有抑瘤活性,有望以单药治疗带来超越两药联用的ADC治疗方案。
信达生物以口头报告和壁报形式发布了新一代ROS1 TKI抑制剂taletrectinib关键研究长期随访数据。结果显示,TKI初治患者中位持续缓解时间(mDOR)近50个月,mPFS达46.1个月,ORR达89.8%。taletrectinib还展现出强大的中枢神经系统活性,在未经TKI治疗且伴有脑转移的患者中颅内缓解率达76.5%,在经TKI治疗且伴有脑转移的患者中这一比例为65.6%。
Nuvalent公布了zidesamtinib治疗晚期ROS1阳性NSCLC的研究更新数据,其中包含既往接受Augtyro或Ibtrozi治疗的耐药患者亚组结果。两个亚组的ORR分别为41%和47%,亚组中脑转移患者的ORR高于整个亚组,分别为44%和71%。Augtyro经治患者的mDoR为15.7个月,Ibtrozi经治患者的mDoR暂未达到。
对于ROS1基因突变的NSCLC,已有辉瑞的Xalkori、罗氏的Rozlytrek和BMS的Augtyro获批,但市场表现并不理想。taletrectinib已在中国、美国等地获批上市,zidesamtinib预计在今年9月获批,有望为这类患者带来新的治疗希望。
不止RAS,还有肿瘤疫苗
据美国癌症协会发布的《2026年癌症统计报告》,胰腺癌的五年生存率约为13%。胰腺癌因致密纤维化间质、免疫细胞极度匮乏及强免疫抑制微环境,是典型的“免疫沙漠”型冷肿瘤,几乎不响应单药免疫检查点抑制剂。过去十年,几乎所有胰腺癌新药都没能挺过Ⅲ期。
终于,RAS抑制剂和肿瘤疫苗在这个“癌王”身上撕开了两道口子。
2026 AACR上,Revolution更新了pan-RAS (ON)分子胶daraxonrasib(RMC-6236)的I/II期临床数据。结果显示,一线未经治疗的RAS突变转移性胰腺导管腺癌患者,RMC-6236单药展现出亮眼的早期抗肿瘤疗效,ORR达47%,含1例完全缓解,DCR高达92%。截至2025年12月1日数据锁定时,mPFS和mOS 暂未成熟,预计6个月PFS为71%,OS 为83%。联合化疗的表现也不错,单药和联合化疗的安全性和耐受性均可控。
目前daraxonrasib正在全球开展四项III期临床试验,三项针对胰腺癌(两项正在进行,一项已完成),一项针对NSCLC。该公司近期宣布,针对既往接受过治疗的转移性胰腺癌患者的关键性III期临床试验RASolute 302已达到所有主要终点和关键次要终点,包括PFS和OS。在该试验中,daraxonrasib在所有入组患者(不论是否存在RAS突变)中均展现出前所未有的OS获益。
中国公司奋力追赶,RAS抑制剂后继者在本届AACR亮相。
劲方医药在壁报中展示其口服Pan RAS(ON)抑制剂GFH276在多种RAS突变的胰腺癌、非小细胞肺癌和结直肠癌动物模型中的实验数据。据劲方医药新闻稿,GFH276具有以低至1/3剂量即可达到或超越RMC-6236抑瘤效果的潜力。此外,劲方还公布了口服 KRAS G12D(ON/OFF)抑制剂GFH375/VS-7375的临床前数据,展示了GFH375在抗肿瘤活性、靶点选择性、信号通路抑制的持久性、抗耐药和联合用药等方面的竞争优势。
和誉医药公布了小分子pan-KRAS抑制剂ABSK211的临床前数据,ABSK211在多种RAS突变模型中展现出显著而稳定的抗肿瘤药效。相关结果支持ABSK211向临床阶段推进,目前正处于IND申报支持研究阶段。
拓展阅读
如果说KRAS抑制剂是绕开免疫系统、直接阻断驱动突变的精准拆弹,那么肿瘤疫苗则是直击胰腺癌“免疫沙漠”,把 “冷肿瘤” 变 “热”,在“荒漠”里种下可持续的抗肿瘤免疫生态。
美国纪念斯隆・凯特琳癌症中心的Vinod Balachandran 团队公布了由BioNTech与基因泰克联合开发的治疗性mRNA癌症疫苗autogene cevumeran (BNT122,RO7198457)Ⅰ期临床6年长期随访结果,是本届AACR胰腺癌领域除RMC-6236外最具里程碑意义的成果。
该研究纳入16例可切除胰腺导管腺癌患者,采用手术+PD-L1抑制剂阿替利珠单抗+定制mRNA疫苗+化疗的序贯组合方案。结果显示,疫苗激活了8例(50%)患者的肿瘤特异性免疫细胞。4~6 年随访约7人存活且无复发,生存率87.5%,中位无复发生存期(mRFS)未达到。无应答患者者2人存活,中位总生存期约3.4年,mRFS为13.4个月。
目前,验证该方案的全球Ⅱ期试验正在推进,未来有望成为可切除胰腺癌术后新标准辅助方案,改写胰腺癌免疫治疗无效的历史认知。
结合本届AACR上的其他胰腺癌研究来看,该领域的研发思路已从过往单一药物单打独斗,迈入靶向-免疫深度协同新阶段,治疗场景也从晚期姑息治疗延伸至术后长效防复发,胰腺癌的治疗格局正在被彻底改写。
编辑 | 姚嘉
yao.jia@PharmaDJ.com
访问研发客网站,深度报道和每日新闻抢鲜看